מחקר שפורסם לאחרונה ב- Journal of Clinical Investigation סקר את העדויות על הפרעה ביממה, בריאות מטבולית ומחזורי תפוקה של תנועה צירקדית גנים קפוט (שעון).
שגרות החיים היומיומיות קשורות לדפוסי הסביבה, וכתוצאה מכך לאבולוציה של מקצבי יממה. רמזים כמו טמפרטורה, אור שמש, מזון וקול, הנקראים zeitgebers, מתאימים את המקצבים הצירקדיים לתנאים חיצוניים. עדויות הולכות וגדלות קושרות משבשי יממה או זמני זמן לתוצאות שליליות בבני אדם.
סקירה מקיפה של הקשר בין בריאות מטבולית וביטוי גנים צירקדי חסר. ככזה, המחקר הנוכחי סיכם והשווה ראיות ממודלים של בעלי חיים עם ממצאים ממחקר אפידמיולוגי כדי לקדם את ההבנה של התרומה של שיבוש יממה וביטוי גנים של שעון לפתולוגיות הקשורות לבריאות מטבולית.
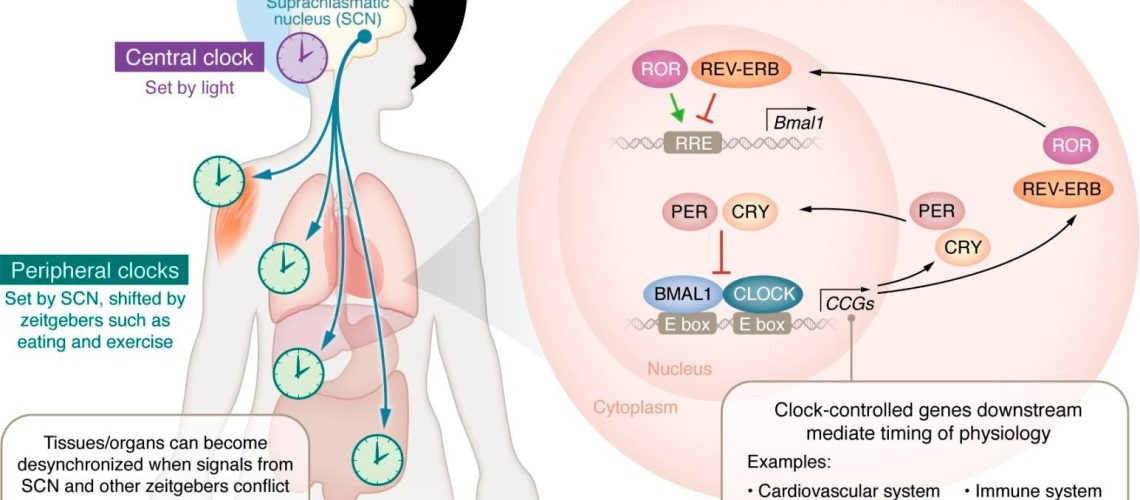
שליטה יממה של איתות גן שעון ליבה מולקולרית וויסות פיזיולוגי. השעונים המרכזיים, ההיקפיים והמולקולריים והתהליכים הפיזיולוגיים בשליטה צירקדית. השעון הצירקדי (סגול) בגרעין העל-כיאסמטי (SCN) של המוח קובע שעונים היקפיים באיברים ובסוגי רקמה בודדים (ירוק בהיר) באמצעות אותות הכוללים הורמונים במחזור, מטבוליטים, מערכת העצבים הסימפתטית וטמפרטורת הגוף. בתוך התאים של ה-SCN ובכל סוג איבר/רקמה, כל תא מכיל לולאות משוב לתעתוק-תרגום, השעונים המולקולריים המניעים את המקצבים הצירקדיים. שעונים מולקולריים אלו מווסתים את השעתוק של אלפי CCG ומכוונים את הביטוי התנודתי היומי של אלפי COG וגורמי שעתוק נוספים המתווכים את התזמון של אינספור תהליכים פיזיולוגיים כפי שמיוצגים במסלול השעון המולקולרי בתוך התאים. לימוד: הפרעה ביממה, גנים של שעון ובריאות מטבולית.
מקצבי יממה במודלים של בעלי חיים
מניעים גנטיים של מקצבי יממה בבעלי חיים התגלו לראשונה בזבוב הפירות, תסיסנית מלנוגסטרשחשף כי הגן התקופה (לְכָל) וחלבון (PER) היו חיוניים לשעון הצירקדי. מחקרים נוספים אימתו את הממצאים הללו וגילו גם גנים נוספים של שעון ליבה (CCG), דמויי ARNT 1 של המוח והשריר (BMAL1), קריפטוכרום (בוכה), ו לְכָל אורתולוגים (PER1 – PER3).
ב שָׁעוֹן מודל של עכבר גנטית, בעלי חיים הראו תזמונים משתנים של צריכת מזון עם האכלה אד ליביטום וצרכו יותר קלוריות מעבר לשלב הפעיל; הם פיתחו תסמונת מטבולית והשמנת יתר והפחיתו את מקצבי הפעילות. שינויים מטבוליים דומים צוינו במודלים אחרים של עכברים עם מוטציות ברכיבי שעון מולקולרי.
הומאוסטזיס של גלוקוז מושפע ממנגנוני איתות גנים ספציפיים לתא המווסתים על ידי CCGs ספציפיים. מחקר מצא כי בתאי β בלבלב של עכברים עם ביטוי BMAL1 שלם, דימרי BMAL1/CLOCK נקשרו לאתרים רגולטוריים, כלומר, CCGs, המניעים שעתוק של מטרות (גנים פלט שעון), שונים מתאי הכבד. לעומת זאת, אלו עם BMAL1 מופרע פיתחו אי סבילות לגלוקוז.
רוב אתרי הקישור ל-BMAL1/CLOCK בתאי β אינם מזוהים ברקמות אחרות, מה שתומכים בתפקיד ספציפי לרקמות של השעון בבריאות המטבולית. מאמצים ניכרים הושקעו בחקר ההשפעות של משבשי יממה בעכברים, כולל שינוי בפעילות, שינה, חשיפה לאור וצריכת מזון. מחקרים המחקים חשיפה לעבודה במשמרות דיווחו כי משבשי יממה עלולים לשנות את ביטוי ה-CCG ואת הבריאות המטבולית.
יתר על כן, עכברים מסוג פרא עם תזמון צריכת מזון שגוי ביחס לתקופות לא פעילות ופעילות הפגינו עלייה מואצת במשקל. עכברים שצרכו דיאטה עתירת שומן בתקופות לא פעילות היו בעלייה במשקל גבוה יותר ואחוז שומן בגוף מאלה שניזונו באותה תקופה בתקופה הפעילה שלהם. בניגוד לכך, עכברים שניזונו בתזונה עתירת שומן עם האכלה מוגבלת בזמן היו מוגנים מפני עלייה במשקל.
עדויות ממחקר אפידמיולוגי ומבוסס אוכלוסיה
עדויות ראשוניות מצביעות על כך שהבריאות המטבולית משתנה עקב הפרעה צירקדית מניתוחים אפידמיולוגיים של עובדי משמרות. מחקר האחיות ציין כי לנבדקים שנחשפו לעבודה במשמרות לילה יש צריכת קלוריות גבוהה יותר, משכי שינה קצרים יותר וסיכויים מוגברים להשמנה. מחקר אחד מצא רמות גרלין גבוהות יותר לאחר ארוחה וקסנין נמוך יותר (הורמון שמקורו במעיים) בזרם הדם אצל עובדים במשמרות לילה.
יתרה מכך, 21 מבוגרים היו נתונים להפרעה צירקדית (הגבלת שינה). שלושה שבועות לאחר מכן, מבוגרים עם הפרעה ביממה הפחיתו משמעותית את קצב חילוף החומרים במנוחה ורמות גלוקוז בצום/אחרי ארוחה גבוהות יותר בהשוואה לבסיס; שינויים אלו נרמלו תשעה ימים לאחר החזרה לדפוסי ערות/שינה סטנדרטיים.
ביטוי CCG והפרעה ביממה
מחקר שכלל 18 אחיות ציין פחות גנים קצביים בתאים חד-גרעיניים בדם היקפי של עובדי משמרות לילה סיבוביות מאשר עובדים במשמרות יום. מחקר אחר שכלל 60 אחיות חשף ביטוי דיפרנציאלי של כמעט כל ה-CCGs. במחקר נפרד, 22 אנשים היו נתונים לסינכרון מאולץ של 28 שעות ימים, והתחלת השינה נדחפה ארבע שעות בכל לילה.
בעוד שמקצבי המלטונין של 24 שעות נשמרו ברובם, לתמלילים הצירקדיים הייתה הפחתה של עד פי שישה. יתר על כן, אלפי תמלילים שינו ביטוי במחקר עם 26 אנשים מוגבלי שינה, עם PER1, PER2, PER3, CLOCK, ו CRY2 מושפע באופן משמעותי. יתרה מכך, גנים רבים של מתח מטבולי וחמצוני שונו גם הם עם הגבלת שינה.
פתולוגיה מטבולית ו-CCGs
יתכן קשר דו-כיווני בין ביטוי CCG לבריאות מטבולית, שכן החמרה בבריאות המטבולית, כְּשֶׁלְעַצמוֹ, יכול לשנות את ביטוי CCG באופן ספציפי לרקמות. מחקר עם 28 נשים עם השמנת יתר חולנית ו-21 נשים רזות שאינן עובדות במשמרות ללא סוכרת חשף ביטוי שונה של CCGs שונים בנבדקים שמנים. עדויות נוספות מצביעות על כך שירידה במשקל יכולה לשנות את ביטוי CCG.
יתרה מכך, מחקרים העלו שאפילו חשיפה לטווח קצר למשבשי יממה עלולה לשנות את ביטוי ה-CCG ואת המסלולים המטבוליים. מחקר אחד של 14 גברים בריאים איפשר שלושה ימים של שינה רגילה והפך את לוחות הזמנים של היום והלילה לשלושת הימים הבאים. חומצות שומן חופשיות ורמות גלוקוז בצום היו גבוהות משמעותית לאחר הפרעה מאשר בתנאים רגילים.
הערות לסיום
גוף גדל והולך של עדויות קושר בין פעילויות שעון לתוצאות מטבוליות פתולוגיות. מפרדיגמת סיכון, ההשפעה של משבשי יממה תלויה במשך החשיפה ובאיכות. דוגמה לכך תהיה עבודה במשמרות לסירוגין. במודל של דה-סינכרון של רקמות, הפרופילים המטבוליים של הרקמות אינם מיושרים עקב זמני תגובה דיפרנציאליים הדרושים לשיקום מקצבים נורמליים בעקבות חשיפה לא הולמת של צייטגבר או הפרעה ביממה.
תקופות ממושכות של עבודה במשמרות לסירוגין עשויות שלא לאפשר ריחוף של איברים פנימיים. יתר על כן, עבודה במשמרות אינה תמיד שם נרדף לחוסר סנכרון צירקדי, מכיוון שיכולים להיות עובדים במשמרות עם היגיינה צירקדית מתאימה. לפיכך, הגילוי של מרכיבים של אי-התאמה צירקדית תורמים לבריאות לקויה הוא מורכב. בסך הכל, יש צורך במחקר נוסף כדי להרחיב את בסיס הראיות ולקדם את ההבנה של קשרים אלה.