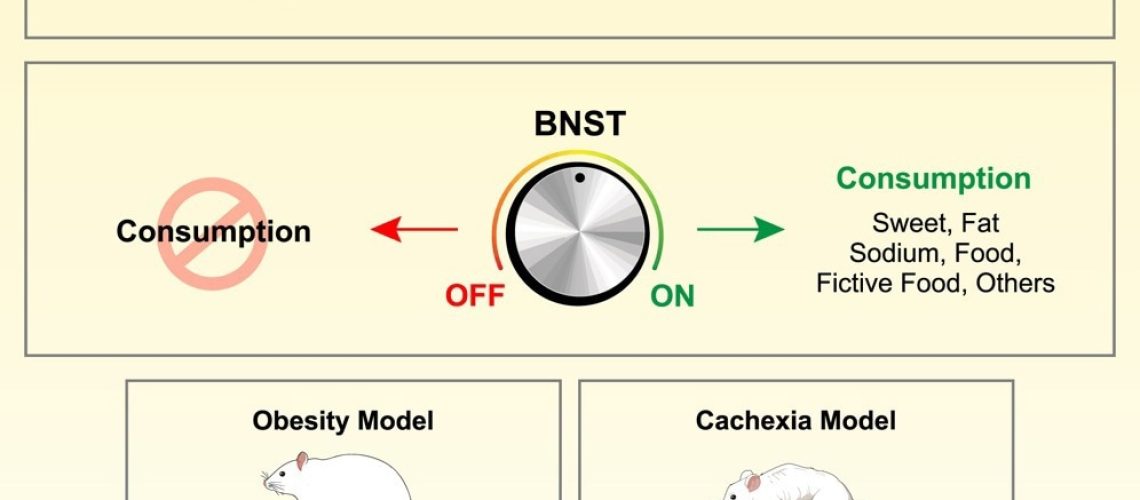
מדענים חשפו כיצד גרעין המיטה של המוח של ה- Stria terminalis משמש כמרכזיה של אב, מיזוג תגמול וזקוק לאותות כדי לשלוט באכילה, תגלית שיכולה להנחות טיפולים חדשים להשמנה וירידה במשקל הקשורה למחלות.
לימוד: מרכז מוח השולט בתגובות השלמה
במחקר שפורסם לאחרונה בכתב העת תָאקבוצת חוקרים בדקה האם גרעין המיטה של ה- Stria terminalis (BNST) משלב פרודינורפין מרכז אמיגדלה (CEA) (CEA) (CEA) (פדין) ואותות פפטיד הקשורים להיפותלמי (AGRP) כדי לשלוט בצריכה, עם השלכות במורד הזרם על משקל הגוף.
רֶקַע
התשוקה נראית פשוטה-ראה סוכר, רוצה סוכר-אך הבחירה לצרוך בפועל היא משא ומתן מוחי. אנשים מרגישים את זה כאשר קינוח אינו ניתן לעמוד בפניו בעודם רעבים, ובכל זאת נשכחים אחרי ארוחת הצהריים. בריאות הציבור מרגישה שזה בין השמנת יתר, טיפולי סרטן מתנפחים על ידי תיאבון ותרופות לשובע. נשאלת שאלה: היכן "זה טעים" ו"גוף שלי צריך את זה "עונים? ה- BNST הוא מרכזיה המשלבת ערכיות חושית עם מצב פנימי לוויסות הצריכה. הידיעה כיצד עבודות זו יכולה לעזור נגד ירידה במשקל הקשורה למחלות ולשכלל טיפולים נגד השמרה. יש צורך במחקר נוסף כדי למפות את הספציפיות של קלט וכללים תלויים במדינה על פני חומרים מזינים.
על המחקר
החוקרים זיהו תחילה נוירונים של CEA המקודדים ערכיות מתוקה באמצעות רצף חומצות ריבונוקלאיות של ACT-SEQ יחיד (scRNA-seq) וגן מיידי-מדרג FOS ביטוי משותף כדי לזהות נוירונים CEA המתוקים המבטאים FOS ו- FOS ו- FOS פדיןו הם רשמו פעילות מנוירונים אלה עם נגיף הקשור לאדנו (AAV) שהועברו באופן מעגלי חלבון פלואורסצנטי ירוק-קלמודולין-M13 פפטיד סידן 6S (GCAMP6S) ופוטומטריה של סיבים תוך כדי העברת טעימים באמצעות פיסטולה תוך-אורלית. כדי לבחון את הסיבתיות, הם הביעו את Channelrhodopsin-2 (Chr2) או את האניון המעכב Channrhodopsin gtacr2 ב- פדין נוירונים והפעלה או השתקה משולבת ללקק או למשימות לחיצה מנוף. מעקב אחר התחקות של אנטרוגרד ממופה תחזיות מ- CEA פדין נוירונים ל- BNST. התגובות בתוך ה- BNST נסוגו על ידי מיקוד לאוכלוסיית הטרנספורטר החומצה החומצתית של גמא-אמינובוטירית (VGAT) וביצוע פוטומטריה של סיבים ואופטוגנטיקה.
ההתכנסות של אותות מצב פנימי נבדקה באמצעות כלבת מונוסינפטית שמתחקות אחר נוירונים של BNST VGAT ועל ידי נוירונים מפוזרים באופטוגנטית של AGOUTI (AGRP) בגרעין הארקאט (ARC) שמביעים את Chrimsonr. הדמיית סידן מיקרו-אנדוסקופית עם עדשת שבירה של שיפוע (GRIN) קידוד אנסמבל מכמות במצבים פד, רעבים ונתרן. לבסוף, כימוגנטיקה (קולטני מעצבים מופעלים באופן בלעדי על ידי תרופות מעצבים (DREADDS), HM3DQ; Clozapine N-Oxide (CNO)) ומודול מפעיל פרמקולוגי מבחינה פרמקולוגית 4–4-GLYCINE SELETOLE COLETORITOL (PSAM4-GLYR) פלוס אולטרפוטציה של אולטרפוטציה (PSAM4-GLYR). אפנון BNST משנה את צריכת המזון ואת משקל הגוף בעכברים שטופלו בציספלטין או עם דיאטה-נשמנת.
תוצאות המחקר
פדין-נוירונים חיוביים במשיכה המקודדת של CEA ל- Sweet: הפעלה אופטוגנטית עשתה מים ניטרליים אחרת מבוקשים מאוד, והשתקה בוטלה העדפה הן לממתיק מלאכותי והן לסוכר תוך השארת העדפת השומן שלמה, ומדגימה את הספציפיות של המודוליות. תחזיות צפופות מ- CEA אלה פדין נוירונים ל- BNST מיפו; בתוך BNST, נוירוני VGAT הגיבו בחוזקה וסלקטיבית לגירוי מתוק. גירוי אופטוגנטי של פדין הטרמינלים ב- BNST הגדילו את הליקוק למים, וביססו קשר סיבתי בין קידוד מתוק של אמיגדלה וצריכה; לעומת זאת, עיכוב נוירונים של BNST VGAT דיכא את צריכת המתוק. חשוב לציין כי פדין למעגל Bnst לא הניע ליקוח יבש כאשר לא היה נוזל זמין, מה שמצביע על השלמה ולא על חיפוש תגמול טהור, ואילו הפעלה פדין Somata ב- CEA אכן מעורר גירוי עצמי של ליקה יבשה על ידי מעורבות יעדים נוספים הקשורים לתגמול.
מצב פנימי משקל בעוצמה את עיבוד ה- BNST. רעב מוגבר תגובות מתפתחות מתוקות ב- BNST והגביר את הצריכה בכ- 250-300%, בעוד עכברי נוקאאוט של TRPM5 לא הראו השפעה זו; גירוי כניסות AGRP ל- BNST בעכברים מחודדים חיקו שיפור זה, וגייסו נוירונים BNST מתוקים שקטים בעבר ותומכים בהתכנסות של טעם וזקוקים לאותות בתוך BNST. מעקב מונוסינפטי רטרו -סינפטי אישר כניסות ישירות מה- CEA והקשת לנוירונים VGAT BNST. מעבר לרעב, דלדול הנתרן הגדיל באופן סלקטיבי את התגובות של BNST לנתרן כלוריד (NACL) ב- ~ 300% והעביר התנהגות לעבר חיפוש מלח, וחשף שערים ספציפיים למצב לצורך.
ברמת האוכלוסייה, הדמיית סידן תאי יחיד מיקרואנדוסקופיים חשפו כי מצבים פנימיים מגייסים נוירונים BNST נוספים מבלי לשנות באופן משמעותי את אמפליטודות התגובה האישית, ובכך הרחיבו את ההרכב המייצג מתוק במהלך הרעב. מפענח Softmax שהוכשר על פעילות BNST הפריד בין זהות גירוי (מתוק לעומת מלח) ומצב פנימי (פד, רעב, מתרוקן נתרן), השג ~ 80% דיוק בסך הכל ומראה שהרכבים BNST מקודדים במשותף "מה" ו"צורך ".
באופן סיבתי, ה- BNST התנהג כבקר צריכה כללי: הפעלה אופטוגנטית של נוירונים VGAT של BNST הניע את צריכת הרחבה, כולל מזון מוצק, מים מתוקים, נתרן גבוה, בדרך כלל חומרים מרים סלידה, ואפילו כדורי מזון פיקטיביים, ואילו התנהגות מדכאת של השתקה אינן פוספקות של גירוי או מצב. בדיקות תרגום הדגישו את הרלוונטיות הקלינית. במודל ציספלטין הגורם לירידה במשקל דמוית Cachexia, הפעלה כימונית של נוירונים VGAT של BNST שמרתה על משקל הגוף. לעומת זאת, עיכוב כימוגנטי של BNST גרם לירידה במשקל בעכברים שמנים הנגרמים על ידי דיאטה, השפעה שהפכה כאשר הפסקת העכבה. אגוניסט פפטיד -1 דמוי גלוקגון (GLP-1R), Semaglutide, גרם ל- FOS באופן סלקטיבי בנוירונים BNST של חלבון קינאז C (PKCΔ), מה שמצביע על כך שנוירונים אלה הם אתר פוטנציאלי התורם לפעולה של תרופת האנטי-אויביות. יחד, נתונים אלה מגדירים את ה- BNST כ"חיוג צריכה "אחיד המשלב באופן גמיש ערך תיאבוני וצורך פנימי להניע תגובות השלמות.
מסקנות
לסיכום, עבודה זו מציבה את ה- BNST כמרכז בקרה שהופך את האדיבות לאכילה על ידי מיזוג ערכיות חושית מ- CEA פדין נוירונים עם אותות זקוקים מנוירוני AGRP. מבחינה קלינית, מנוף דו כיווני על צריכה מצביע על דרכים להתמודד עם בזבוז הקשור לסרטן או, בניגוד, לקידום ירידה במשקל על ידי עיכוב. הקשר של אגוניזם GLP1R עם נוירונים BNST חיוביים PKCΔ מדגיש נקודת דרך מכניסטית לתרופות נגד השמינות.