על ידי אישור ליקוי קוגניטיבי לפני הזמנת בדיקות דם עמילואידיות, גישה דו-שלבית זו חותכת חיוביות כוזבות, מייעלות הפניות ומניעה את האבחנה של אלצהיימר קרוב יותר למרפאות היומיומיות.
מחקר: איתור טיפול ראשוני של מחלת אלצהיימר באמצעות בדיקה קוגניטיבית דיגיטלית המנוהלת על ידי עצמה וסמנים ביולוגיים בדם. קרדיט תמונה: Orawan Pattarawimonchai / Shutterstock
במחקר שפורסם לאחרונה בכתב העת רפואת טבעחוקרים בשוודיה ובארצות הברית העריכו אם סוללה קוגניטיבית דיגיטלית קצרה המנוהלת על עצמה, לבד או בשילוב עם פאנל ביו-סמן עמילואיד מבוסס דם, מגלה בצורה מדויקת יותר ליקוי קוגניטיבי ומחלת אלצהיימר קלינית (AD) בטיפול ראשוני מאשר טיפול סטנדרטי.
רֶקַע
אחד מכל שלושה מבוגרים מבוגרים דואג מאובדן זיכרון, ובכל זאת רבים אף פעם לא מקבלים אבחנה מדויקת בזמן. AD היא הגורם המוביל לדמנציה, המונעת על ידי תצהיר עמילואיד-בטא (Aβ), צבירת טאו והתנוונות עצבית. שלבים מוקדמים כמו ירידה קוגניטיבית סובייקטיבית (SCD) וליקוי קוגניטיבי קל (MCI) מחליקים לעתים קרובות בדיקות נייר קצרות כמו בדיקת מצב מיני-מנטאלי (MMSE) או הערכה קוגניטיבית במונטריאול (MOCA), במיוחד במרפאות ממהרות. נוזל מוחי -שדרה (CSF) או טומוגרפיה של פליטת פוזיטרון עמילואיד (PET) יכולים לאשר פתולוגיה, אך שיטות אלה הן פולשניות, יקרות או נדירות. בדיקות דם כמו TAU 217 זרחן (P-TAU217) מבטיחות, ובכל זאת ההסתברויות המוקדמות משתנות באופן נרחב בטיפול ראשוני, כאשר חיוביות עמילואיד בדרך כלל נמוכה יותר ב- SCD וגבוה יותר ב- MCI או דמנציה, ומשפיעים על ערך חיזוי חיובי (PPV). הנחיות בינלאומיות מדגישות יותר ויותר זרימות עבודה דו-שלביות המאשרות ליקוי לפני בדיקת סמן ביולוגי. מחקר נוסף אמור לאמת מסלולי חזית יעילים, מדויקים וניתנים להרחבה.
על המחקר
החוקרים הכשירו ביוקוג ואושרו, סוללת בדיקה מבוססת טאבלט, המנוהלת על עצמה, על פני שתי קבוצות שוודיות. קבוצה משנית לטיפול משני ממחקר הביופינדר -2 (ClinicalTrials.gov NCT03174938) שימשה לבניית מודלים לוגיסטיים-רגרסיה ולבסס קיצוצים; קבוצה עצמאית לטיפול ראשוני מ -19 מרפאות במחקר הטיפול הביופינדר-ראשוני (NCT06120361) שימשה לצורך אימות חיצוני. BioCog כללה רשימת עשר מילים (שלוש זיכרונות מיידיים, זיכרון מעוכב והכרה מעוכבת), משימה מהירה של עיבוד קוגניטיבי ופריטים הקשורים להתמצאות לזמן. ליקוי קוגניטיבי אובייקטיבי הוגדר באמצעות הסוללה החוזרת על עצמה להערכת המצב הנוירופסיכולוגי (RBANS); בטיפול משני נעשה שימוש בפרוקסי עבור ה- RBAN מבדיקות נוירופסיכולוגיות דומות.
בחירת המודל השתמשה בחיסול תכונות רקורסיביות עם קריטריון המידע של Akaike (AIC) ואזור מקלט-מקלט-מאפיין מתחת לעיקול (AUC) לביצועים. תוכניות קציצה אחת ושתי חתכים הוגדרו מראש; האחרון יצר אזור ביניים שייפתר על ידי הערכה נוספת. שני ספי הסתברות ביולוגיים (0.332 ו- 0.769) נבחרו כדי למקד לרגישות של 95% ולספציפיות של 95%. רופאים לטיפול ראשוני (PCPS) ביצעו הערכות סטנדרטיות, כולל MMSE, MOCA, טומוגרפיה ממוחשבת ושיקול דעת קליני. נבדקה זרימת עבודה דו-שלבית: שלב 1 כלל ביוקוג כדי לאתר ליקוי; שלב 2 כלל לוח פלזמה (precivityAd2) בהפקת ציון ההסתברות העמילואיד -2 (APS2) מ- Aβ42, Aβ40, P-TAU217 ולא-P-TAU217. ניתוחי רגישות השתמשו בציון הגלובלי של דירוג דמנציה קליני (CDR) ≥0.5 כהפניה לירידת ערך חלופית.
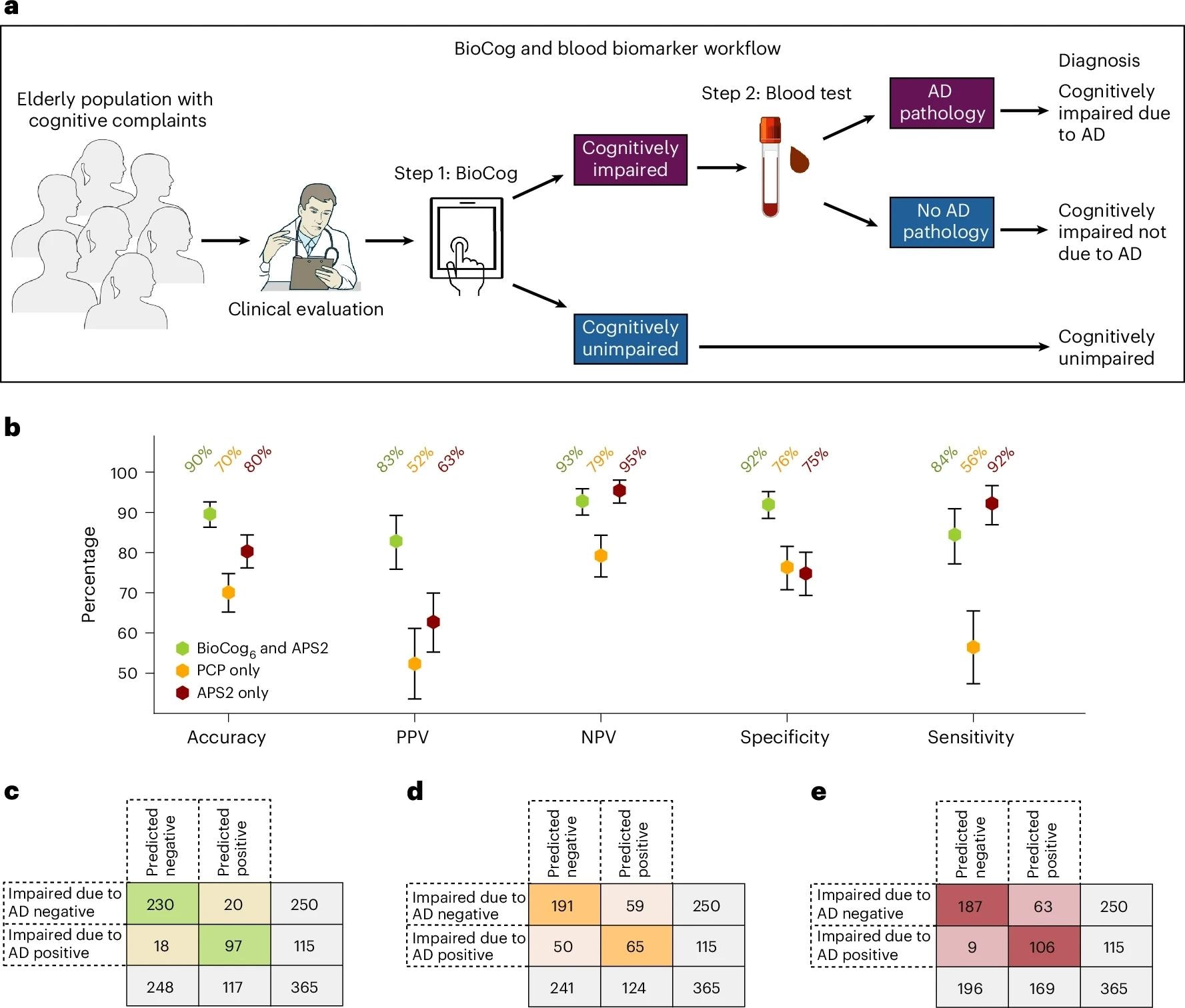
השוואה בין בדיקות דיגיטליות לבין זרימת עבודה אבחנתית מבוססת סמן ביולוגי בדם לבין ההערכה הקלינית הסטנדרטית הנוכחית בקבוצה הטיפולית הראשונית. השוואות בוצעו בקבוצת משנה של אנשים עם כל הנתונים הקיימים הקיימים (n = 365; ראה טבלה משלימה 17 למאפייני אוכלוסייה מפורטים). א. זרימת העבודה הדו-שלבית המוצעת שלנו לטיפול ראשוני מורכבת משלב 1, THE איתור ליקוי קוגניטיבי באמצעות הביוקוג, ואחריו שלב 2, הערכת סמן ביולוגי בדם כדי להעריך האם פתולוגיה של AD קיימת אצל אנשים לקויים קוגניטיביים. בהערכת זרימת העבודה באמצעות הביוקוג שלנו6 מודל לשלב 1 ולסמן הביולוגי של הפלזמה APS2 לשלב 2 (ירוק). זרימת העבודה הושוותה לעומת הערכה קלינית סטנדרטית על ידי PCPמוֹדָעָהכתום), וכנגד זרימת עבודה המשתמשת רק בסמן הביולוגי של הפלזמה APS2 ללא הערכה קוגניטיבית (אדום). סרגלי שגיאות מצביעים על 95% CI, כאשר נקודת המרכז תואמת את הערך הממוצע. קרדיט: תמונות ב א הותאם מ- niaid nih bioart (https://bioart.niaid.nih.gov).
תוצאות המחקר
בטיפול משני (n = 223; גיל ממוצע 73 שנים), המודל הטוב ביותר של שישה משתנים (BioCog6: זיכרון מעוכב, מהירות עיבוד נכונה, ביצועים זיכרון מיידיים, זמן כולל, גיל והכרה מאוחרת) השיגו AUC של 0.96 ו 89% דיוק עבור פגיעה קוגניטיבית מאומתת באופן אובייקטיבי בניתוק יחיד. גישה דו-קוטית הגיעה לדיוק של 96% כאשר 18% מהמשתתפים באזור ביניים הדורש מעקב. פסיכומטריה תמכה בכדאיות ותוקף: מתאם מתכנס חזק עם אנלוגים נייר, מתאם חלש שונה עם תחומים לא קשורים, זמן השלמה ממוצע של כ -11 דקות, ורק כ -2% דיווח על קושי בהוראות.
אימות חיצוני בטיפול ראשוני (n = 403; גיל ממוצע 77 שנים) הראה דיוק BioCog6 AUC 0.93 ו- 85%(ערך חיזוי חיובי (PPV) 87%, ערך חיזוי שלילי (NPV) 83%, רגישות 88%, ספציפיות 82%) באמצעות ניתוק אחד, תוך צורה משמעותית של הערכת PCP (דימוי של 73%) על פי דימוי של שימושים). עם שני חתכים שהועברו מאימונים, הדיוק עלה ל 90% (PPV 91%, NPV 89%) עם קבוצת ביניים של 18%. השוואות ראש בראש העדיפו את BIOCOG6 על פני MMSE, MOCA, מיני COG, והסוללה האוטומטית של CAMBRIDGE Neuropsychological Learning (CANTAB) לומדת מזווגת, הן בניתוחי קוצץ אחד והן במקומות זמינים, ניתוחים של שני חתכים, גם לאחר התאמות דמוגרפיות.
באופן ביקורתי, זרימת העבודה הדו-שלבית המותאמת לטיפול ראשוני, BIOCOG תחילה, ואחר כך בדיקת דם רק עבור אלו שהופקו באופן אובייקטיבי, זיהו AD קליני מאומת ביולוגי (ליקוי כתוצאה מספינה של AD על ידי קונצנזוס מומחה עם תמיכה ב- CSF או Aβ-PET) עם 90%דיוק (PPV 83%, NPV 93%, 92%). זה עבר מסלולי PCP בלבד (דיוק 70%) וביצעו את בדיקות הדם בלבד (דיוק 80%), שהראו שיעור חיובי כוזב של 17%כשמשתמשים בהם ללא פילטר ליקוי. בעזרת שני ניתוק הן עבור BioCog והן של APS2 העלו דיוק ל 95% עם אזור ביניים גדול יותר (כ- 30%), והדגיש סחר בין הוודאות לבין הפניות בלתי מוגדרות. הממצאים היו מדויקים בעת החלפת CDR ≥0.5 עבור RBANS (מדדים ראשוניים טבלו בצניעות אך נותרו גבוהים) וכאשר הסירו את הגיל ממודל הביוקוג.
הפרשנות מתרכזת בהסתברות מוקדמת: מכיוון שרק אנשים עם לקות קוגניטיבית (לא SCD) זכאים לפילטר מיושם לאחרונה למוקד Aβ, פילטר יעיל חזיתית המאשר ליקוי לפני שביו-סמנים בדם מפחית חיובי שווא, משפר את PPV ומתיישר עם ההמלצות הבינלאומיות ואת פרופיל הארגון העדיף של ארגון הדם. משלוח דיגיטלי מתקנן במינהל, לוכד תכונות תזמון מעבר לציוני RAW וממזער את זמן כוח האדם, היתרונות למרפאות עסוקות העומדות בפני הביקוש ההולך וגובר. עם זאת, המחברים מזהירים כי BioCog צריך להשלים, לא להחליף, את השיפוט הקליני וכי עדיין נדרש אימות בשפות, תרבויות אחרות ומסגרות אורכיות.
מסקנות
הוכחת מושג זה מדגימה כי סוללה קוגניטיבית דיגיבטית קצרה ומנוהלת על עצמה יכולה לזהות במדויק ליקוי קוגניטיבי אובייקטיבי בטיפול ראשוני. כאשר אחריו לוח ממוקד של מסקרת דם ממוקד, הוא יכול לאבחן AD קליני ברמת דיוק גבוהה משמעותית מאשר התקן הנוכחי של הטיפול. גישת "מבחן-עד-דם" של הצעד משפרת את הוודאות האבחנתית, מפחיתה הפניות בלתי הולמות ומתעדפת מועמדים לטיפולים ממוקדים AP. בעוד שהכללות מעבר למסגרות שוודיות ותועלת אורך זקוקה למחקר נוסף, המסלול הוא מעשי, ניתן להרחבה ותואם את ההנחיות הבינלאומיות: לאשר תחילה פגיעה, ואז השתמש בסמנים ביולוגיים בדם כדי להסיק פתולוגיה של עמילואידים, ומביאים אבחנות קודמות יותר ובטוחות יותר בהישג יד של מרפאות שגרתיות.