לאחרונה רפואת טבע המחקר משלב מדידות של חלבוני פלזמה ומידע קליני כדי לבנות מודלים של חיזוי דל לשכיחות של 10 שנים של מספר מחלות נדירות ושכיחות.
לימוד: חתימות פרוטאומיות משפרות את חיזוי הסיכון למחלות נפוצות ונדירות. קרדיט תמונה: ArtemisDiana / Shutterstock.com
אבחון מחלה וחתימות פרוטאומיות
פיתוח כלים שימושיים מבחינה קלינית לזיהוי אנשים בסיכון מוגבר למחלה נותר אתגר משמעותי ברפואה מדויקת. היעדר כלים אלה מעכב לעיתים קרובות את האבחונים, ובכך תורם לתוצאות שליליות של המטופל.
ניתן להשתמש בחלבוני פלזמה בודדים לאבחון מחלות מסוימות, כגון טרופונינים לתסמונות כלילית חריפות. חתימות פרוטאומיות בפלזמה יכולות גם לשקף את מצב הבריאות הנוכחי, התנהגויות בריאותיות ואפילו גורמים גנטיים וסביבתיים של מחלה.
עדיין לא ברור אם ניתן להשתמש בפרוטאומי פלזמה כדי לחזות מחלות מסוימות לבד או בשילוב עם סמנים אחרים. מחקרים קודמים שבדקו את תפקידה של פרוטאומית פלזמה באבחון נקשרו למגבלות מסוימות, כולל גדלי מדגם קטנים והכללה של כמה מחלות נפוצות, במקום נקיטת גישת גילוי אגנוסטי. יש גם חוסר בראיות על דיוק מדדי הסקר בהשוואה למודלים קליניים ללא חלבונים.
לגבי המחקר
מדגם המחקר כלל 41,931 אנשים מפרויקט Biobank Pharma Proteomics של בריטניה. המדידות של כ-3,000 חלבוני פלזמה שולבו עם מידע קליני כדי לבנות מודלים של חיזוי דל ל-218 מחלות נדירות ושכיחות. מחלות אלו היו קשורות לשיעורי תחלואה ו/או תמותה גבוהים.
כדי לבנות את המודל, בודדו 80 מקרי תקריות בתוך 10 שנים מהמעקב מה-Biobank האקראי של בריטניה. נעשה שימוש גם במקרים של תקריות הכלולים בתת-הקבוצה 'נבחר קונסורציום'.
השילוב של נתונים מטיפול ראשוני, רישום סרטן ומוות, נתונים סטטיסטיים של פרקים בבתי חולים ומחלות שדווחו על עצמם הובילו לפנוטיפים מאומתים שעליהם התבססו הגדרות המחלה. מקרי אירוע שנרשמו במהלך ששת החודשים הראשונים של המעקב לא נכללו במחקר. גם מקרים שכיחים או כאלה שתועדו לפני ביקור ההערכה הבסיסי לא נכללו.
פרופיל פרוטאומי תפס 2,923 חלבונים ייחודיים שמטרתם 2,941 מבחני. הותאמה מסגרת תלת-שלבית למידת מכונה (ML), שכללה בחירת תכונות, כוונון, אופטימיזציה של היפרפרמטרים ואימות.
מחצית מהמדגם שימשה לבחירת תכונה, בעוד שהחצי השני חולק באופן שווה לצורך אופטימיזציה ואימות של מודל. לאחר מכן הושוו המודלים מבוססי הנתונים הפרוטאומיים לאלה המבוססים על מידע קליני בלבד או שילוב של מידע קליני ונתונים מ-37 מבחנים קליניים.
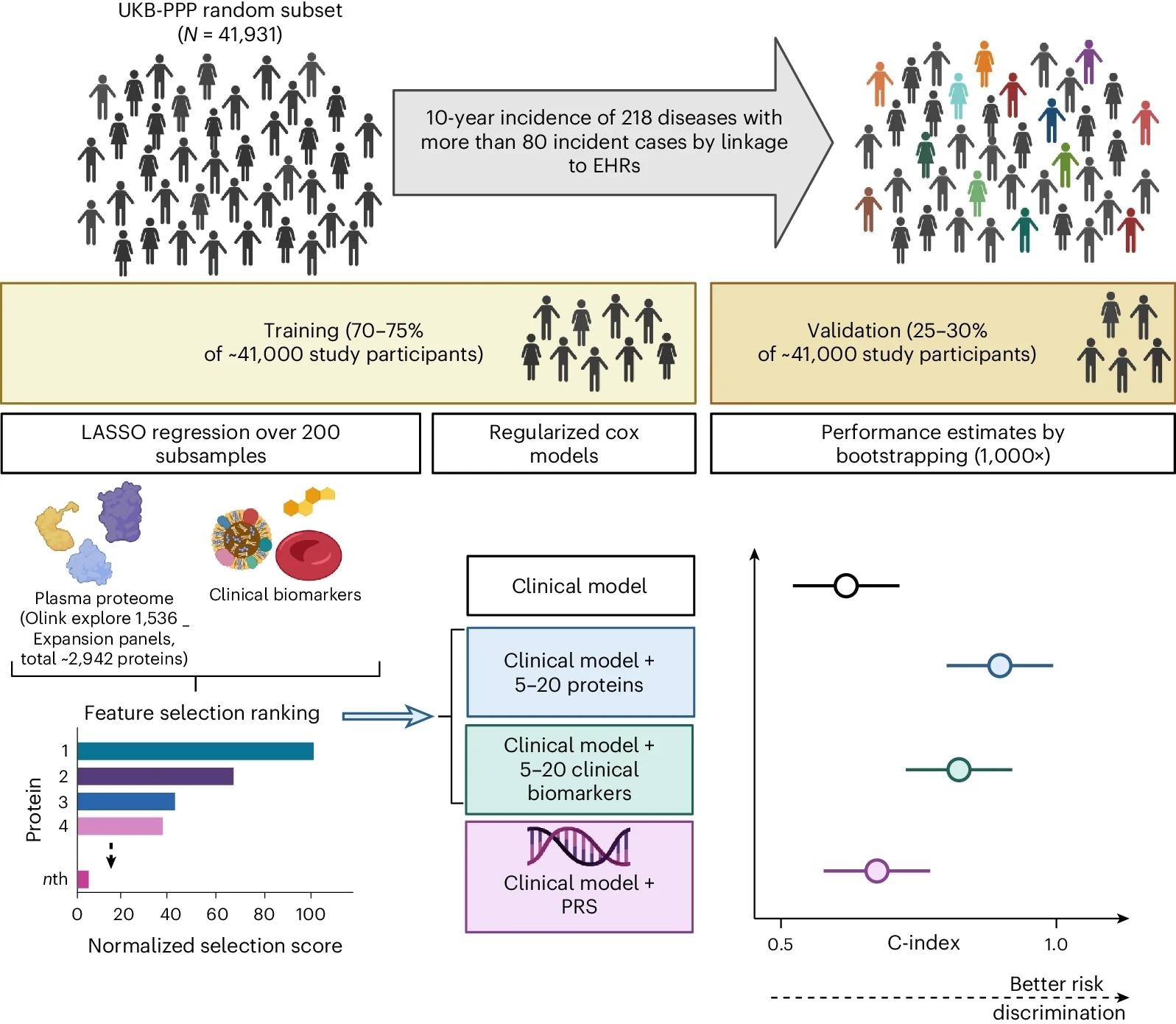 מחקר עוקבה זה מבוסס על תת-קבוצה אקראית של יחידי UKB-PPP (N = 41,931). הקבוצה חולקה לאימון (כולל שלבי בחירת תכונה ואופטימיזציה) וערכות אימות לפיתוח מנבאים מבוססי חלבון דל (כולל 5-20 חלבונים מהלוחות Olink Explore 1536 ו-Explore Expansion) עבור 218 מחלות שהוגדרו באמצעות נתונים מבריאות UKB -שאלון, טיפול ראשוני, סטטיסטיקות של פרקי בית חולים ורישום סרטן ומוות. הביצועים של מודלים המשתמשים בחתימות חלבון הושוו עם מודלים המשתמשים במידע קליני בסיסי בלבד או באמצעות מידע קליני בסיסי בשילוב עם נתוני בדיקה קלינית או PGS כלל-גנום. נוצר עם BioRender.com.
מחקר עוקבה זה מבוסס על תת-קבוצה אקראית של יחידי UKB-PPP (N = 41,931). הקבוצה חולקה לאימון (כולל שלבי בחירת תכונה ואופטימיזציה) וערכות אימות לפיתוח מנבאים מבוססי חלבון דל (כולל 5-20 חלבונים מהלוחות Olink Explore 1536 ו-Explore Expansion) עבור 218 מחלות שהוגדרו באמצעות נתונים מבריאות UKB -שאלון, טיפול ראשוני, סטטיסטיקות של פרקי בית חולים ורישום סרטן ומוות. הביצועים של מודלים המשתמשים בחתימות חלבון הושוו עם מודלים המשתמשים במידע קליני בסיסי בלבד או באמצעות מידע קליני בסיסי בשילוב עם נתוני בדיקה קלינית או PGS כלל-גנום. נוצר עם BioRender.com.
ממצאי המחקר
מודלים קליניים השיגו את הביצועים הגבוהים ביותר עבור מחלות אנדוקריניות וקרדיווסקולריות. עבור תת-קבוצה של 163 מחלות, חמישה חלבונים בלבד פעלו כמו גם המודל הקליני וטובים משמעותית עבור 30 מחלות נוספות.
שילוב של חמישה עד 20 חלבונים שיפר משמעותית את הביצועים של מודלים קליניים עבור 67 מחלות נדירות ושכיחות, כולל מחלת צליאק, מחלת נוירונים מוטוריים ופיברוזיס ריאתי. עבור 28 מחלות, מודלים המשלבים נתוני בדיקת דם עמדו בביצועים גבוהים יותר מהמודלים הקליניים.
עבור 52 מתוך 67 המחלות הללו, מודלים עם חתימות חלבון דל עלו על מודלים קליניים עם מבחני דם. כולל חלבונים הגדילו את המודלים במיוחד עבור מחלות פחות שכיחות.
כוח הניבוי החזק של חלבונים הודגם עבור חולי מיאלומה נפוצה (MM) שאובחנו לאחרונה. ריצוף של חומצה ריבונוקלאית חד-תאית (RNA) ממח עצם הדגיש שארבעה מתוך חמשת החלבונים המנבאים, כולל B-דמוי קולטן Fc (FCRLB), גלוטמיניל-פפטיד ציקלוטרנספראז (QPCT), בן משפחה SLAM 7 (SLAMF7), ונמק גידולים חבר משפחה של קולטן גורם 17 (TNFRSF17) באו לידי ביטוי ספציפי בתאי פלזמה.
עבור שש מחלות, ניתן היה לקבוע את התוקף החיצוני של דגמי החלבון במחקר EPIC-Norfolk. עבור ארבעה מתוך חמשת החלבונים, שהצליחו לחזות יותר מעשר מחלות, גיל היה המתאם העיקרי.
באופן השוואתי, מצב העישון היה המתאם העיקרי לליגנד 17 של כימוקין (מוטיב CXC) (CXCL17). עם זאת, שילוב נתוני חלבון שיפר את יכולת הניבוי האבחנתי בהשוואה לגורמי סיכון קונבנציונליים.
זוהו גם חלבונים שהיו מנבאים אך ורק מחלה אחת בלבד, שכללו TNFRSF13B עבור גמופתיה חד-שבטית של מובהקות בלתי מוגדרת (MGUS) ו-TNFRSF17 או אנטיגן התבגרות תאי B עבור MM. בניתוחי רגישות, שילוב חלבונים נוספים לא בהכרח שיפר את ביצועי המודל; עם זאת, כולל סמנים ביולוגיים ספציפיים שיפרו חיזוי למחלות נבחרות.
מסקנות
חתימות חלבון פלזמה דלילות יכולות לשפר חיזוי בהשוואה למבחנים קליניים סטנדרטיים למחלות נפוצות ונדירות. עם זאת, יש צורך במחקרים עתידיים כדי לאמת ממצאים אלה באוכלוסיות מגוונות מבחינה אתנית ובאזורים גיאוגרפיים שונים. עבור מחלות נדירות יותר, נדרשים דגימות גדולות יותר כדי להעריך את שיעורי הגילוי במדויק.
פלטפורמות פרוטאומיות נוכחיות מספקות מבחני חלבון כימות יחסיים; עם זאת, תרגום קליני יצטרך פיתוח נוסף ואימות של מבחני חלבון כימות מוחלטים.
נראה כי חלבוני פלזמה טובים יותר לניבוי מחלות השייכות להתמחויות קליניות מסוימות. לכן, החיזוי של מחלות אחרות יצטרך להתבסס על מידע קליני שונה.



