במחקר שפורסם לאחרונה בכתב העת רפואת טבעחוקרים ערכו מחקר אקראי, כפול סמיות, מבוקר פלצבו שלב 2a כדי לחקור את הבטיחות והיעילות של LM11A-31 בניהול מחלת אלצהיימר (AD) באמצעות קולטן נוירוטרופין p75 (p75NTR) וויסות.
אלצהיימר מאוחרת היא הצורה השכיחה ביותר של דמנציה, המאופיינת בכשל סינפטי, ניוון ואובדן. למרות ששתי תרופות ראשוניות לספירה מכוונות להצטברות של חלבון עמילואיד-β או טאו חריג, הן מתייחסות רק לקבוצת משנה של הפתופיזיולוגיה. אפשרות נוספת היא להתמקד בביולוגיה עמוקה, הכוללת קולטנים ורשתות איתות המשפיעות על מסלולים ביולוגיים בסיסיים. מחקרים פרה-קליניים מראים כי אפנון p75NTR עם הכימיקל הקטן הראשון בכיתה LM11A-31 מפחית אובדן סינפסה המושרה על ידי עמילואיד ופתולוגי.
מחקר: אפנון קולטן נוירוטרופין p75 במחלת אלצהיימר קלה עד בינונית: ניסוי אקראי, מבוקר פלצבו שלב 2a. קרדיט תמונה: Burdun Iliya / Shutterstock
לגבי המחקר
בניסוי הקליני האקראי הנוכחי, חוקרים חקרו האם LM11A-31 יכול לעכב את התקדמות מחלת האלצהיימר על ידי אפנון p75NTR בבני אדם.
החוקרים העניקו כמוסות פומיות של LM11A-31 במינונים של 200 מ"ג ו-400 מ"ג לעומת פלצבו ביחס של 1:1:1 ל-242 חולי מחלת אלצהיימר קל עד בינוני במשך 26 שבועות. למשתתפים אושרה ביולוגית מחלת אלצהיימר (נוזל מוחי (CSF) חלבון עמילואיד β 42 (Aβ42) מתחת ל-550 ng/l או יחס Aβ42:Aβ40 מתחת ל-0.89) שאובחנה באמצעות קריטריונים של McKhann, Mini-Mental State Examination (MMSE) וציונים בין 2618 , ציונים של סולם דיכאון גריאטרי (GDS) מתחת ל-5.0, ציוני סולם איסכמי שונה של Hachinski (HIS) ≤ 4.0, השכלה פורמלית במשך ≥8.0 שנים, וירידה קוגניטיבית קודמת במשך ≥6.0 חודשים.
אנשים מתאימים צרכו מעכבי אצטילכולין אסטראז (AChEIs) או אנטגוניסטים חלקיים לקולטן N-methyl-D-aspartate (NMDA) במשך 3.0 חודשים מעל ל-3.0 חודשים לפני תחילת המחקר. הם לא צרכו באופן קבוע תרופות אסורות כמו נוירולפטיקה, בנזודיאזפינים, תרופות אנטי-אפילפטיות, תרופות הרגעה, תרופות נגד יתר לחץ דם פעילות מרכזית, תרופות נוטרופיות (למעט גינקו בילובה) או משככי כאבים המכילים אופיואידים.
התוצאה העיקרית הייתה בטיחות וסבילות, שהוערכו באמצעות סולם חומרת התאבדות של קולומביה (C-SSRS), סימנים חיוניים, לחץ דם ופרמטרים המטולוגיים. המחקר השתמש בהדמיית תהודה מגנטית מבנית (sMRI), טומוגרפיה פליטת פלורודאוקסיגלוקוז-פוזיטרון (FDG-PET) וסמנים ביולוגיים של CSF כדי להעריך תוצאות קוגניטיביות משניות במחלת אלצהיימר. מדדי AD כוללים טאו פוספוריל ב-Thr181, חלבון טאו כולל, פעילות Aβ40, Aβ42 ו-AChE. הצוות השתמש בסוללת בדיקה נוירופסיכולוגית מותאמת אישית כדי להעריך תוצאות קוגניטיביות משניות בקו הבסיס, בשבוע 12 ושבוע 26.
תוצאות משניות ומחקריות כללו חלבונים סינפטיים (Synaptosomal-associated protein-25 (SNAP25), Synaptotagmin-1 (SYT1) ונוקלאופרוטאין (NG)), חלבונים מיקרוגליים (קולטן טריגר מסיס מבוטא על תאים מיאלואידים 2 (sTREM2)), סמנים ביולוגיים אסטרוציטיים (YKL40), וסמנים ביולוגיים ניווניים (שרשרת קלה של נוירופילמנט (NfL)). החוקרים ביצעו גם בדיקות הדמיה חקרניות, הערכות קליניות ובדיקת רושם גלובלי קליני (CGI).
הצוות השיג דגימות CSF בהקרנה ובביקורים אחרונים כדי להעריך את רמות sTREM2 על ידי בדיקות אימונו. הם קבעו את רמות SNAP25 ו-SYT1 באמצעות ספקטרומטריית משקעים-מסה אימונו (IP-MS), ואילו NG נמדד באמצעות מבחן אימונוסורבנטי מקושר אנזים (ELISA). תוצאות קוגניטיביות כללו את ציוני AD Assessment Scale-Cognitive Subscale (ADAS-Cog-13) וציוני MMSE. החוקרים חקרו את ההשפעות של טיפול ב-LM11A-31 על שלמות החומר האפור ומטבוליזם של גלוקוז באזורי מוח פגיעים ל-AD, תוך ניתוח משתתפי AD Neuroimaging Initiative (ADNI) שנבחרו על סמך גיל, ציון MMSE וחריגות ב-CSF Aβ42.
תוצאות
המחקר מצא כי LM11A-31 בטוח ומקובל, ללא חששות בטיחותיים רציניים. תופעות הלוואי המתפשטות כוללות כאבי ראש, שלשולים, אאוזינופיליה ודלקת אף, כאשר בעיות במערכת העיכול ואאוזינופיליה הן הסיבות הנפוצות ביותר להפסקה. קבוצת ה-400 מ"ג ראתה הפסקות תרופות גדולות יותר מאשר קבוצות ה-200 מ"ג ופלסבו. MRI לא מצא חששות בנוגע לבטיחות התרופות, כולל הפרעות הדמיה הקשורות לעמילואיד. הצוות לא ציין הבדלים משמעותיים בהערכות קוגניציה או הפרעות הדמיה הקשורות לעמילואיד בין שתי קבוצות הטיפול. שינויים ב-CSF האורך, מחקרים בהדמיה של אזורי עניין ומבחנים קוגניטיביים לא הראו הבדל בין שתי קבוצות המינון.
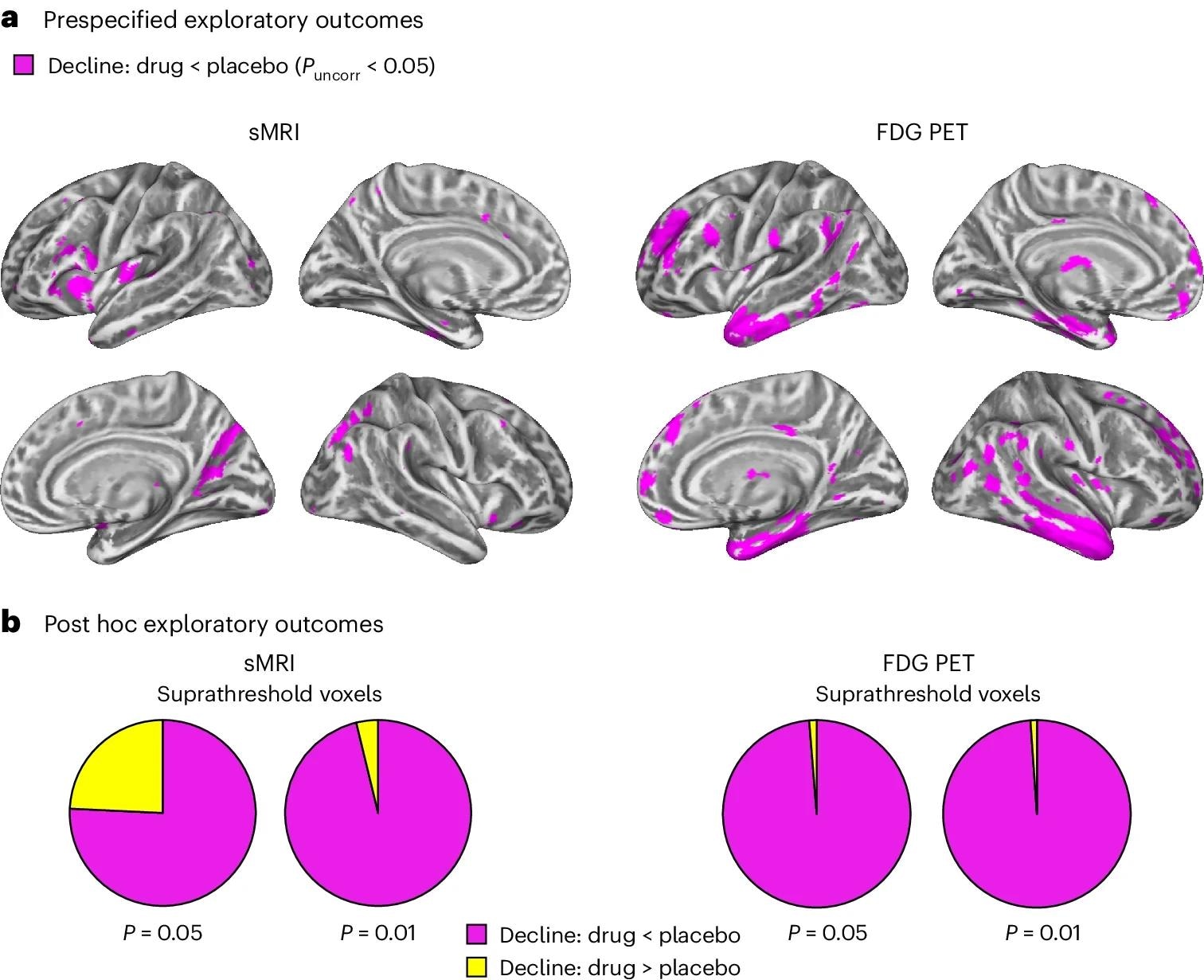 א, ניתוחי השפעות מעורבות של גורמים של מודלים שיתופיות בדקו את האינטראקציות הדו-כיווניות בין טיפול (תרופה או פלצבו) לזמן (לפני או אחרי הטיפול). ניגודיות t חד-צדדית שבדקה את האינטראקציה עקבית ההשערה (התרופה מאטה את ההתקדמות לאורך זמן ביחס לפלסבו) גילתה שטיפול ב-LM11A-31 האט את ניוון האורך (לוחות שמאל) ואת תת-מטבוליזם של גלוקוז (פאנלים ימין) בקבוצת התרופות (sMRI) , n = 127; PET, n = 121) בהשוואה לקבוצת הפלצבו (sMRI, n = 66; PET, n = 62). ווקסלים המציגים אפקט אינטראקציה זה מוצגים בסף P < 0.05 לא מתוקן (מגנטה) על משטח קליפת המוח הספציפי לאוכלוסייה. ההמיספרות השמאלית והימנית נמצאים בשורות העליונות והתחתונות, בהתאמה. אזורי מוח המציגים השפעות אינטראקציה לא עקביות בהשערות מוצגים באיור נתונים מורחבים. 7. ב, המספר הכולל של ווקסלים באזורי המוח של פגיעות AD a priori (השטח הכולל של תרשימי עוגה) המציגים אינטראקציה עקבית השערה (מגנטה) או אינטראקציה לא עקבית השערה (צהוב) בכל שיטת הדמיה (sMRI, פאנל שמאלי; FDG PET, לוח ימין) בספים ליברלים יותר ויותר של P < 0.01 ו- P < 0.05 לא מתוקנים. סימולציות של מונטה קרלו קבעו כי היחסים של ווקסלים המציגים השפעות עקביות השערה לעומת היפותזה לא עקבית היו גבוהים משמעותית מאלה שנצפו על בסיס נתונים מדומים אקראי עבור sMRI ו-PET (P < 0.001 לכל אחד; דו צדדי).
א, ניתוחי השפעות מעורבות של גורמים של מודלים שיתופיות בדקו את האינטראקציות הדו-כיווניות בין טיפול (תרופה או פלצבו) לזמן (לפני או אחרי הטיפול). ניגודיות t חד-צדדית שבדקה את האינטראקציה עקבית ההשערה (התרופה מאטה את ההתקדמות לאורך זמן ביחס לפלסבו) גילתה שטיפול ב-LM11A-31 האט את ניוון האורך (לוחות שמאל) ואת תת-מטבוליזם של גלוקוז (פאנלים ימין) בקבוצת התרופות (sMRI) , n = 127; PET, n = 121) בהשוואה לקבוצת הפלצבו (sMRI, n = 66; PET, n = 62). ווקסלים המציגים אפקט אינטראקציה זה מוצגים בסף P < 0.05 לא מתוקן (מגנטה) על משטח קליפת המוח הספציפי לאוכלוסייה. ההמיספרות השמאלית והימנית נמצאים בשורות העליונות והתחתונות, בהתאמה. אזורי מוח המציגים השפעות אינטראקציה לא עקביות בהשערות מוצגים באיור נתונים מורחבים. 7. ב, המספר הכולל של ווקסלים באזורי המוח של פגיעות AD a priori (השטח הכולל של תרשימי עוגה) המציגים אינטראקציה עקבית השערה (מגנטה) או אינטראקציה לא עקבית השערה (צהוב) בכל שיטת הדמיה (sMRI, פאנל שמאלי; FDG PET, לוח ימין) בספים ליברלים יותר ויותר של P < 0.01 ו- P < 0.05 לא מתוקנים. סימולציות של מונטה קרלו קבעו כי היחסים של ווקסלים המציגים השפעות עקביות השערה לעומת היפותזה לא עקבית היו גבוהים משמעותית מאלה שנצפו על בסיס נתונים מדומים אקראי עבור sMRI ו-PET (P < 0.001 לכל אחד; דו צדדי).
LM11A-31 הפחית ביעילות עליות הקשורות ל-AD ב-Aβ42 ו-CSF Aβ40 בהשוואה לקבוצת הפלצבו. זה גם הדגים ירידה באחוז השינוי השנתי החציוני בסמן הביולוגי SNAP25 הפרה-סינפטי וירידה בסמן הביולוגי של NG פוסט-סינפטי, מה שמצביע על כך ש-LM11A-31 מאט את מהלך האובדן הפרה-סינפטי ופוסט-סינפטי. LM11A-31 גם הפחית עליות אורכיות ב-YKL40, וכתוצאה מכך לירידה ב-MMSE ולעלייה ב-ADAS-Cog-13. זה גם הפחית את אובדן החומר האפור באפרקולום הקדמי ובקליפת הקודקוד האחורית ואת הירידה המטבולית של הגלוקוז באזורים כמו הקורטקס האנטורינאלי, הקורטקס הטמפורלי, ההיפוקמפוס, האינסולה והקורטקס הפרה-פרונטלי.
מסקנת המחקר היא כי מיקוד ל-p75NTR עם LM11A-31 מתאים למחקרים קליניים בקנה מידה גדול יותר. LM11A-31 עמד בנקודת הסיום הבטיחותית העיקרית ונסבל היטב על ידי חולי AD קל עד חמור. הממצאים מצביעים על מחקרים נוספים עם משך טיפול ארוך יותר כדי לחקור את הכדאיות של ויסות מולקולה קטנה של p75NTR כטיפול משנה מחלה בAD. המחקר מצא כי LM11A-31 השפיע באופן עמוק על מספר סמנים ביולוגיים, כולל CSF Aβ40, Aβ42, SNAP25, NG ו-YKL40, מה שמצביע על כך שהוא מאט את ההתפתחות הפתולוגית. מחקרים עתידיים בבני אדם יכולים להעריך אינדיקטורים נוספים של מצב גליה.



