בדיקת דם חדשה מבוססת מתילציה של DNA יכולה לזהות חולי סוכרת מסוג 2 בסיכון הגבוה ביותר להתקף לב או לשבץ מוחי מראש, להכות ציוני סיכון מסורתיים ופתיחת הדלת למניעה מוקדמת יותר וממוקדת יותר.
מחקר: סמנים ביולוגיים אפיגנטיים מנבאים אירועים מקרווסקולריים אצל אנשים עם סוכרת מסוג 2. קרדיט תמונה: Dragon Claws / Shutterstock
במחקר שפורסם לאחרונה בכתב העת דיווחי תאים רפואייםהחוקרים זיהו סמנים ביולוגיים אפיגנטיים שחוו אירועים מקרו -וסקולריים מקריים (IMEs) אצל אנשים עם סוכרת מסוג 2 (T2D).
לאנשים עם T2D יש סיכון גבוה פי שניים עד ארבעה מחלות לב וכלי דם (CVD) מאשר אנשים שאינם סוכרתיים. זיהוי אנשים הנמצאים בסיכון לאירועים מקרווסקולריים (MES) הוא קריטי למניעת מחלות. עם זאת, התחזית שלי אצל אנשים עם T2D היא תת -אופטימלית. בעוד שציוני ריבוד סיכונים עבור CVD זמינים, יש להם יכולת מתונה לרדת חולי T2D. ככאלה, יש צורך לזהות סמנים ביולוגיים חדשים כדי לשפר את חיזוי ה- CVD ו- ME בנבדקי T2D.
המחקר והממצאים
במחקר הנוכחי, החוקרים זיהו סמנים ביולוגיים אפיגנטיים מבוססי דם כדי לחזות IMEs אצל אנשים שאובחנו לאחרונה עם T2D. הם כללו 752 משתתפים עם T2D שאובחן לאחרונה עם נתוני מתילציה DNA (DNAM) זמינים וללא MES ידועים מכל חולי הסוכרת החדשים בסקאניה (ANDIS) ובמחוז אופסלה (ANDIU) קבוצות ב"קבוצה פרוספקטיבית עבור MES ב- T2D. " מתוכם, 102 אנשים פיתחו MES במהלך מעקב ממוצע של כארבע שנים ובמקסימום שבע שנים, ואילו 650 לא עשו זאת.
החוקרים ניתחו את DNAM של מעל 853,000 אתרים בדם כדי לזהות סמנים ביולוגיים אפיגנטיים הקשורים ל- MES עתידי. הם גילו ש- DNAM של 461 אתרים היה קשור ל- IMEs באמצעות מודל רגרסיה של COX המותאם למגדר, גיל, מדד מסת גוף (BMI), והמוגלובין גליקלי (HBA1C). אתרים אלה, שהוסברו על 422 גנים, הופצו על פני הגנום.
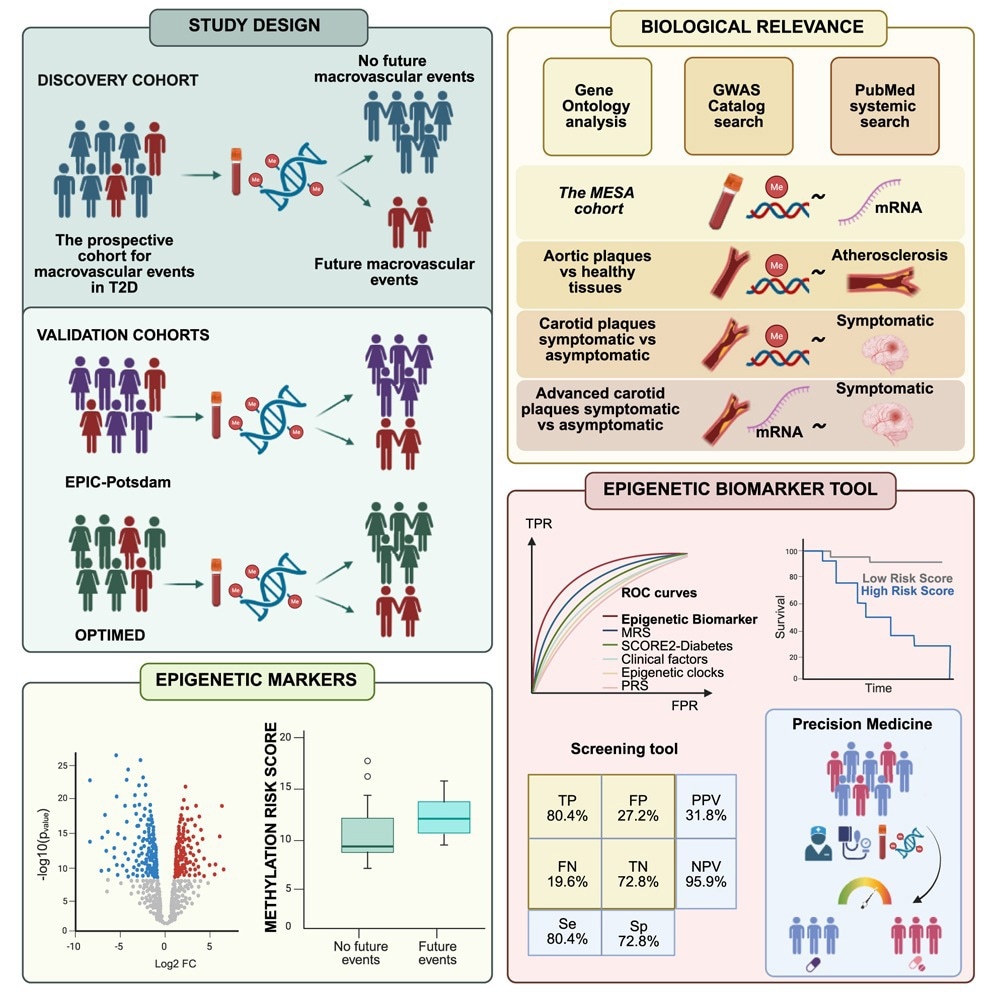
Garcı´a-Calzo´ n et al. זהה כלי סמן ביולוגי מבוסס דם המסייע בחיזוי מחלות לב וכלי דם עתידיות, אשר אנשים עם סוכרת מסוג 2 נוטים יותר להתפתח. הממצאים שלהם תומכים בשימוש בסמנים ביולוגיים אפיגנטיים כדי לשפר את ריבוד הסיכון ולהנחות אסטרטגיות מניעה מותאמות אישית יותר בטיפול בסוכרת.
יתר על כן, התוצאות נותרו עקביות, עם כ -453 אתרים הקשורים ל- IMEs, לאחר התאמה נוספת לתרופות, עישון, פרופילי שומנים והרכב תאים. בשלב הבא, הצוות בדק האם ציון סיכון למתילציה (MRS) היה מנבא MES עתידי אצל אנשים שאובחנו לאחרונה עם T2D. אתרי מתילציה עם הבדלי מתילציה מוחלטים ≥ 2% בין ביקורת לאנשים עם IMEs סוננו לצורך הכללה ב- MRS.
ה- MRS כלל 87 אתרי מתילציה; מרבית האתרים (74%) היו היפומטילטיים אצל אלו עם IMEs יחסית לבקרות. חוץ מזה, ה- MRS היה שונה באופן משמעותי בין בקרות לאנשים עם MES. בשלב הבא, הצוות ביצע אימות צולב פי חמישה באמצעות מודלים לוגיסטיים כדי להעריך אם ה- MRS יכול להבדיל בין בקרות לאנשים עם IMEs בקבוצה הפוטנציאלית עבור MES ב- T2D.
לשם השוואה, ניתוח אימות צולב בוצע רק עם גורמי סיכון קליניים של MES. יתר על כן, נבדק השילוב של גורמים קליניים ו- MRS. מקלט המפעיל עקומות אופייניות חשפו כי ה- MRS ניבא IMEs עם שטח מתחת לעיקול (AUC) של 0.81, ואילו גורמי סיכון קליניים בלבד ניבאו IMEs עם AUC של 0.69. השילוב של ה- MRS לגורמי סיכון קליניים הניב AUC של 0.84.
בדיקות סטטיסטיות הראו כי ה- MRS ביצעו באופן משמעותי יותר מגורמי סיכון קליניים בלבד (p = 0.001), והמודל המשולב ביצע באופן משמעותי את גורמי הסיכון הקליניים (P = 1.7 × 10⁻). ניתוח דיוק-זיקוק, המתאים לנתונים לא מאוזנים, הראה גם רגישות ודיוק משופרים עבור מודלים מבוססי MRS.
בשלב הבא, יכולתו של MRS לחזות MES הושווה עם ציוני סיכון CVD מבוססים, ציון סיכון פוליגני (PRS) על בסיס 204 פולימורפיזם של מחלות עורקים כליליות הקשורות לגרעין (SNPs), ושעוני תמותה אפיגנטיים. מחקר סוכרת פרוספקטיבית של בריטניה (UKPDS) וציוני הסיכון של ציון 2-דיאבטיות המנבאים CVD אצל אנשים סוכרתיים היו בעלי AUC של 0.54 ו- 0.62, בהתאמה, בחיזוי MES.
ה- PRS, השעונים האפיגנטיים ותמותה וציוני סיכון אחרים (מחקר רב-אתני של טרשת עורקים, CVD טרשת עורקים וציוני סיכון של פרמינגהם) היו גרועים משמעותית מאשר MRS או MRS פלוס גורמים קליניים, כאשר AUCs נעים בין 0.61 ל- 0.68. נקודת הניתוק האופטימלית של הכלי המשולב של Biomarker, שהראתה את התחזית הטובה ביותר, הוערכה כ- 0.023, עם רגישות וספציפיות של 0.804 ו- 0.728, בהתאמה. בניתוק זה, המודל השיג ערך חיזוי שלילי גבוה של 95.9% וערך חיזוי חיובי בינוני של 31.8%, כלומר הוא יכול לזהות באופן אמין אנשים שלא סבירים לחוות IMEs אך היה פחות מדויק לאישור הנמצאים בסיכון. ניתוחי שיפור סיווג מחדש נטו הראו שיפור מתמיד של 28.2% קטגורי ו -90.2% לעומת גורמי סיכון קליניים בלבד. על פי ההערכה, הבדיקה עולה כ -200 דולר למדגם, גורם שהמחברים מציעים יכול להיות בר ביצוע לסינון קליני אם משתמשים בו באופן סלקטיבי באוכלוסיות בסיכון גבוה.
יתרה מזאת, החוקרים העריכו האם 64 הגנים הודיעו ל 87 אתרי מתילציה ב- MRS מראים ביטוי דיפרנציאלי בלוח קרוטידי מחולים סימפטומטיים ואסימפטומטיים. הם מצאו ביטוי דיפרנציאלי של ארבעה גנים בלוח מחולים סימפטומטיים בהשוואה לחולים אסימפטומטיים. הם גם דיווחו כי 72% מהגנים של ה- MRS היו קשרים קודמים ל- CVD בספרות או נתוני GWAS, וכי מספר אתרי מתילציה חופפים לאלה המתילציה באופן דיפרנציאלי ברקמת פלאק אבי העורקים.
בשלב הבא, הצוות ביצע ניתוחי אימות של אתרי המתילציה הקשורים ל- IMEs בקבוצות אופטימליות ואפי-פוטסדאם. הם אישרו 43 ו- 32 אתרי מתילציה בקבוצות אופטימטיות ואפי-פוטסדאם, בהתאמה, באמצעות מודלים של רגרסיה של COX המותאמים ל- BMI, גיל, מין ו- HBA1C. יתר על כן, חמישה מתוך 87 אתרים ב- MRS היו קשורים ל- IMEs בקבוצה האופטימלית.
MRS שפותח באמצעות חמשת האתרים הללו (MRS5Sites) היה שונה באופן משמעותי בין בקרות לאנשים עם IMEs בקבוצה האופטימלית לבין הקבוצה הפוטנציאלית של MES ב- T2D. לשילוב של גורמי סיכון קליניים ו- MRS5Sites היה AUC של 0.8 בקבוצה האופטימלית ו- 0.78 בקבוצה הפוטנציאלית של MES ב- T2D. ראוי לציין כי אופטימיזציה כללו משתתפי T2D שאובחנו לאחרונה, ואילו Epic-Potsdam היה קבוצת אוכלוסייה כללית, התומכת ביישנות רחבה יותר של הממצאים.
מסקנות
לסיכום, המחקר זיהה ותוקף סמן ביולוגי מבוסס דם, שחזה את הסיכון של ה- ME הראשון, בשילוב עם גורמי סיכון קליניים ללא תלות, אצל אנשים שאובחנו לאחרונה עם T2D. נבדקי T2D עם MRS בשילוב עם גורמי סיכון קליניים של יותר מ- 0.023, עשויים לפתח MES במהלך המעקב המרבי של שבע שנים. בסך הכל, הסמן הביולוגי האפיגנטי מנבא את IMEs טוב יותר מציוני סיכון מבוססים, ותומך בשימוש הקליני העתידי שלו.
עם זאת, המחברים מציינים כי יש צורך באימות חיצוני באתניות אחרות, וכי ה- PPV המתון משקף ככל הנראה את השכיחות הנמוכה של אירועים באוכלוסייה שזה עתה אובחנו. הם גם מזהירים כי גורמים סביבתיים כמו תזונה, פעילות גופנית ותרופות יכולים להשפיע על מתילציה של DNA, וכי אלה לא נלכדו במלואם בקבוצות הנוכחיות.