סריקות מוח של יילוד חושפות כיצד גרסאות גנטיות הקשורות לאוטיזם משפיעות על חיווט עצבי מוקדם, ומציעות תובנות טריות על מקורותיהם של הבדלים נוירו-התפתחותיים.
מחקר: אוטיזם גרסאות נפוצות הקשורות לשינויים בחומרים לבנים בלידה: ניתוחים מבוססי-חתך מבוסס פיקדל של 221 ילודים ילידי אירופה מהפרויקט המתפתח של Connectome Connectome. קרדיט תמונה: atthapon raksthaput / shutterstock
במחקר שפורסם לאחרונה בכתב העת פסיכיאטריה תרגומיתקבוצה של חוקרים בדקה את הקשר בין גרסאות גנטיות נפוצות הקשורות לאוטיזם לבין וריאציות מבניות בחומר הלבן בקרב ילודים ילידי מונחים, והדגישו אסוציאציות פוטנציאליות שעשויות לתרום למחקר עתידי על סמני אוטיזם מוקדמים ולא לשמש כסמנים ביולוגיים מוחלטים.
רֶקַע
הפרעת ספקטרום אוטיזם (ASD) משפיעה על כ -1 מכל 100 ילדים ברחבי העולם, ובכל זאת אבחנה מוקדמת נותרה אתגר. מחקרים מתעוררים מראים כי הבדלים בחומר הלבן – רשת התקשורת של המוח – יכולים להתגלה בינקותם ועלולים לשמש אינדיקטורים מוקדמים לאוטיזם.
חומר לבן מתפתח במהירות במהלך ההיריון והינקות, ויוצר קשרים עצביים חיוניים התומכים בקוגניציה ובתפקוד מוטורי. גורמים גנטיים ממלאים תפקיד מכריע בתהליך זה, אך השפעתם המדויקת נותרה לא ברורה.
ההתקדמות בהדמיה עצבית מאפשרת כעת לחוקרים למפות את השינויים המוח המוקדמים הללו, לשפוך אור על האופן בו נטייה גנטית מעצבת מסלולי עצבים. הבנת קישורים אלה עשויה להוביל להתערבויות קודמות, ולשפר את התוצאות לילדים בסיכון לאוטיזם.
בעוד שמחקרים בדקו את הבדלי החומר הלבן בקרב ילדים גדולים יותר, מעט מאוד ידוע על האופן בו גרסאות גנטיות משפיעות על מבנה המוח בילודים, ומחייבים חקירה נוספת.
על המחקר
המחקר הנוכחי ניתח מבני חומר לבן אצל 221 תינוקות ילידי מונחים של אבות אירופאים מהפרויקט המתפתח של Connectome Connectome. הדמיה משוקללת דיפוזיה מתקדמת שימשה לתפוס סריקות מוח ברזולוציה גבוהה, מה שמאפשר לחוקרים לבחון צפיפות סיבים מיקרוסקופיים ומורפולוגיה מקרו-מבנית. עיבוד מקדים של נתונים כלל הפחתת רעש, תיקון תנועה ונורמליזציה לתבנית מוח ספציפית למחקר.
ניתוח גנטי כלל דגימות רוק שנאספו בלידה או 18 חודשים, שעובדו כדי לזהות סמנים גנטיים נפוצים הקשורים לאוטיזם. מדדי בקרת איכות הבטיחו אמינות נתונים, למעט דגימות עם מידע גנטי לא שלם. ציונים פוליגניים, המייצגים סיכון אוטיזם מצטבר, חושבו על סמך מחקרי אסוציאציה רחבי גנום והותאמו להבדלי אבות.
מודלים סטטיסטיים העריכו את הקשר בין סיכון גנטי למבנה החומר הלבן, המהווים משתנים כמו נפח מוח מוחלט, גיל הריון ומין. ניתוח העשרה מוגדר גנים נערך כדי לזהות מסלולים ביולוגיים הקשורים לשינויים בחומר לבן הקשורים לאוטיזם. ניתוחים נוספים בוצעו כדי לבחון אם מסלולים גנטיים ספציפיים השפיעו על ההבדלים המבניים בקישוריות החומר הלבן.
תוצאות המחקר
תינוקות עם ציונים פוליגניים בעלי אוטיזם גבוה יותר הראו עלייה משמעותית בחתך רוחב של אגרוף הסיבים ברדיאטה העולה העולה השמאלית, אזור מוח המכריע לתפקודים מוטוריים וקוגניטיביים. זה מצביע על כך שנטייה גנטית לאוטיזם עשויה לעצב את ארגון החומר הלבן המוקדם, אם כי יש צורך במחקרים נוספים כדי לאשר את משמעותו לתוצאות התפתחותיות מאוחרות יותר.
ניתוח נוסף הצביע על כך שמאפייני החומר הלבן המיקרוסקופי נותרו ללא שינוי, בעוד שהבדלים מקרו -מבניים בולטים ברדיאטה של קורונה מעולה ובדרכים קשורים. ממצאים אלה תואמים עם מחקרים קודמים המדווחים על נפח החומר הלבן אצל תינוקות ופעוטות שאובחנו אחר כך עם אוטיזם. עם זאת, המחקר לא מצא הבדלים מיקרו-מבניים משמעותיים, מה שמרמז כי השינויים שנצפו קשורים יותר לחתך של צרור סיבים ולא לצפיפות או לארגון ברמה המיקרוסקופית.
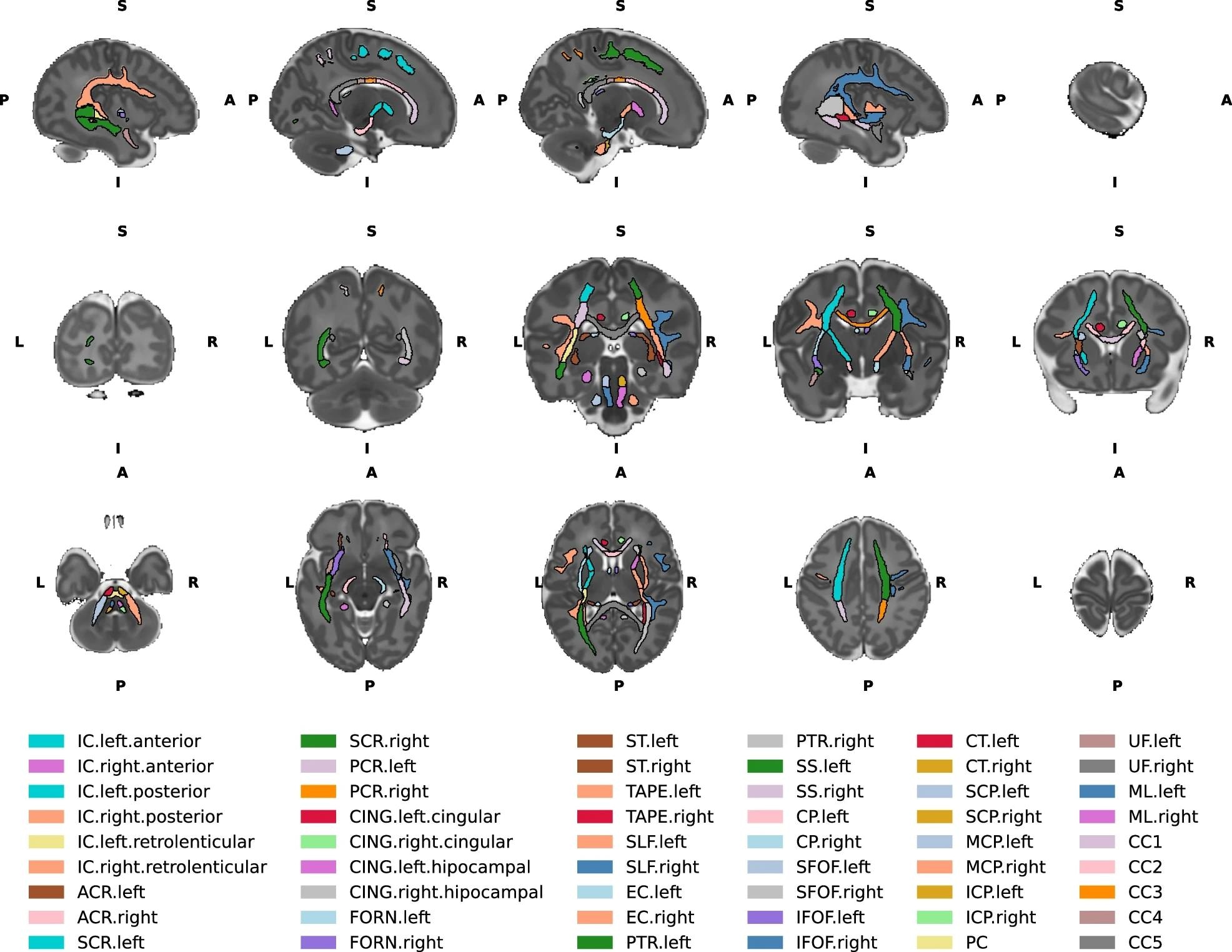
שורה עליונה – מבט משמאל לימין של פרוסות המוח. שורה אמצעית אחורית לתצוגה כלילית קדמית של פרוסות המוח. שורה תחתונה – נחותה מנוף צירי מעולה של פרוסות המוח. כמוסה פנימית של IC, Acr adterior Corona Radiata, SCR Corona Radiata, PCR Corona Radiata אחורי, Cingulum Cingulum, Forn Fornix, St stria terminalis, Slf מעולה אורך מעולה, Cabsula חיצוני, קריאה של PTR Thalamic, Ssgitulus sgitulus, cperclal cperclal cperclal cpertal cperlal cpebral sagital sagital sagital sagtal, SFOF Fasciculus פרונט-אוקפיטל מעולה, אם חזית נחותה נחותה אוקסיפיטלית פסיקולוס, CT Corticospinal Tract, Peduncle Cerebellar McP, Peduncle mcp Middle, Peduncle Celebellar Percus pertsul Callosul Callosul, CALSULS, CALSULS PRESSULA, CALSULS, CALSULS CALLAS, CC1, , CC2 PREMOTOR/PELLEMERING PART, CC3 CORPUS CALLOSUM חלק מנוע, CC4 CORPUS CALLOSUM חלק חושי, CC5 CORPUS CALLOSUM PARIETAL/TEMPORAL/OCCIPITAL. L- שמאל, R- ימין, א-קדמי, p- אחורי, s-superior, i- נחות.
חקירה עמוקה יותר של דפוסי קישוריות המוח העלתה כי תינוקות עם ציונים פוליגניים אוטיזם גבוהים יותר העלו את אזורי החתך בדרכי החומר הלבן הנוספות, כולל נתיבים המעורבים בעיבוד סנסורימוטורי וקוגניטיבי. שינויים אלה עשויים למלא תפקיד בקישוריות המוח הלא טיפוסית שנצפתה אצל אנשים עם אוטיזם.
ניתוח מסלול גנטי חשף כי הגרסאות הקשורות לאוטיזם הקשורות לשינויים בחומר לבן הוצגו יתר על המידה בגנים הקשורים לקישוריות עצבית ותפקוד סינפטי. ראוי לציין כי גנים כמו MAPT, KCNN2 ו- DSCAM – המעורבים באופן מובהק בסיכון לאוטיזם – הודגשו במחקר, מה שמחזק את ההשערה כי שינויים בחומר לבן קשורים לתהליכים עצביים התפתחותיים החיוניים לתפקוד קוגניטיבי ומוטורי.
אף על פי שמובהקים סטטיסטית, גדלי האפקט היו קטנים, וכמה ממצאים – כמו אלה שקשורים לרדיאטה של קורונה מעולה הנכונה – לא שרדו תיקוני בדיקות מרובות, מה שמצביע על הצורך באימות נוסף.
ממצאים אלה מראים כי שינויים בחומרים לבנים בילודים משקפים השפעות גנטיות על התפתחות המוח המוקדמת ולא משמשות כסמנים ביולוגיים מוחלטים לאוטיזם. אם תוקף במחקרים גדולים יותר, תוצאות אלה עשויות להיות בעלות השלכות עמוקות על אסטרטגיות סינון והתערבות מוקדמות, מה שמאפשר תמיכה התפתחותית יזומה לפני שיופיעו תסמינים התנהגותיים.
מסקנות
לסיכום, ממצאים אלה מדגישים את ההשפעה העמוקה של הגנטיקה על התפתחות המוח המוקדמת. על ידי זיהוי הבדלי מוח מבניים בלידה, החוקרים מתקרבים להבנת מקורותיו המוקדמים ביותר של אוטיזם.
איתור שינויים אלה מוקדם יכול לתרום למחקר על התערבויות בהתאמה אישית, מה שמאפשר טיפולים ממוקדים לפני שיופיעו תסמינים התנהגותיים. עם זאת, המחקר אינו מציע כי טכניקות הדמיה עצבית עכשווית יכולות לחזות באופן אמין אוטיזם אצל ילודים. ככל שמדעי המוח מתקדמים, שילוב תובנות גנטיות עם הדמיה עצבית עשוי לעזור לחזות תוצאות התפתחות עצביות, ובסופו של דבר לשפר את חייהם של אנשים עם אוטיזם ומשפחותיהם.
מחקר עתידי צריך לחקור כיצד שינויים מבניים מוקדמים אלה קשורים להתפתחות קוגניטיבית והתנהגותית לטווח הארוך, תוך עיצוב אסטרטגיות חדשות להתערבות ותמיכה מוקדמת.