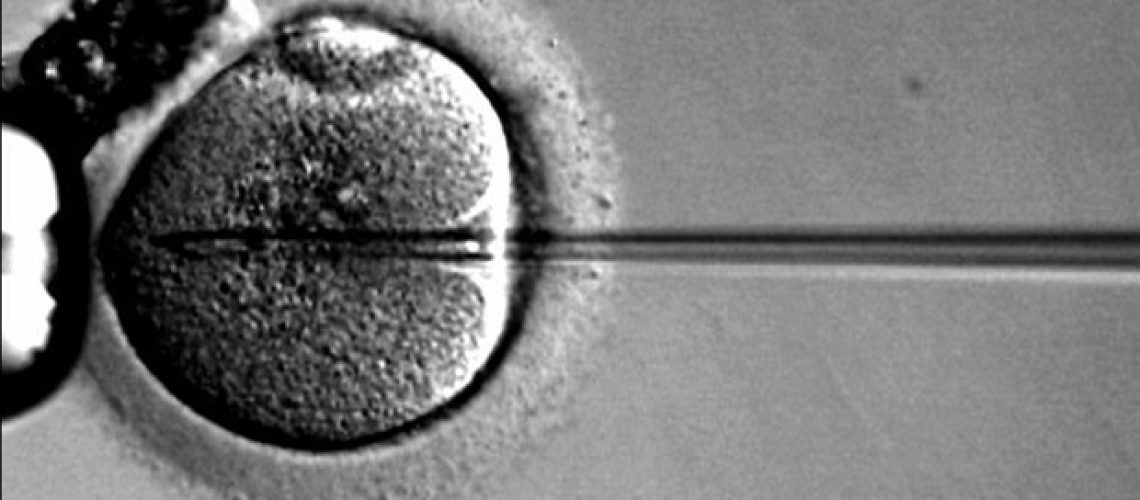
מחקר חדש בהובלת חוקרים מ-Mass Eye and Ear, חבר ב-Mas General Brigham, הדגים את היעילות של טיפול גנטי לשיקום תפקוד השמיעה לילדים הסובלים מחרשות תורשתית. בניסוי של שישה ילדים שהתקיים בבית החולים Eye & ENT של אוניברסיטת פודן בשנגחאי, סין, החוקרים מצאו את הטיפול הגנטי החדש כטיפול יעיל לחולים עם צורה ספציפית של חירשות אוטוזומלית רצסיבית הנגרמת על ידי מוטציות של OTOF גן (אוטופרלין)., נקרא DFNB9. עם המטופל הראשון שלו שטופל בדצמבר 2022, מחקר זה מייצג את הניסוי הקליני הראשון בבני אדם למתן תרפיה גנטית לטיפול במצב זה, עם הכי הרבה חולים שטופלו והמעקב הארוך ביותר עד כה. התוצאות שלהם מתפרסמות ב-24 בינוארה' ב ה-Lancet.
אם ילדים אינם מסוגלים לשמוע, המוח שלהם יכול להתפתח בצורה חריגה ללא התערבות. התוצאות מהמחקר הזה באמת יוצאות דופן. ראינו את יכולת השמיעה של ילדים משתפרת באופן דרמטי משבוע לשבוע, כמו גם את החזרת הדיבור שלהם".
Zheng-Yi Chen, DPhil, מדען עמית במעבדות Eaton-Peabody ב-Mass Eye and Ear ופרופסור חבר לניתוחי אף-אוזן-גרון-ראש צוואר בבית הספר לרפואה של הרווארד
אובדן שמיעה משפיע על יותר מ-1.5 מיליארד אנשים ברחבי העולם, כאשר חירשות מולדת מהווה כ-26 מיליון מהאנשים הללו. לאובדן שמיעה בילדים, יותר מ-60 אחוז נובעים מסיבות גנטיות. DFNB9 למשל, היא מחלה תורשתית הנגרמת על ידי מוטציות של OTOF גן וכישלון בייצור חלבון אוטופרלין מתפקד, הדרוש להעברת אותות הקול מהאוזן למוח. אין כיום תרופות מאושרות על ידי ה-FDA המסייעות לחירשות תורשתית, מה שפתח את הדלת לפתרונות חדשים כמו טיפולים גנטיים.
על מנת לבדוק טיפול חדשני זה, נצפו שישה ילדים עם DFNB9 במשך תקופה של 26 שבועות בבית החולים Eye & ENT של אוניברסיטת Fudan. משתפי הפעולה של Mass Eye and Ear השתמשו בוירוס קשור אדנו (AAV) הנושא גרסה של האדם OTOF גן להחדרת הגן בזהירות לאוזניים הפנימיות של המטופלים באמצעות הליך כירורגי מיוחד. נעשה שימוש במינונים שונים של הזרקה בודדת של הווקטור הנגיפי.
לכל ששת הילדים במחקר הייתה חירשות מוחלטת, כפי שמצוין על ידי סף תגובת גזע מוח שמיעתי (ABR) ממוצע של מעל 95 דציבלים. לאחר 26 שבועות, חמישה ילדים הפגינו התאוששות שמיעה, והראו הפחתה של 40-57 דציבל בבדיקת ABR, שיפורים דרמטיים בתפיסת הדיבור והיכולת המשוחזרת לנהל שיחה רגילה. בסך הכל, לא נצפתה רעילות מגבילת מינון. במהלך המעקב אחר החולים, נצפו 48 תופעות לוואי, כאשר רובן המשמעותי (96%) היו בדרגה נמוכה, והשאר חולפים ללא השפעה ארוכת טווח.
ממצאי הניסוי יוצגו גם ב-3 בפברוארמחקר ופיתוח במפגש שנתי של האגודה למחקר באף אוזן גרון.
מחקר זה מספק ראיות לגבי הבטיחות והיעילות של טיפולים גנטיים בטיפול ב-DFNB9, כמו גם הפוטנציאל שלהם לצורות אחרות של אובדן שמיעה גנטי. יתרה מכך, התוצאות תורמות להבנת הבטיחות של החדרת AAV לאוזן הפנימית האנושית. לגבי השימוש ב-AAV, ההצלחה של וקטור AAV כפול הנושא שני חלקים של OTOF הגן בולט. בדרך כלל, ל-AVS יש מגבלת גודל גנים, וכך גם לגן כמו OTOF שחורג מהגבול הזה, ההישג עם וקטור ויראלי כפול פותח את הדלת לשימוש של AAV עם גנים גדולים אחרים שהם בדרך כלל גדולים מדי עבור הווקטור.
"אנחנו הראשונים שיזמו את הניסוי הקליני של OTOF טיפול גנטי. זה מרגש שהצוות שלנו תרגם את העבודה ממחקר בסיסי במודל בעלי חיים של DFNB9 לשיקום שמיעה אצל ילדים עם DFNB9", אמר מחבר המחקר הראשי Yilai Shu, MD, מבית החולים Eye & ENT של אוניברסיטת פודן באוניברסיטת פודן. שו בעבר שימש כעמית בתר-דוקטורט במעבדה של חן ב-Mass Eye and Ear, "אני באמת נרגש מהעבודה העתידית שלנו על צורות אחרות של אובדן שמיעה גנטי כדי להביא טיפולים ליותר מטופלים".
החוקרים מתכננים להרחיב את הניסוי לגודל מדגם גדול יותר וכן לעקוב אחר התוצאות שלהם לאורך ציר זמן ארוך יותר.
"לא מאז שהומצאו שתלי שבלול לפני 60 שנה, לא היה טיפול יעיל לחירשות", אמר חן. "זהו אבן דרך ענקית המסמלת עידן חדש במאבק נגד כל סוגי אובדן השמיעה".