במכתב מחקר שפורסם לאחרונה בכתב העת הזדקנות הטבע, חוקרים השתמשו ברצף פרוטאומי של נוזלי המוח והשדרה של החולים והבקרות כדי לחקור את ההטרוגניות של מחלת האלצהיימר. הממצאים שלהם חשפו חמישה תת-סוגים מולקולריים שמתארים גורמי סיכון גנטיים ופתולוגיות מחלות שונות, כולל שיעורי התקדמות וזמני הישרדות. תוצאות אלו מצביעות על דרישות התערבות שונות לכל תת-סוג ומדגישות את הצורך ברפואה מותאמת אישית כדי לאבחן ולטפל במצב.
מכתב: פרוטאומיקת נוזל מוחי בחולים עם מחלת אלצהיימר חושפת חמישה תת-סוגים מולקולריים עם פרופילי סיכון גנטי מובהקים. קרדיט תמונה: Lightspring / Shutterstock
מחלת אלצהיימר והיתרונות של פרוטאומיקה
מחלת אלצהיימר (AD) היא הפרעה מוחית מתקדמת המשפיעה בעיקר על אנשים מבוגרים, המאופיינת בהתנוונות של נוירונים האחראים על זיכרון וקוגניציה. על פי ההערכות, זה משפיע על 5% מהאנשים בין הגילאים 65-74, 13.1% בין 75-84 ו-33.3% מעל גיל 84, המשפיעים כיום על 44 מיליון אנשים, כאשר מספר זה עולה מדי שנה. AD מוכרת כגורם המוביל לדמנציה ברחבי העולם, ללא תרופה ידועה כיום והטיפול מוגבל לניהול סימפטומים. בעוד שבסיס סופי למחלה טרם זוהה, הגנטיקה והחשיפה הסביבתית אחראית למצב.
מחקר שנערך לאחרונה זיהה ש-AD איננה מחלה יחידה אלא מונח גג עבור ספקטרום של מצבים המשתנים באופן משמעותי ברמה המולקולרית. למרבה הצער, התקדמות המחקר הללו מבטלת חלק גדול של ספרות קודמת שניסתה להבהיר את הפתופיזיולוגיה הקלינית של AD, בהתחשב בכך שחולים שונים עשויים להגיב בצורה שונה משמעותית לאותה חשיפה קלינית.
'פרוטאומיקה' היא חקר האינטראקציות, התפקוד, ההרכב והמבנים של חלבונים ופעילויותיהם התאיות. הוא משלב טכניקות רצף חדשניות של 'הדור הבא' כגון ספקטרומטריית מסה (MS) לזיהוי ואפיון של אלפי תת-יחידות חלבון בנוזלים ביולוגיים. נוזל המוח השדרתי (CSF) הוא הנגיש ביותר מבין הנוזלים הביולוגיים הללו הקשורים למצבים נוירולוגיים בשל המגע המתמיד שלו עם המוח ומערכת העצבים המרכזית (CNS) ותפקידו כפרוקסי לתהליך הפתופיזיולוגי של המוח.
לגבי המחקר
במחקר הנוכחי, החוקרים השתמשו בגישת קוהורט-מקרה-ביקורת, תוך שימוש ב-CSF מחולי AD ובקרות בריאות תואמות גיל, כדי לחשוף את החלבונים המווסתים באופן דיפרנציאלי מעלה ומטה בקבוצות אלה באמצעות ניתוחים פרוטאומיים. קבוצת המדגם של המחקר נגזרה מ-Amsterdam Dementia Cohort (ADC), מחקר מתמשך של כל החולים שביקשו טיפול במרכז לאלצהיימר באמסטרדם מאז שנת 2000.
קריטריוני ההכללה של המחקר כללו AD מאובחן, שאושר על סמך נוכחות של סמן עמילואיד לא תקין (מקרים) ובקרות תואמות גיל, מין ודמוגרפיה. CSF משתי העוקות נאסף ונתון לכרומטוגרפיה נוזלית בעלת ביצועים גבוהים (HPLC) ספקטרומטריית מסה (MS) – LC-MS/MS. לאחר מכן נעשה שימוש בבדיקות אימונוסורבנטיות מקושרות אנזים (ELISA) למדידת עמילואיד-β42t-tau, p-tau 181, ויחס עמילואיד-β42/עמילואיד-β40, הקובעים העיקריים של חומרת AD ושלב ההתקדמות.
דגימות דם ממקרים וביקורות הועברו עוד יותר לאפוליפופרוטאין E (APOE) גנוטיפ כדי לסנן פולימורפיזמים חד-נוקלאוטידים הידועים כמעצימים או מדכאים AD. הדמיית תהודה מגנטית משוקלת T1 (MRI) שימשה כדי להמחיש דפוסי ניוון מוחיים ולהעריך את ההבדלים בתמונת העצב של חולי AD ושל הבקרות. לבסוף, סוללות בדיקה נוירופסיכולוגיות סטנדרטיות ניתנו לנבדקים במהלך ההרשמה הראשונית, עם מעקב שנתי כדי להעריך את קצב ומידת התקדמות AD.
ממצאי המחקר
המחקר הנוכחי כלל 609 מקרים ו-187 ביקורת. מתוך המקרים של AD שנכללו, 107 הראו קוגניציה תקינה, 103 הראו ליקוי קוגניטיבי קל (MCI), ו-209 הראו דמנציה. ניתוחי LC-MS/MS זיהו 3,863 חלבוני CSF ייחודיים, מתוכם 1,309 חלבונים (28,408 פפטידים) היו משותפים לכל המשתתפים שנכללו ושימשו לניתוחים נוספים. מתוכם, ניתוחי אשכולות חשפו 1,058 חלבונים הקשורים ל-AD. שילוב של תוצאות מקבץ עם מאפיינים קליניים של מטופלים גילה חמישה תת-סוגים נפרדים של AD.
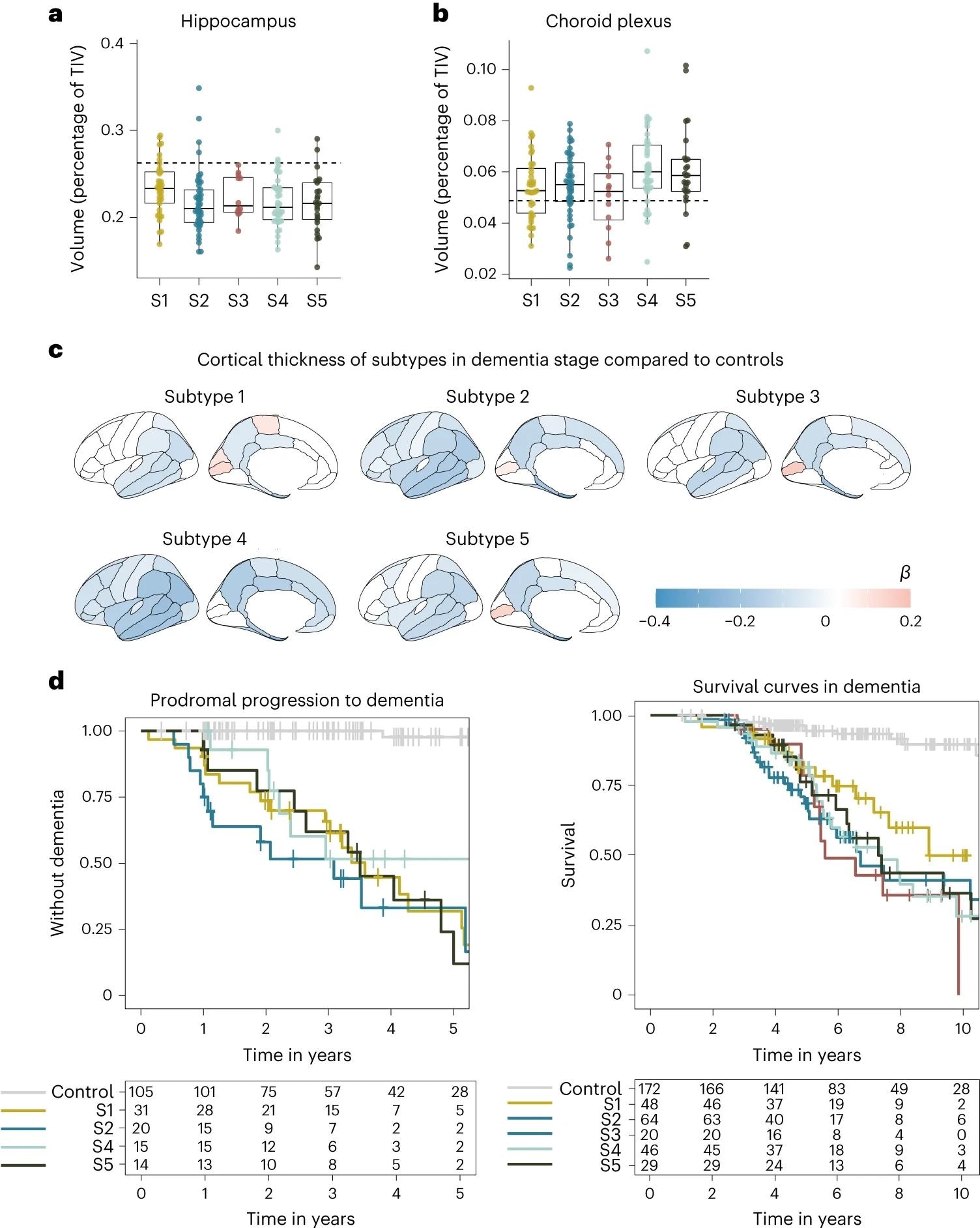 אנפח ההיפוקמפוס החציוני כאחוז מהנפח התוך גולגולתי הכולל (TIV) בהשוואה לתתי סוגים בשלב הדמנציה. בנפח מקלעת הכורואיד כאחוז של TIV בהשוואה לתתי סוגים בשלב הדמנציה. ג, ניוון קורטיקלי הקשור לתתי-סוגים של AD בשלב הדמנציה בהשוואה לביקורות (n=160). β מציין עובי קליפת המוח הממוצע במ"מ, בממוצע על פני ההמיספרה הימנית והשמאלית ומותאם לגיל ולמין. ד, התקדמות קלינית מ-MCI לדמנציה לפי תת-סוג (משמאל; לא כולל תת-סוג 3 עקב n=2) וזמן מדמנציה למוות לפי תת-סוגים (ימין). כל מדדי ניוון מבוססים על אנשים עם דמנציה בלבד. א,ב, עלילות הקופסה מתארות את החציון במרכז; הגבולות מציינים את הרבעון הראשון והשלישי, בעוד שהשפם מתרחב למעלה ולמטה עד פי 1.5 מהטווח הבין-רבעוני (מוגבל לנקודות נתונים שנצפו בפועל), והנקודות מצביעות על ערכי אדם בודדים (תת-סוג 1, n = 37; תת-סוג 2, n = 45; תת-סוג 3, n = 12; תת-סוג 4, n = 40; תת-סוג 5, n = 25).
אנפח ההיפוקמפוס החציוני כאחוז מהנפח התוך גולגולתי הכולל (TIV) בהשוואה לתתי סוגים בשלב הדמנציה. בנפח מקלעת הכורואיד כאחוז של TIV בהשוואה לתתי סוגים בשלב הדמנציה. ג, ניוון קורטיקלי הקשור לתתי-סוגים של AD בשלב הדמנציה בהשוואה לביקורות (n=160). β מציין עובי קליפת המוח הממוצע במ"מ, בממוצע על פני ההמיספרה הימנית והשמאלית ומותאם לגיל ולמין. ד, התקדמות קלינית מ-MCI לדמנציה לפי תת-סוג (משמאל; לא כולל תת-סוג 3 עקב n=2) וזמן מדמנציה למוות לפי תת-סוגים (ימין). כל מדדי ניוון מבוססים על אנשים עם דמנציה בלבד. א,ב, עלילות הקופסה מתארות את החציון במרכז; הגבולות מציינים את הרבעון הראשון והשלישי, בעוד שהשפם מתרחב למעלה ולמטה עד פי 1.5 מהטווח הבין-רבעוני (מוגבל לנקודות נתונים שנצפו בפועל), והנקודות מצביעות על ערכי אדם בודדים (תת-סוג 1, n = 37; תת-סוג 2, n = 45; תת-סוג 3, n = 12; תת-סוג 4, n = 40; תת-סוג 5, n = 25).
תת-סוג 1 מאופיין על ידי היפרפלסטיות נוירונית, תת-סוג 2 על ידי הפעלה חיסונית מולדת, תת-סוג 3 על ידי חוסר ויסות RNA, תת-סוג 4 על ידי תפקוד לקוי של מקלעת choroid, ותת-סוג 5 על ידי הפרעה בתפקוד מחסום דם-מוח. APOE גנוטיפ אימת אשכולות מזוהים והציע בסיס גנטי ייחודי לכל תת-סוג.
"יש לציין כי כל תת-סוג היה קשור לגורמי סיכון גנטיים שונים של AD, מה שמעיד על כך שכל תת-סוג של AD CSF משקף מנגנונים מולקולריים ספציפיים. תת-הסוגים היו שונים גם בדפוסי ניוון קליפת המוח ובזמני הישרדות, מה שמדגיש את הרלוונטיות הקלינית שלהם".
התת-סוגים נמצאו שונים באופן משמעותי על ידי הפתולוגיה הקלינית שלהם, כפי שהודגש על ידי בדיקות נוירופיזיולוגיות – תת-סוג 3 היה אגרסיבי יותר באופן משמעותי בקצב ההתקדמות שלו בהשוואה לתתי הסוגים האחרים. בהתחשב במידת הייחודיות הגנטית והפתופיזיולוגית של תת-סוגים אלו, מתברר הצורך ברפואה מותאמת אישית.
"…תופעות לוואי הנובעות מטיפולים מסוימים עשויות להיות תלויות גם בתת-סוג. לדוגמה, בעוד נוגדנים עשויים לחצות ביתר קלות את מחסום הדם-מוח בתת-סוג 5, אנשים אלו עשויים להיות בסיכון מוגבר לדימום מוחי שיכול להתרחש עם טיפול נוגדנים."
מסקנות
המחקר הנוכחי השתמש בפרוטאומיקה כדי לחקור את ההבדלים הספציפיים למטופל בפרופילים הגנטיים והפתופיזיולוגיים תחת מטריית AD. ממצאי מחקר חושפים יותר מ-1,000 חלבונים המובעים באופן דיפרנציאלי בחולי AD, וחשוב מכך, ש-AD מורכבת לפחות מחמישה תת-סוגים שונים הנבדלים בבסיסם הגנטי והקליני.
"בהתחשב בדפוסים המובהקים של תהליכים מולקולריים ופרופילי סיכון גנטיים של AD, סביר להניח שתתי-סוגים של AD ידרשו טיפולים ספציפיים. לדוגמה, אנשים תת-סוג 1 עשויים להפיק תועלת מטיפולים המפעילים TREM2, תת-סוג 2 ממעכבי חיסון מולדים, תת-סוג 3 מאנטיסנס. אוליגונוקלאוטידים שמשחזרים עיבוד RNA, תת-סוג 4 מעיכוב חדירת מונוציטים ותת-סוג 5 מטיפולים מוחיים".