צלילה עמוקה במרכז הפיקוד של המוח לרעב מראה כיצד פענוח מעגליו יכול להפוך את העתיד של טיפולי הרזיה.
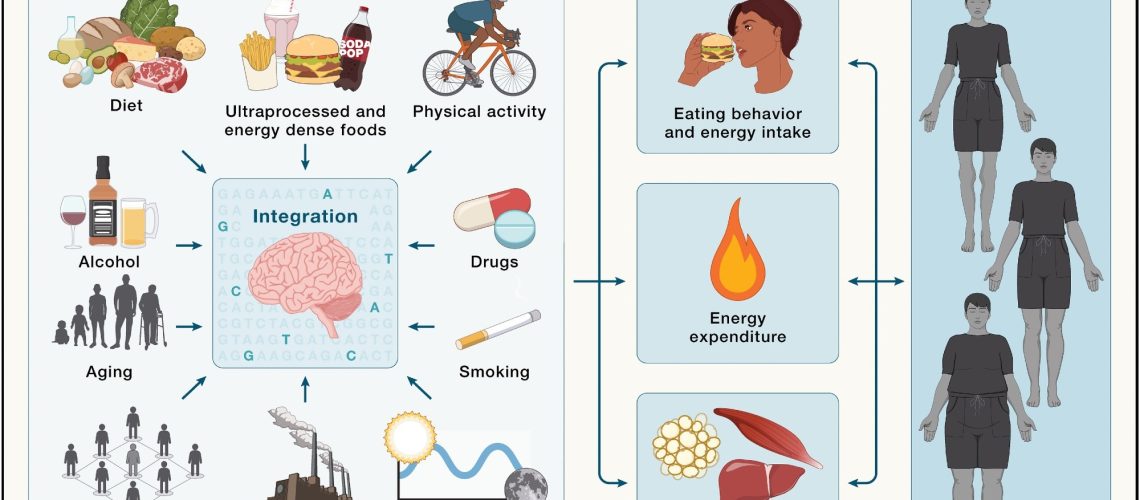
שילוב מוחי של רמזים סביבתיים בוויסות איזון אנרגיה ואדיפות – גורמים סביבתיים (משמאל) משולבים על ידי המוח בהקשר של האיפור הגנטי של האדם (מאויר על ידי SNPs מודגשים) ופרופיל אפיגנטי. בתגובה, המוח מווסת את התפוקות ההתנהגותיות והפיזיולוגיות, כגון צריכת אנרגיה, הוצאות אנרגיה וחלקת דלק (אמצע), אשר כולם משפיעים על איזון האנרגיה, ובסופו של דבר מעצבים שונות בין -אינדיבידואלית בשומן (מימין).
בסקירה שפורסמה לאחרונה בכתב העת תָאקבוצה של מחברים סינתזה כיצד מערכת העצבים המרכזית (CNS) משלבת אותות נוירואנדוקריניים כדי לשלוט בהומאוסטזיס באנרגיה ולתרגם מנגנונים אלה לפרמקותרפיה בטוחה ויעילה באנטי-ביטולית.
רֶקַע
כיצד הפכה מערכת הישרדות למשבר בריאות עולמי? מאז שנות השמונים, שיעורי ההשמנה זינקו, והפכו כעת למיליארד אנשים ברחבי העולם, כאשר מחלות לב וכלי דם מניעות את רוב מקרי המוות הקשורים להשמנה. גנטיקה וסביבה מקיימים אינטראקציה: גופים מסוימים מתוכננים לעלות במשקל (השערת "גן נסחף"), אחרים מתנגדים, ורמזי מזון מודרניים וגורמי לחץ מגבירים את הפער.
פתוגנזה של השמנת יתר כרוכה במנגנוני "דחיפה" (היפרפגיה מונעת מוח) ו- "משיכה" (סחיטת דלק היקפית). בינתיים, מעגלי מוח התפתחו כדי להגן על חנויות אנרגיה, ולא על התזונה האולטרה-מעובדת של ימינו. הבנת האופן בו המוח, הבטן, רקמת השומן והכבד שיחה היא המפתח לפיתוח טיפולים בטוחים ויעילים נגד השמרה. יש צורך במחקר נוסף כדי למפות מעגלים עצביים ונוירופלסטיות תלויה בפעילות המאפשרת ירידה במשקל ארוכת טווח.
מפה נוירואנדוקרינית של הומאוסטזיס אנרגיה
המוח בוררות את איזון האנרגיה על ידי מיזוג אותות שומן איטי עם רמזים מהירים וקשרי ארוחה. רקמות שומן ממסירות סטטוס דרך לפטין, ואילו דרכי העיכול (GI) משחררת הורמונים כמו פפטיד -1 דמוי גלוקגון (GLP-1), פוליפפטיד תלוי גלוקוז (GIP), cholecystokinin (cck), פפטיד ימיה (pyy), gelecystokinin (cck), peptide yy (pyy), gexy and grelin and grelin the grelin and grelin the grelin the grelin זה (grelin) (grelin) ( קיבה כדי לעורר תיאבון באמצעות נוירונים פפטיד הקשורים לאגוטי (AGRP). אותות אנדוקריניים אלה משלימים אפורים נרתיקיים ועמוד השדרה שחשים התרחבות מעי וחומרים מזינים, ומעניקים ל- CNS משוב מהיר.
יחד, תשומות אנדוקריניות ועצביות מתאמות עיכול, שובע והומאוסטזיס מטבולי. הכבד מוסיף את קולו, גורם גידול פיברובלסט 21 (FGF21), גורם צמיחה דמוי אינסולין 1 (IGF-1), ופפטיד אנטי-מיקרוביאלי 2 (LEAP2), ואילו מטבוליטים קטנים וחומצות מרה מסובבים את ההודעה.
מעגלים היפותלמיים: קביעת תקציב האנרגיה
לגרעין הקשת (ARC), הסמוך לחציון החציוני (איבר עקבי (CVO)), יש גישה מיוחסת להורמונים ומטבוליטים המסתובבים. נוירונים של קשת מבטאים קולטנים ללפטין, גרלין ואינסולין ומקבלים תשומות מההיפותלמוס paraventricular (PVH), היפותלמוס Ventromedial (VMH), והיפותלמוס הדורסומדיאלי (DMH), וגרעין של StriaSt (DMH), StriaSt TriaSt. (NTS).
נוירונים AGRP מקדמים רעב משחררים חומצה γ-aminobutyric (GABA), נוירופפטיד y (NPY) ו- AGRP כדי לעכב מעגלי שובע, ואילו פרו-אופיומלנוקורטין (POMC) משחררים את המנועים של McOnocortin (α-msh) (α-msh) (α-msh) (α-msh) (α-msh) (α-msh) (α-msh) (α-msh) (α4) ( צריכה. פלסטיות סינפטית במעגלים אלה (למשל, ארגון מחדש תלוי לפטין של תשומות) מסתגל למצבי אנרגיה. תפוקות קשת אלה מקרינות באופן נרחב, ומאפשרות לרשתות היפותלמיות להגדיר תיאבון והוצאות.
שליטה אחורית ומוח נרתיק: שובע ללא מחלה
קומפלקס הנרתיק הגבי (DVC) משלב אותות קרביים להפסקת הארוחות. ב- NTS, נוירונים של קולטן קלציטונין (CALCR), כולל תת-קבוצה של פפטיד משחרר פרולקטין (PRLH), מדכאת האכלה ללא סלידה ויכולה לרסן את הרעב מונע AGRP דרך מסלולי פוליסינפט.
לעומת זאת, מעגלי Postrema (AP) יכולים לזווג דיכוי תיאבון עם סבל: גורם בידול צמיחה 15 (GDF15) פועל באמצעות תאי גלייה הנגזרים על קו הנוירוטרופיה (GDNF) קולטן משפחתי אלפא דמוי נוירונים (GFRIL) המפעילים תאים פפטיד-פטונין של CALCILED (CGRP) (CGRP) (CGRP).
ענייני איתותים ספציפיים לגלוקגון דמוי גלוקגון (GLP-1R) עניינים: פעולת GLP-1R ב- AP מניעה סלידה, ואילו פעולת GLP-1R ב- NTS מקדמת שובע, ומציעה מדוע תרופות מסוימות מרגישות חלקות יותר מאחרות.
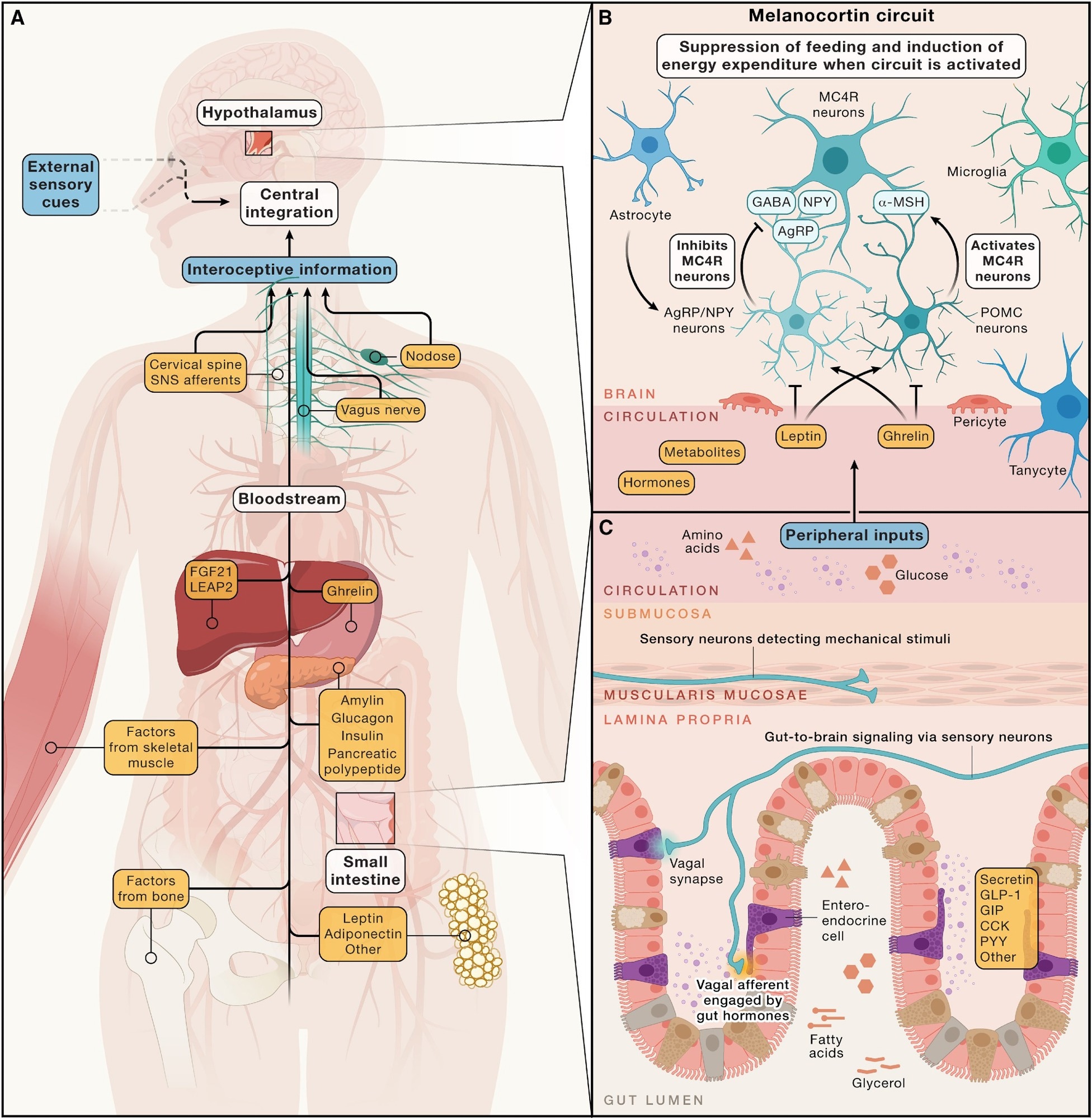
תשומות הורמונליות, מטבוליות ועצביות למעגלי מוח המווסתים הומאוסטזיס אנרגיה – (א) סקירה מפושטת של אותות היקפיים הנובעים ממערכות איברים מרובות, יחד עם רמזים חושיים מהסביבה החיצונית. אותות אלה משולבים על ידי מערכת העצבים המרכזית כדי לווסת את צריכת האנרגיה וההוצאות, תוך שמירה על שומן יציב לאורך זמן. תקנה זו כוללת שני אותות אחסון אנרגיה לטווח הארוך, כמו לפטין, והן אותות לטווח הקצר הקשורים לצריכת אנרגיה מיידית, כמו הורמונים במערכת העיכול וחומרים מזינים. (ב) הגרעין הקושרי של ההיפותלמוס מכיל את מעגל המלנוקורטין, המגיב מאוד לסטיות בהורמונים המסתובבים (למשל, אלה מהדרכי העיכול) ורקמת השולחן ומטבוליטים. מרכזי במעגל זה הם נוירונים AGRP מקדמים רעב ונוירונים POMC המקדמים שובע. אוכלוסיות עצביות אלה מווסתות את איזון האנרגיה באמצעות תשומות מעכבות ומעוררות לנוירונים המבטאים MC4R במורד הזרם, בהתאמה. (ג) תשומות היקפיות רבות המשפיעות על מעגלי מוח המווסתים את איזון האנרגיה מקורם במעיים. תאים אנטואנדוקריניים משחררים הורמונים, כמו Secretin, GLP-1, GIP, CCK ואחרים, למחזור הדם כתגובה לגירויים שונים, כמו נוכחות של חומרים מזינים לומינליים. בנוסף, אפרייני הנרתיק ממכרים מידע מכני וכימי – כמו התרחבות בטן ותכולת תזונה – ממערכת העיכול למוח למוח.
מוטיבציה ותגמול: מדוע אוכלים טעימים מנצחים
מסלולי mesocorticolimbic, תחזיות דופמין אזור טגמנטלי גחון (VTA) לגרעין Accumbens (NAC) ולקליפת המוח הקדם -פרונטלית, מקצים בולטות תמריץ לרמזים למזון. ההיפותלמוס הרוחבי (LH) מתממשק למעגלי תגמול אלה באמצעות הורמון מרכזי מלנין (MCH) ונוירונים אורקסין, המקרנים ל- VTA ו- NAC והטיה המבקשים מזון טעים. מכיוון שמערכות הומאוסטטיות והדוניות משתלבות, טיפולים יעילים חייבים לדכא את הכונן לאכול מבלי לשטוח מוטיבציה יומיומית. איתות בטן למוח באמצעות הנרתיק יכול להפעיל נוירונים דופמין לאחר חישת סוכר, ולסייע להסביר מדוע אוכלים מעובדים במיוחד מרגישים משכנעים גם ללא רמזים טעם חזקים.
ממעגלים לתרופות: מה עובד עכשיו
תרופות קודמות עבדו בעיקר באמצעות מונואמינים (דופמין, נוראפינפרין, סרוטונין), כמו בפנטרמין-טופירמט או בופרופיון-נלטרקסון, והניבו הפסד של 8% -10% עם פיצויים קרדיווסקולריים, GI ופסיכולוגיות. הנדסת פפטיד שינתה את המשחק: אלבומין הפיך מחייב מחצית חיים מורחבים של אינסטין, מה שמאפשר טיפולי GLP-1; Liraglutide ייצר הפסד מתוקן של 5.4% בתיקון פלסבו לאחר 56 שבועות אצל אנשים עם השמנת יתר ללא סוכרת.
המניע משותף של קולטן פוליפפטיד אינסולינוטרופי תלוי גלוקוז (GIPR) יכול להבהב סלידה קשורה ל- GLP-1R תוך שמירה על דיכוי צריכת, סיבה אחת מתקבלת על הדעת משיג ירידה גבוהה יותר במשקל. אגוניסטים לקולטן אמילין (AMYR), הפועלים באמצעות מתחמי חלבון (RAMP) של CALCR-קולטן (RAMP) ב- AP וב- ARC, מדכאים גם הם את צריכת העשרה ועשויים לעשות זאת עם פחות אותות סלידה. ראוי לציין כי אמייקרטין המולקולה היחידה GLP-1R/AMYR אמייקרטין הניע ירידה במשקל של 24% בניסוי שלב 1/2.
פערי ידע עם הימור בעולם האמיתי
אלמונים מרכזיים כוללים אילו אוכלוסיות עצביות מקיימות שובע שאינו מתמרץ, כיצד דיאטה וסטרס מעצבים סינפסות מחדש ברשתות היפותלמיות, מוחיות ותגמולים וכיצד 'לחדור מחדש' מעגלים לא מסתגלים בבטחה. מענה על שאלות אלה ישכלול טיפול ספציפי לחולים (בחירת עמוד השדרה של אינגדין, תוספות קולטנים של אמילין), תפחית את הפסקת ההפסקה והרחיב יתרונות קרדיומטבוליים למשפחות ומערכות בריאות עבור חולים רבים.
מסקנות
לסיכום, המוח הוא מרכז הפיקוד של הומאוסטזיס אנרגיה. על ידי שילוב אותות אנדוקריניים מרקמת שומן, דרכי העיכול, הלבלב והכבד עם קלט עצבי מהיר, מעגלים מרכזיים, ממסלולי קשת מלנוקורטין ועד רשתות DVC ומזוקורטיקולימבי, קבעו תערוכה, הוצאות ותגמול.
תרופות פפטיד המכוונות למסלולי GLP-1R, GIPR ו- Amylin כבר מספקים ירידה משמעותית במשקל. הצלחה עתידית תהיה תלויה במיפוי נוירופלסטיות תלויה בפעילות ובעיצוב שילובים שממקסמים את השובע, ממזער את הסלידה ומגן על בריאות הקרדיומבולית לטווח הארוך לאנשים בכל מקום.