למרות עשרות שנות מחקר, עד כה התעלמו במידה רבה מהשפעתו של כרומוזום ה-X על אלצהיימר. גלה כיצד שבעה לוקוסים גנטיים שהתגלו לאחרונה יכולים לחולל מהפכה בהבנתנו את המחלה.
מחקר: מחקר קשר רחב כרומוזום X למחלת אלצהיימר. קרדיט תמונה: nobeastsofierce / Shutterstock
חקירות קונבנציונליות של התורמים הגנטיים לסיכון והתקדמות מחלת אלצהיימר (AD) התעלמו מתפקידו של כרומוזום X, בעיקר בשל מגבלות ניתוח טכני. כדי להתמודד עם פערי הידע הללו, מחקר שפורסם לאחרונה בכתב העת פסיכיאטריה מולקולרית מינפה נתונים נרחבים של מחקר X-Chromosome-Wide Association (XWAS) מ-115,841 מקרי AD (כולל מקרים קליניים מאובחנים ומקרי פרוקסי) ו-613,671 בקרות לזיהוי אותות גנטיים המעידים על פתופיזיולוגיה של AD.
המחקר בחן שלושה דפוסים של השבתת כרומוזום X (XCI) בנשים (r-XCI, s-XCI ו-e-XCI) ולא מצא אותות גנום רחב הקשורים ל-AD באזורים הלא פסאודואוטוזומליים של כרומוזום X . יש לציין כי המחקר זיהה שבעה לוקוסים בעלי ספי מובהקות רחבי כרומוזום X אשר עשויים לתרום לגנים הקשורים ל-AD (למשל, FRMPD4, DMD ו-WNK3), אשר הודגשו כיעדים חיוניים למחקר עתידי.
רֶקַע
מחלת אלצהיימר (AD) היא הפרעה נוירודגנרטיבית הקשורה לגיל המאופיינת בזיכרון מתקדם וירידה קוגניטיבית. זה נותר המבשר השכיח ביותר לדמנציה מבוגרים, ללא תרופה מזוהה עד כה. עשרות שנים של מחקר הדגישו כמה (>80) תורמים גנטיים (לוקים) לסיכון ל-AD. למרבה הצער, מגבלות טכניות מסורתיות הביאו לכך שכרומוזום ה-X נשלל בעיקר מחקירות אלו.
כרומוזום X מהווה 5% מהגנום, כאשר מחקרים קודמים הראו שהוא מכיל עד 15% מהגנים התורמים למוגבלות אינטלקטואלית גנטית. דימורפיזם מיני משמעותי (הבדלים בין גברים לנקבה) הן בתכונות של כרומוזום X (לנשים יש שני כרומוזומי X, בעוד שלגברים יש רק אחד) והן בתוצאות AD (נשים נמצאות בסיכון גבוה יותר ל-AD וחיות זמן רב יותר עם AD בהשוואה לעמיתיהם הגברים, בעוד גברים מפגינים ירידה קוגניטיבית מהירה יותר הקשורה ל-AD) מחייבת הבנה משופרת של תפקידו של כרומוזום X בסיכון והתקדמות AD.
על המחקר
המחקר הנוכחי נועד לטפל בפערים בהבנתנו את תפקידו של כרומוזום ה-X בסיכון והתקדמות AD על ידי שימוש במחקר X-Chromosome-Wide Association מעמיק (XWAS). מערך הנתונים של המחקר נגזר מ-35 מחקרים קודמים, שתי קבוצות משפחתיות עצמאיות ושני ביו-בנקים (UK Biobank (UKB) ו-FinnGen. הוא כלל 115,841 מקרי AD (52,214 מקרים קליניים מאובחנים ו-55,868 מקרי פרוקסי), פרוקסי AD (מוגדרים כ'שני ההורים מדגימים דמנציה' אצל נשים ו'אמהות המדגימות דמנציה' אצל גברים), ו-613,671 מקרי ביקורת (55% נשים), כולם מהם ממוצא אירופי.
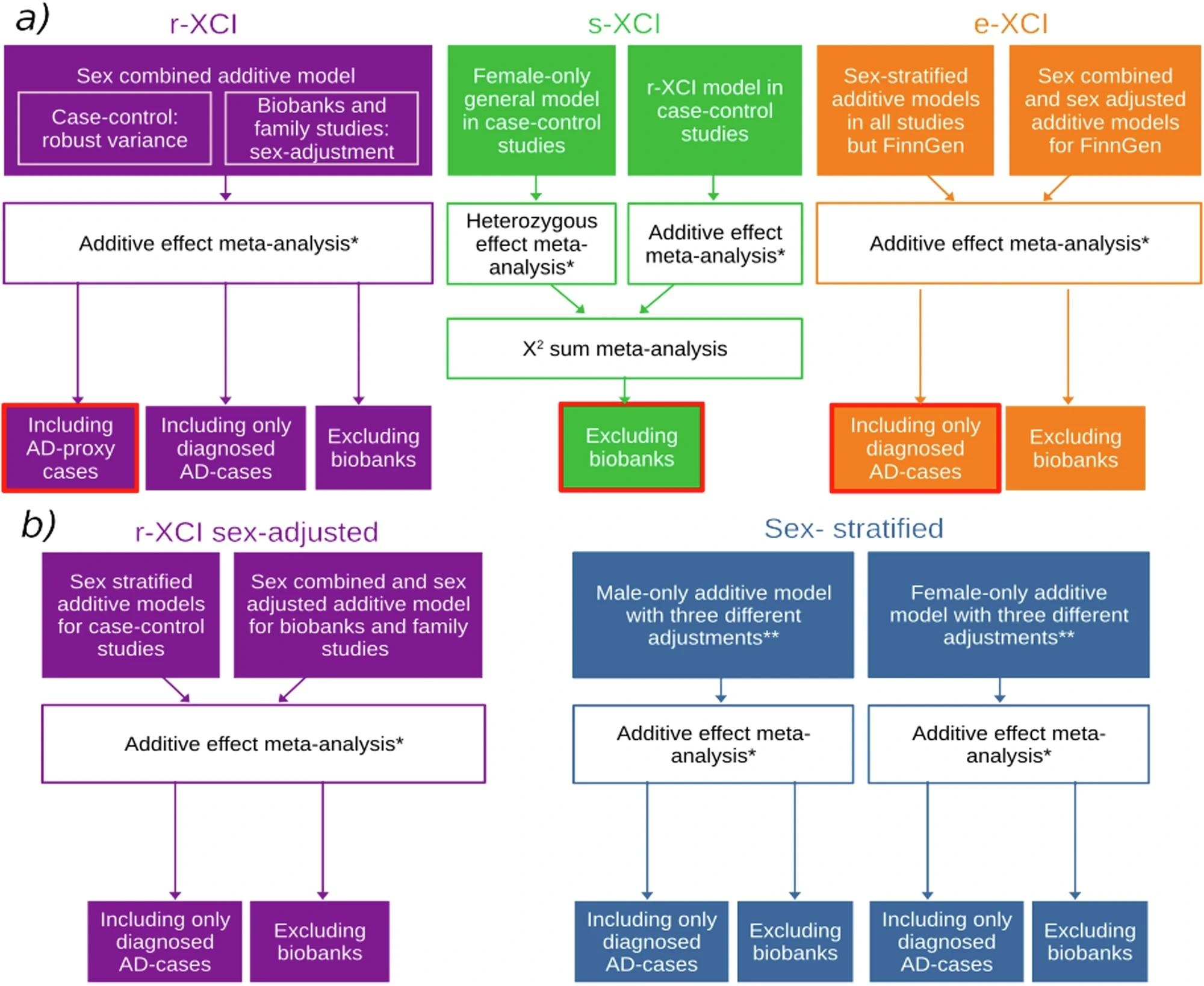 א ניתוחים עיקריים ו ב ניתוחי רגישות. צבעי הקופסה מציינים את הגישה: סגול, ירוק, כתום וכחול מייצגים גישות r-XCI, s-XCI, e-XCI וגישות מרובדות מין, בהתאמה. תיבות בעיגול באדום הן הניתוחים העיקריים של r-XCI, s-XCI ו-e-XCI. * מטא-אנליזה של אפקט קבוע עם גישה משוקללת השונות הפוכה כפי שהוטמעה ב- METAL. **מודלים מרובדי מין הותאמו על 1) רכיבים עיקריים (PC) ו/או מרכז הגנוטיפים; 2) מחשבים אישיים, מרכז וגיל; 3) מחשבים אישיים, מרכז, גיל ו-APOE.
א ניתוחים עיקריים ו ב ניתוחי רגישות. צבעי הקופסה מציינים את הגישה: סגול, ירוק, כתום וכחול מייצגים גישות r-XCI, s-XCI, e-XCI וגישות מרובדות מין, בהתאמה. תיבות בעיגול באדום הן הניתוחים העיקריים של r-XCI, s-XCI ו-e-XCI. * מטא-אנליזה של אפקט קבוע עם גישה משוקללת השונות הפוכה כפי שהוטמעה ב- METAL. **מודלים מרובדי מין הותאמו על 1) רכיבים עיקריים (PC) ו/או מרכז הגנוטיפים; 2) מחשבים אישיים, מרכז וגיל; 3) מחשבים אישיים, מרכז, גיל ו-APOE.
לאחר ניתוחי רגישות, 63,838 מקרים מאובחנים של AD ו-806,335 ביקורת נכללו עבור ניתוחים במורד הזרם. המחקר שילב עוד ניתוחי סמנים ביולוגיים של נוזל מוחי (Aβ42 ו-pTau) והערכות ליקויים קוגניטיביים (Mini-Mental State Examination (MMSE)) בתת-קבוצה של משתתפים (5,522 ו-2,661, בהתאמה). יש לציין כי המחקר הוציא מהניתוחים אזורים פסאודואוטוזומליים, בעיקר בשל הדרתם משבבי הגנוטיפים של רוב המשתתפים.
חישוב אנליטי כלל בדיקות אסוציאציות שבוצעו תחת שלושה משטרי אי-אקטיבציה של כרומוזום X (XCI) המתייחסים למצבי XCI שונים של נשים – 1. XCI אקראי (r-XCI), 2. XCI מוטה (s-XCI) ו-3. Escape XCI ( e-XCI). החוקרים ערכו בנוסף ניתוחים מרובדים למין כדי להסביר את השונות הנגרמת על ידי מנגנוני XCI, מה שעלול לגרום להשפעה חזקה מהצפוי אצל גברים. אמצעי בקרת איכות מחמירים וניתוחי רגישות יושמו כדי להבטיח מהימנות נתונים גבוהה וכדי לצמצם שלילי שווא פוטנציאליים הנובעים מהבדלים מתודולוגיים ספציפיים לביו-בנק.
"כדי לשמור על איזון סביב מינון אללים בין המינים, השבתת כרומוזום X (XCI) מתרחשת אצל נקבות. תהליך זה הוא המקום שבו כרומוזום X אחד מושתק בתעתוק במהלך התפתחות האישה. הבחירה בעותק המושתק היא לרוב אקראית (XCI אקראית או r-XCI), אך ביטול ההפעלה יכול להיות מוטה גם לכיוון עותק ספציפי (מוטות XCI או s-XCI חשוב, עד). שליש מהגנים של כרומוזום ה-X 'בורחים' מאינאקטיבציה ומתבטאים משני כרומוזומי ה-X בתאים נשיים (בריחה XCI או e-XCI).
לבסוף, חישובי קולקליזציה גנטית שהשוו את תוצאות המחקר (לוקוסים גנטיים מזוהים) עם נקודות נתונים קיימות של תכונות חלבון וביטוי כמותיות (pQTL ו-eQTL, בהתאמה) כדי לזהות תכונות וסמנים ביולוגיים המייצגים ירידה קוגניטיבית.
ממצאי מחקר
ניתוחי ה-XWAS שנערכו בזאת זיהו 666,264 r-XCI, 442,001 e-XCI ו-438,420 וריאנטים s-XCI, מתוכם 288,320, 276,902 ו-263,169, בהתאמה, היו שכיחות ≥ 1% (מינורי %). יש לציין, שאף אחת מהגישות שהופעלו לא זיהתה אותות משמעותיים בכל הגנום, מה שמצביע על כך שהאזורים הלא פסאודואוטוזומליים של כרומוזום ה-X נטולי גורמי סיכון גנטיים נפוצים הקשורים ל-AD.
זוהו שבעה לוקוסים עם ספי מובהקות לכל כרומוזום X, כולל ארבעה לוקוסים נפוצים (Xp22.32, FRMPD4, DMD ו-Xq25) ושלושה לוקוסים נדירים (WNK3, PJA1 ו-DACH2). לוקוסים אלה מודגשים כיעדים לחקירה עתידית ועשויים להחזיק את המפתח לגילוי התערבויות קליניות, טיפוליות ותרופתיות נגד תחילתה והתקדמות של AD.
FRMPD4, גן המובע במוח המקושר לרזרבה קוגניטיבית, הראה אותות חזקים במיוחד. לעומת זאת, גרסאות נדירות יותר כמו אלה ב-PJA1 ו-DACH2 הדגימו איכות נתונים ירודה (למשל, כיסוי גרסאות דליל ואיכות זקיפה נמוכה יותר), המדגישים את הצורך באופטימיזציות מתודולוגיות במחקר עתידי.
מסקנות
המחקר הנוכחי מייצג את ה-XWAS הגדול ביותר על AD עד כה, מנתח נתונים מלמעלה מ-115,000 מקרים ו-613,000 בקרות. הוא מציג את הניסיון הראשון להתייחס למורכבות של כרומוזומי X, כגון שונות בדפוסי XCI נשיים והמגבלות של שיטות ספציפיות לביובנק. למרות שלא נמצאו קשרים משמעותיים בכל הגנום, זוהו שבעה לוקוסים מרמזים, כולל FRMPD4, DMD ו-WNK3. במקביל לביטוי גנים וחקירות אפיגנטיות, מחקר זה עשוי להוות בסיס להתערבויות קליניות עתידיות נגד סיכון והתקדמות AD.