במחקר שפורסם לאחרונה ב- כתב עת לרפואה ניסיוניתחוקרים זיהו את הטרופיזם הסלולרי וההשלכות התעתיקים של תסמונת נשימה חריפה חמורה נגיף קורונה 2 (SARS-CoV-2) על ידי הדבקה של רקמת ריאה אנושית ושימוש ברצף חומצה ריבונוקלאית חד-תאית (scRNA-seq) כדי לבנות מחדש את תוכנית התמלול ב"פסאודו-זמן זיהום" "עבור סוגי תאי ריאה שונים.
זיהומים בדרכי הנשימה התחתונות, כמו מחלת נגיף הקורונה 2019 (COVID-19), הם גורם מוות מוביל ברחבי העולם, ומייצרים דלקת ריאות ותסמונת מצוקה נשימתית חריפה. קשה להבין את השלבים המוקדמים שלהם. חוקרים השתמשו בגישות היסטופתולוגיות קלאסיות ובפרופיל רב-אומי חד-תאי כדי להסיק שלבים מוקדמים בפתוגנזה של בני אדם משטיפה של ריאות, ביופסיה או חומרי נתיחה. גישות אלו חושפות תמונה יסודית של דלקת ריאות COVID-19 ברזולוציה תאית ומולקולרית שאין שני לה, מה שמרמז על מודלים של זיהום כולל אפיתל מכתשית, נימים, מקרופאגים ותאי מיאלואיד.
מחקר: מקרופאגים אינטרסטיציאליים הם מוקד של השתלטות ודלקת ויראלית בהתחלת COVID-19 בריאות אנושית. קרדיט תמונה: Dotted Yeti / Shutterstock
לגבי המחקר
במחקר הנוכחי, החוקרים פיתחו מודל ניסיוני של COVID-19 לחקור תהליכים מולקולריים מוקדמים ומנגנונים פתוגניים של זיהום SARS-CoV-2 ברמה התאית ברקמות מקוריות של הריאה האנושית.
החוקרים ביססו את הטרופיזם הסלולרי של SARS-CoV-2 ואת ההשפעות הייחודיות והדינמיות שלו על ביטוי הגנים התאיים המארח בסוגים ספציפיים של תאי ריאה. היעדים הבולטים היו מקרופאגים תושבי ריאות, מתוכם SARS-CoV-2 אחד משתלט על תעתיקים, מה שגורם לתוכנית אנטי-ויראלית מארח ממוקד (IFN), וכמה כימוקינים, פרו-פיברוטים ופרו-דלקתיים וציטוקינים המאותתים למגוון מבניים ואימונולוגיים. תאים של הריאה.
כדי לקבוע את השלבים המוקדמים של COVID-19 בריאות אנושית, החוקרים חתכו רקמת ריאה שהתקבלה מדגימות ניתוחיות או מיחידי תורמי איברים לקטעים עבים והשתמשו בהם לניתוח תרבית רקמה. לאחר מכן, הם חשפו את הרקמות לזן SARS-CoV-2 USA-WA1 2020 בריבוי זיהום של 1.0 (MOI) למשך שעתיים לפני שאפשרו לזיהום SARS-CoV-2 להימשך יומיים עד שלושה. הם ביצעו בדיקת פלאק על סופרנטנטים של תרבית.
החוקרים הפרידו את הפרוסות ובחנו אותן על ידי scRNA-seq כדי להעריך את הביטוי הגנטי של המארח והנגיף במהלך הזיהום ב-SARS-CoV-2. הם גם בחנו את המבנה והעיבוד של מולקולות ה-RNA הנגיפיות על ידי ניתוח מערך הנתונים של scRNA-seq עם המסגרת של SICILIAN. הם השתמשו בסמני אטלס מולקולריים כדי להבחין בין סוגי תאי ריאה בפרוסות ריאות בריאות ולמדוד רמות RNA ויראלי בתאים נגועים.
הצוות ביצע פלואורסצנציה מרובבת מולקולה בודדת באתר הכלאה (smFISH) כדי לאשר את ממצאי הטרופיזם של תאי הריאה ולהראות תאים נגועים. הם השתמשו בדפוסי ביטוי של גנים חד-תאיים כדי לזהות יעדים תאיים לאותות דלקתיים ופרו-פיברוטיים שנוצרו על ידי זיהום SARS-CoV-2 של a-IMs. הם המציאו טכניקה לטיהור אוכלוסיות מקרופאגים מריאות אנושיות עם ספייק של SARS-CoV-2 (S) לנטיוירוס פסאודוטיפוס חלבון (lenti-S-NLuc-tdT) כדי לחקור את דרכי הכניסה של מקרופאגים ריאות.
החוקרים הדביקו באופן פרודוקטיבי פרוסות ריאות אנושיות שטופחו ex vivo עם SARS-CoV-2, כשהייצור עלה בין 24 ל-72 שעות של תרבית. הם הפעילו חום, טופלו באולטרה סגול (UV), או ניתנו 10.0 מיקרומטר remdesivir, מעכב RNA פולימראז תלוי ב-RNA המשמש כתרופה לטיפול ב-COVID-19, כדי למנוע זיהום במאגר ויראלי.
תוצאות
הניתוח הראה כי SARS-CoV-2 מדביק באופן מועדף מקרופאגים אינטרסטיציאליים פעילים (IMs), שיכולים לצבור מאות מולקולות SARS-CoV-2 RNA, המהוות יותר מ-60% מתעתיק התא ומייצרות גופי RNA ויראלי צפופים. מקרופאגים מכתשיים נגועים (AMs) אינם מציגים תגובות חמורות, עם כניסה ויראלית תלוית חלבון (S) ל-AMs תוך שימוש באנזים 2 (ACE2) הממיר אנגיוטנסין ובאשכול ההתמיינות 169 (CD169) וכניסת IM דרך CD209.
הם מצאו צמתים תת-גנומיים קנוניים בין הרצף יוצא הדופן שקורא מעבר ל-39 האזורים הסופיים שלהם, מה שמצביע על ייצור RNA שליח SARS-CoV-2 (mRNA) מסוג קנוני בתרביות הריאות. הם גם מצאו מאות צמתים תת-גנומיים חדשים, המראים מגוון רחב של RNAs SARS-CoV-2 תת-גנומיים שאינם קנוניים וקנוניים המיוצרים במהלך זיהום ריאתי.
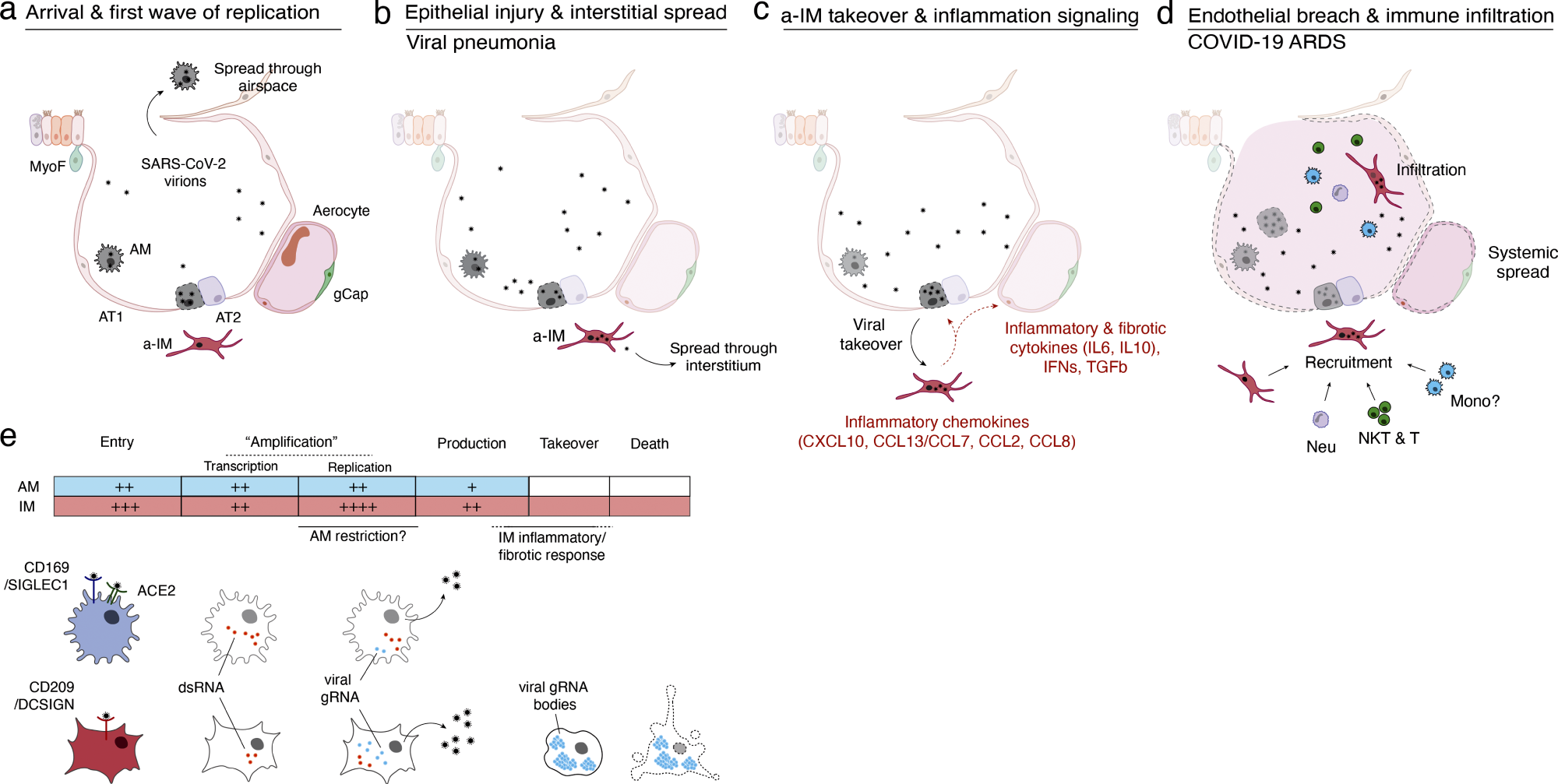 מודל של התחלה, מעבר ופתוגנזה של COVID-19 ומחזור החיים הנגיפי ב-AMs ו-IMs. (מוֹדָעָה) מודל של התחלת COVID-19 בריאות האדם ומעבר מדלקת ריאות ויראלית ל-COVID-19 ARDS קטלני. (א) הפצת ויריון של SARS-CoV-2 והגעה לאלבוליות. לומינלי AM נתקלים בווירונים שנשפכים מדרכי הנשימה העליונות הנכנסים לריאה. AMs יכולים לבטא מספרים נמוכים עד בינוניים של מולקולות RNA ויראלי ויכולים להפיץ את הזיהום אך "להכיל" את ה-RNA הנגיפי מהשתלטות על כל התעתיק ולהראות רק תגובה דלקתית של התא המארח מוגבל מאוד לזיהום ויראלי. (ב) שכפול ופגיעה באפיתל. נגיפים של SARS-CoV-2 נכנסים לתאי AT2 דרך ACE2, הקולטן הקנוני שלו, ו"משכפלים" לרמות גבוהות של RNA נגיפי, מייצרים נגיפים מדבקים ומתחילים דלקת ריאות ויראלית. (ג) השתלטות a-IM ואיתת דלקת. Virions SARS-CoV-2 מתפשטים לחלל הבין-סטיציאלי באמצעות שחרור טרנס-אפיתליאלי של ויריון על ידי תאי AT2 או פגיעה במחסום האפיתל, ונכנסים ל-a-IMs. a-IMs נגועים יכולים לבטא רמות גבוהות מאוד של RNA ויראלי ששולטים ("משתלטים") על התעתיק המארח ויכולים להפיץ את הזיהום. השתלטות ויראלית מעוררת אינדוקציה של הכימוקינים והציטוקינים המוצגים, ויוצרים מוקד לאיתות דלקתי ופיברוטי. (ד) פריצת אנדותל וחדירה חיסונית. הציטוקין הדלקתי a-IM IL6 מכוון לתאים מבניים של המכתשית הגורמים לפירוק אפיתל ואנדותל, והציטוקינים הדלקתיים מגייסים את תאי החיסון המצוינים מהאינטרסטיטיום או ממחזור הדם, אשר מציפים וחודרים למכתשית וגורמים ל-COVID-19 ARDS. מולקולות דלקתיות מקומיות מוגברות על ידי תאי חיסון במחזור, ובאופן הדדי עלולות להתפשט בזרם הדם כדי לגרום לתסמינים מערכתיים של סערת ציטוקינים. (ה) השוואה בין מחזור החיים הנגיפי של SARS-CoV-2 ב-AMs ו-IM. למרות ששניהם יכולים לייצר נגיפים מדבקים, שים לב להבדלים בקולטני כניסה ויראליים (AMs יכולים להשתמש ב-ACE2 וב-CD169/SIGLEC1, בעוד ש-IMs משתמשים ב-CD209); שעתוק RNA ויראלי של תוצרי ביניים dsRNA (גדול יותר ב-AMs); שכפול של RNA גנומי באורך מלא (גדול יותר ב-IMs); השתלטות ויראלית, יצירת גופי RNA והשראת תגובה דלקתית חזקה של תא מארח (רק ב-IMs), והרס/מוות של תאים (רק ב-IMs).
מודל של התחלה, מעבר ופתוגנזה של COVID-19 ומחזור החיים הנגיפי ב-AMs ו-IMs. (מוֹדָעָה) מודל של התחלת COVID-19 בריאות האדם ומעבר מדלקת ריאות ויראלית ל-COVID-19 ARDS קטלני. (א) הפצת ויריון של SARS-CoV-2 והגעה לאלבוליות. לומינלי AM נתקלים בווירונים שנשפכים מדרכי הנשימה העליונות הנכנסים לריאה. AMs יכולים לבטא מספרים נמוכים עד בינוניים של מולקולות RNA ויראלי ויכולים להפיץ את הזיהום אך "להכיל" את ה-RNA הנגיפי מהשתלטות על כל התעתיק ולהראות רק תגובה דלקתית של התא המארח מוגבל מאוד לזיהום ויראלי. (ב) שכפול ופגיעה באפיתל. נגיפים של SARS-CoV-2 נכנסים לתאי AT2 דרך ACE2, הקולטן הקנוני שלו, ו"משכפלים" לרמות גבוהות של RNA נגיפי, מייצרים נגיפים מדבקים ומתחילים דלקת ריאות ויראלית. (ג) השתלטות a-IM ואיתת דלקת. Virions SARS-CoV-2 מתפשטים לחלל הבין-סטיציאלי באמצעות שחרור טרנס-אפיתליאלי של ויריון על ידי תאי AT2 או פגיעה במחסום האפיתל, ונכנסים ל-a-IMs. a-IMs נגועים יכולים לבטא רמות גבוהות מאוד של RNA ויראלי ששולטים ("משתלטים") על התעתיק המארח ויכולים להפיץ את הזיהום. השתלטות ויראלית מעוררת אינדוקציה של הכימוקינים והציטוקינים המוצגים, ויוצרים מוקד לאיתות דלקתי ופיברוטי. (ד) פריצת אנדותל וחדירה חיסונית. הציטוקין הדלקתי a-IM IL6 מכוון לתאים מבניים של המכתשית הגורמים לפירוק אפיתל ואנדותל, והציטוקינים הדלקתיים מגייסים את תאי החיסון המצוינים מהאינטרסטיטיום או ממחזור הדם, אשר מציפים וחודרים למכתשית וגורמים ל-COVID-19 ARDS. מולקולות דלקתיות מקומיות מוגברות על ידי תאי חיסון במחזור, ובאופן הדדי עלולות להתפשט בזרם הדם כדי לגרום לתסמינים מערכתיים של סערת ציטוקינים. (ה) השוואה בין מחזור החיים הנגיפי של SARS-CoV-2 ב-AMs ו-IM. למרות ששניהם יכולים לייצר נגיפים מדבקים, שים לב להבדלים בקולטני כניסה ויראליים (AMs יכולים להשתמש ב-ACE2 וב-CD169/SIGLEC1, בעוד ש-IMs משתמשים ב-CD209); שעתוק RNA ויראלי של תוצרי ביניים dsRNA (גדול יותר ב-AMs); שכפול של RNA גנומי באורך מלא (גדול יותר ב-IMs); השתלטות ויראלית, יצירת גופי RNA והשראת תגובה דלקתית חזקה של תא מארח (רק ב-IMs), והרס/מוות של תאים (רק ב-IMs).
חום, השבתת UV-C או טיפול ב-remdesivir מנעו התפתחות של קשרים קנוניים ולא קנוניים. הצוות צפה בהשתלטות של SARS-CoV-2 על תת-סוג IM משופעל ב-176,382 תאים עם תעתיקים איכותיים שהתקבלו מפרוסות ריאות נגועות של ארבע ריאות תורמות וב-112,359 תאים מפרוסות נגועות מדומה (תורבתו ללא תוספת ויראלית) ו-95,389 בקרה לא-תרבותית. תאים (ישירות מפרוסות ריאה טריות חתוכות). מחקר ביטוי גנים דיפרנציאלי של a-IMs על פני פסאודו-זמן זיהום חשף שינויים בביטוי הגנים המארח התואמים לרמות SARS-CoV-2 RNA.
המחקר מצא כי זיהום והשתלטות של דלקת ריאות COVID-19 גורמים לתגובה מוקדמת של תאים אנטי-ויראליים ספציפית למקרופאגים אינטרסטיציאליים מופעלים, וכתוצאה מכך מרכז איתות אימונולוגי ופיברוטי רב עוצמה. הפעלה של דלקת דלקת אינה שכיחה וניתנת לזיהוי רק מאוחר בזיהום A-IM. חסימת נוגדנים נגד CD169 ו-CD209 מנעה כניסה ל-IMs ו-AMs. המחקר גם הדגיש IMs כיעד הריאות הפגיע ביותר, עם דגש ראשוני על דלקת ופיברוזיס. שתי שושלות מולקולריות ייחודיות של מטרות מקרופאגים מגיבות באופן שונה ל-SARS-CoV-2, ומשפיעות על האטיולוגיה והטיפולים.