במאמר שפורסם לאחרונה ב העברת אותות וטיפול ממוקד, חוקרים מציגים ידע מדעי שנאסף עד כה על הרעיון של מיקרוביוטה תוך-גידולית.
החוקרים סקרו בדיעבד את כל אבני הדרך ההיסטוריות בזירת הטיפול נגד סרטן המבוסס על חיידקים. בנוסף, הם סיכמו את המאפיינים של חיידקים תוך-גידוליים בגידולים שונים והשפעותיהם על התפתחות סרטן וחסינות אנטי-גידולית.
הם גם דנו ביישומים פרוספקטיביים של מיקרוביוטה תוך-גידולית בפרוגנוזה ובטיפול בסרטן.
מיקרוביוטה תוך-גידולית בסרטן: מקור, מאפיינים ותפקוד
לפני המאה ה-19, רקמות הגידול נחשבו סטריליות. בשנת 1885 גילה דויין, מיקרוביולוג, מיקרואורגניזמים בגידולים, מה שהוליד את הרעיון של מיקרוביוטה תוך-גידולית.
במשך הזמן, חוקרים זיהו דרכי פלישה שונות של חיידקים בגידולים, מתוכם ארבעה מרכזיים הם הרס רירית, נדידת רקמות סמוכות ופלישה המטוגנית. ברגע שהם פולשים למיקרו-סביבה של הגידול (TME), חיידקים אלה משפיעים על ההתנהגות הביולוגית של גידולים.
המיקרוביוטה התוך-גידולית מגוונת מאוד; בהתאם, הם משתנים באופן מהותי בין סוגי סרטן, תת-סוגים ושלבים שונים.
לדוגמה, Modestobacter ו Blastomyces נמצאים בשפע יותר בגידולי ריאה מאשר ברקמות סמוכות, בעוד Propionibacterium ו Enterobacteriaceae הם נמוך יותר. יתרה מכך, המיקרוביוטה של קרצינומה של תאי קשקש ריאה מגוונת הרבה יותר מזו של אדנוקרצינומה של הריאות.
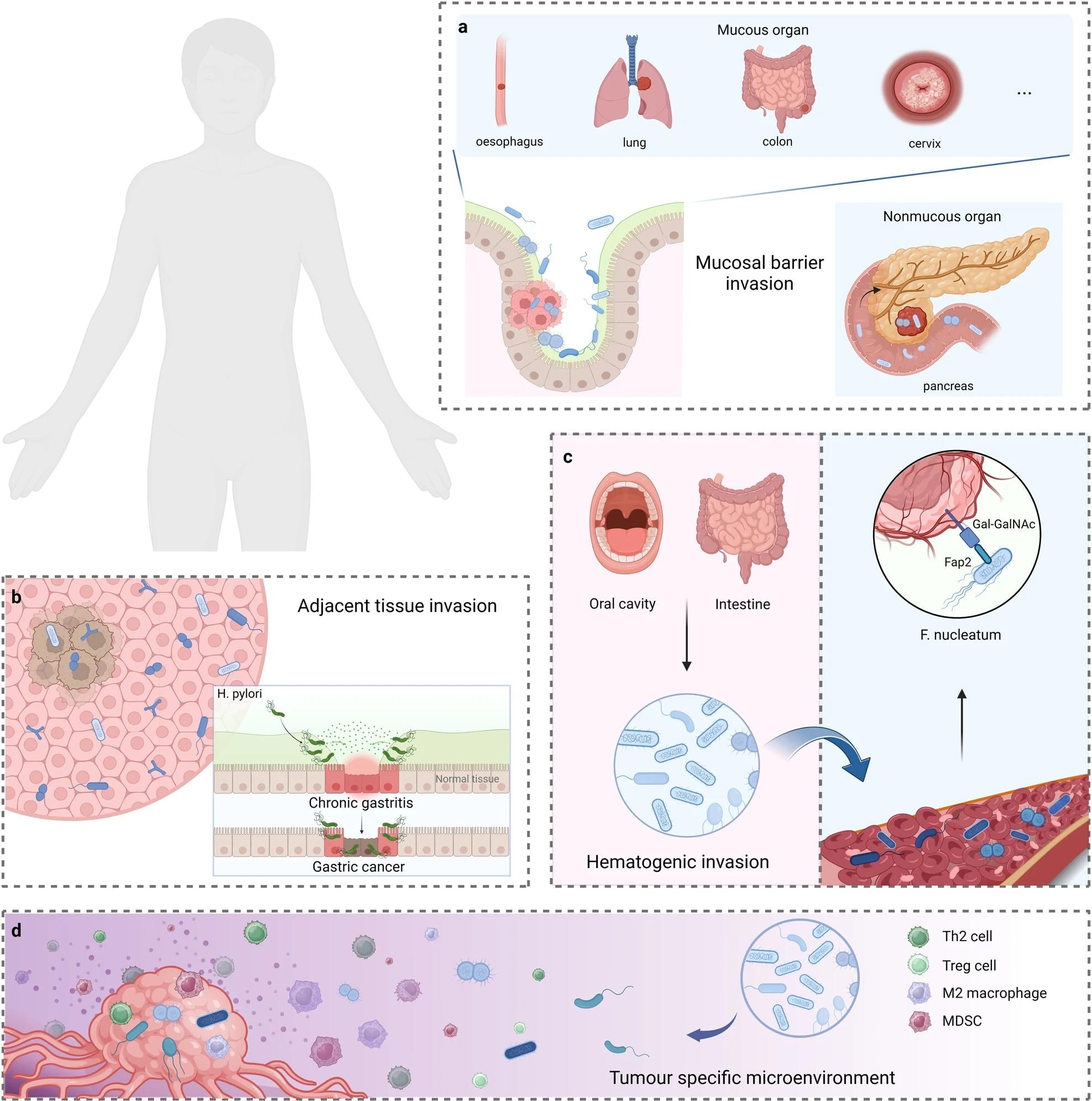 המקורות הפוטנציאליים של מיקרוביוטה תוך-גידולית. פלישת מחסום רירית. מיקרואורגניזמים עלולים לפלוש לגידול דרך הרירית הפגועה. ב פלישת רקמות סמוכות. קהילת המיקרוביום בין הגידול לרקמה נורמלית סמוכה חולקת קווי דמיון רבים. ג פלישה המטוגנית. מיקרואורגניזמים מחלל הפה, המעי וממקומות פוטנציאליים אחרים עשויים להינשא אל מיקומי הגידול ולהתנחל בגידול דרך כלי דם שנהרסים. ד משיכה של מיקרו-סביבה ספציפית לגידול. סביבות מדכאות חיסוניות, היפוקסיות ומטבוליות מועשרות בחומרים מזינים בגידולים עשויות לשפר את הקולוניזציה של חיידקים. נוצר עם BioRender.com
המקורות הפוטנציאליים של מיקרוביוטה תוך-גידולית. פלישת מחסום רירית. מיקרואורגניזמים עלולים לפלוש לגידול דרך הרירית הפגועה. ב פלישת רקמות סמוכות. קהילת המיקרוביום בין הגידול לרקמה נורמלית סמוכה חולקת קווי דמיון רבים. ג פלישה המטוגנית. מיקרואורגניזמים מחלל הפה, המעי וממקומות פוטנציאליים אחרים עשויים להינשא אל מיקומי הגידול ולהתנחל בגידול דרך כלי דם שנהרסים. ד משיכה של מיקרו-סביבה ספציפית לגידול. סביבות מדכאות חיסוניות, היפוקסיות ומטבוליות מועשרות בחומרים מזינים בגידולים עשויות לשפר את הקולוניזציה של חיידקים. נוצר עם BioRender.com
מחקר קודם חשף גם את מגוון המיקרוביוטות בסרטן הכבד, המעי הגס, המעי הגס, הקיבה, השד, הלבלב, הפה, הראש והצוואר, האף-לוע וכמה סוגי סרטן רבייה. עם זאת, הנתונים על הקשר בין מיקרוביוטה תוך-גידולית וסוגים אחרים של סרטן נותרו נדירים, מה שמצדיק מחקר נוסף.
מחקרים מכאניסטיים הוכיחו כי חיידקים תושבי גידול מאמצים שישה מנגנונים עיקריים להשפיע על התחלתה והתקדמות של סרטן. אלו הם חוסר יציבות ומוטציה בגנום, שינויים אפיגנטיים, דלקת ממושכת, הימנעות מהתחמקות חיסונית, הפרעה בחילוף החומרים והפעלת גרורות ופלישה.
וירוס T-lymphotropic human type 1 (HTLV-1) מעכב את מסלול תיקון ה-DNA דרך חלבון HTLV-1 Tax, מה שמוביל לאי יציבות הגנום. באופן דומה, גורמי ארסיות חיידקים (VirFs) גורמים ישירות לסרטן. רקמות סרטן השד מכילות אנזים מסרטן, β-glucuronidase.
שינויים אפיגנטיים כגון מתילציה חריגה של DNA הם המסלול העיקרי עבור הליקובקטר פילורי זיהום כדי לגרום לאדנוקרצינומה בקיבה. מחקרים רבים הראו כיצד וירוסים וחיידקים תוך-גידוליים מווסתים באופן ישיר או עקיף שינויים אפיגנטיים של המארח; עם זאת, מחקרים צריכים לחקור את המנגנונים הבסיסיים שלהם.
דלקת גם הופכת מיקרו-סביבה מדכאת חיסון כדי לקדם את התקדמות הגידול. יתר על כן, תאים דלקתיים באתרים של זיהום מיקרוביאלי מייצרים מיני חמצן תגובתיים (ROS) כדי לגרום נזק ל-DNA, ובכך תורמים להתפתחות סרטן.
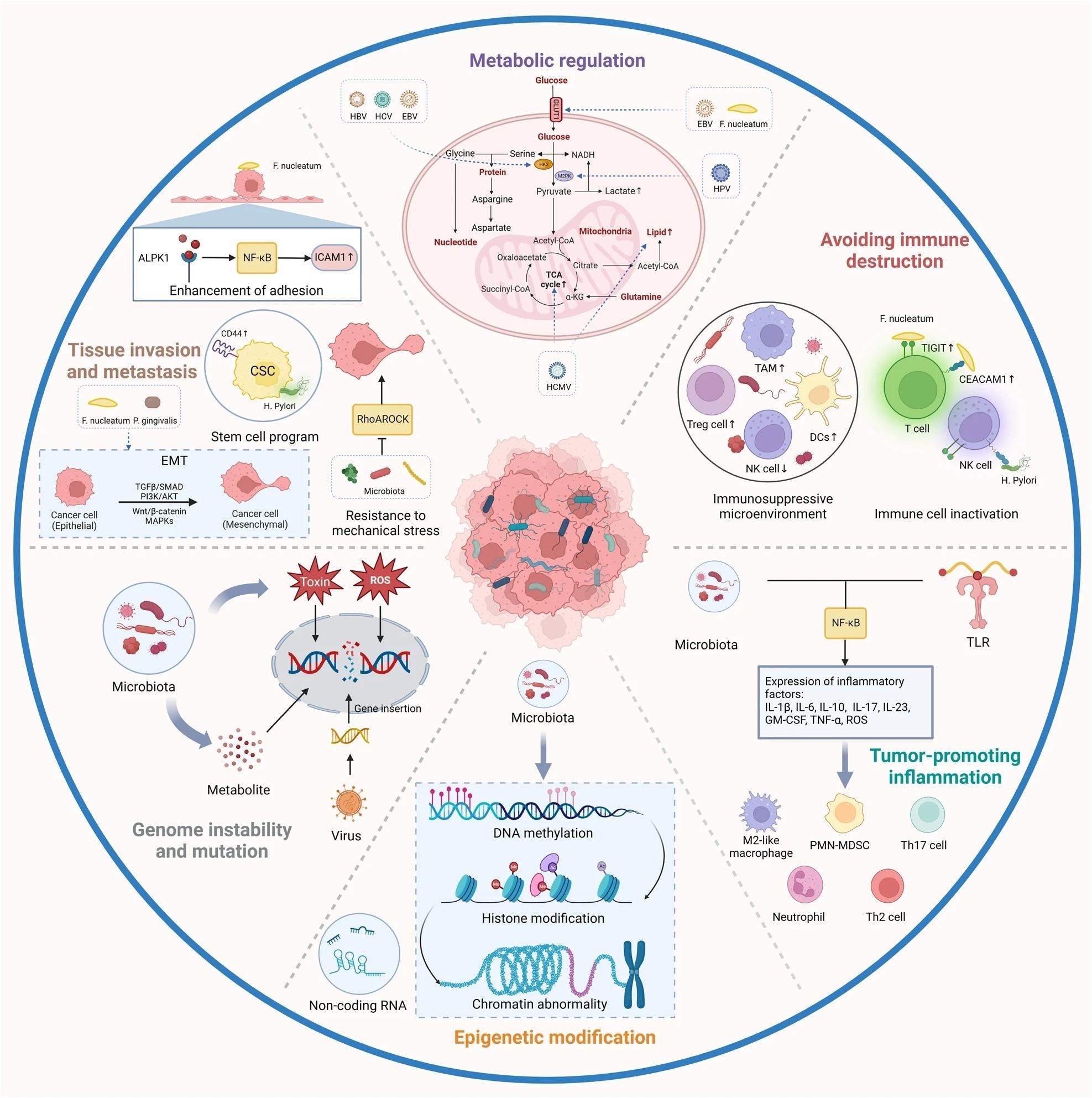 תפקידה של מיקרוביוטה תוך-גידולית בהתפתחות סרטן. ההשפעות הפוטנציאליות של המיקרוביום על הסרטן נותרו חמקמקות. שישה מנגנונים עיקריים הוצעו כדי להסביר כיצד המיקרוביוטה התוך-גידולית משפיעה על התחלת הסרטן והתקדמותו, כולל חוסר יציבות ומוטציה של הגנום, שינוי אפיגנטי, דלקת כרונית, התחמקות חיסונית, ויסות מטבולי, הפעלת פלישה וגרורות. TAM, מקרופאג הקשור לגידול; HK2, הקסוקינאז 2; TCA, חומצה טריקרבוקסילית. נוצר עם BioRender.com
תפקידה של מיקרוביוטה תוך-גידולית בהתפתחות סרטן. ההשפעות הפוטנציאליות של המיקרוביום על הסרטן נותרו חמקמקות. שישה מנגנונים עיקריים הוצעו כדי להסביר כיצד המיקרוביוטה התוך-גידולית משפיעה על התחלת הסרטן והתקדמותו, כולל חוסר יציבות ומוטציה של הגנום, שינוי אפיגנטי, דלקת כרונית, התחמקות חיסונית, ויסות מטבולי, הפעלת פלישה וגרורות. TAM, מקרופאג הקשור לגידול; HK2, הקסוקינאז 2; TCA, חומצה טריקרבוקסילית. נוצר עם BioRender.com
מיקרוביוטה תוך-גידולית מתחמקת גם מתגובות חיסוניות; לדוגמה, HPV מעכב את ההפעלה של תאי T ציטוטוקסי (NK) כדי לקדם ממאירות בתאי סרטן צוואר הרחם האנושיים.
באופן דומה, הם מקלים על גרורות, כפי שמוצג במודל עכבר של סרטן המעי הגס (CRC), כאשר הגידול נמצא אי קולי שיבשו את מחסום כלי הדם במעיים כדי לקדם את הגיוס של תאים גרורתיים והתפשטות של חיידקים לאחר מכן לכבד.
עם זאת, עד כה, הבנה עמוקה של ההשפעות הפוטנציאליות של כל המסלולים הללו על הסרטן נותרה חמקמקה.
יישומים פוטנציאליים של מיקרוביוטה תוך-גידולית בטיפול בסרטן
ביחס ליכולתה של מיקרוביוטה תוך-גידולית לחזות הישרדות סרטן ויעילות טיפולית, מחקרים מצביעים על כך שחלק מהמינים מתואמים באופן חיובי להישרדות הסרטן, למשל, מינים Fusobacterium בקרצינומות של תאי קשקש בפה ובפי הטבעת. לפיכך, מיקוד לחיידק זה עם אנטיביוטיקה עשוי לשפר את האפקט המרפא בחולים אלה.
בעוד שמחקרים נקשרו גבוה F. nucleatum שפע לפרוגנוזה גרועה של CRC, Alexander et al. מצאתי את זה גרנוליקלה ו ג'מלה מינים, זה משפר הישרדות ללא מחלה (DFS) בחולים לאחר כריתת CRC.
חוקרים זיהו גם מיקרוביוטה אחרת בקשר לפרוגנוזה של סוגי סרטן שונים. למשל, שפע של Actinomycetales ו Pseudomonadales הזמנות חזו DFS נמוך יותר בגידולי סרטן ריאות של תאים לא קטנים (NSCLC).
אפילו התערבויות המבוססות על מיקרוביוטה תוך-גידולית, במיוחד אימונותרפיה, הראו פוטנציאל רב בטיפול נגד סרטן.
חוקרים הדגישו את השימוש באנטיביוטיקה מרובעת למניעה ולטפל הליקובקטר פילוריסרטן קיבה שמקורו בתרופות אנטי-ויראליות נגד וירוס הפטיטיס C. באופן מסקרן, חיסונים נגד וירוס הרפס פפילומה ונגיף הפטיטיס B יכולים להעניק הגנה מפני סוגי סרטן רבים, כולל זה של צוואר הרחם בנשים, ראש צוואר וכבד.
יתר על כן, חיידקים מהונדסים, למשל, אי – קולי Nissle 1917, ובקטריופאג'ים, למשל, Fusobacteriumפאגים ממוקדים, הוכחו כמכוונים לחיידקים מזיקים בתוך גידולים.
לנגיפים אונקוליטיים יש גם השפעות טיפוליות חיוביות נגד סוגים שונים של סרטן, כפי שנצפה בשניהם in vivo ו בַּמַבחֵנָה לימודים. עם זאת, לאור יכולתם לשכפל, הם מציבים אתגרים הקשורים לבטיחות במסגרות קליניות.
סיכום
המחקר מלקט מידע ונתונים שעשויים להשלים מחקר עתידי על טיפולי סרטן ממוקדי מיקרוביוטה תוך-גידוליים, המצביעים על פוטנציאל לשיפור אפשרויות הטיפול בסרטן. בהתחשב ביכולות הניבוי והפרוגנוסטיות שלהם, חיידקים תוך-גידוליים עשויים גם לעזור לקדם את המטרה של אונקולוגיה מדויקת.
בעתיד, על החוקרים לשאוף גם לפתח פרוטוקולים סטנדרטיים לחקר חיידקים תוך-גידוליים כדי לתת מענה לממצאים הבלתי עקביים של מחקרים קודמים.
דרושים מחקרים פרוספקטיביים אורכיים נוספים עם דגימות גדולות כדי לחקור את ההשפעות של חיידקים תוך-גידוליים על סרטן ותאי חיסון ולהבין את הפוטנציאל לטיפול בגידולים על ידי שינוי המיקרוביוטה.
ראיות פרה-קליניות קריטיות נגזרות כאלה וגישות בין-תחומיות אחרות עשויות לעזור להפיק תובנות עמוקות לגבי הקשר הכמותי בין חיידקים תוך-גידוליים והשפעתם על גורמים קליניים הקשורים לסוגי סרטן שונים.
בנוסף, חקירת החתימות המיקרוביאליות והטיפולים המשולבים הללו עשויה להוביל ליעדים חדשים להתערבות קלינית בסרטן.



