תאי דם לבנים, או לויקוציטים, הם קו ההגנה הראשון והשני של הגוף מפני אורגניזמים וחלקיקים זרים. עם זאת, מעט תרופות מכוונות לייצור ותנועתם של תאים אלה למטרות שימושיות קלינית. מחקר חדש שפורסם בכתב העת חֲסִינוּת בוחן את נוף מולקולות האיתות כדי לזהות מטרות שניתן לסמים להגירת לויקוציטים לזרם הדם.
מחקר: עיכוב CBP/p300 היסטון אצטילטרנספראז עם מולקולה קטנה מגייסת לויקוציטים ממח העצם באמצעות תגובת הלחץ האנדוקרינית. קרדיט תמונה: Rost9 / Shutterstock
לויקוציטים, לרבות נויטרופילים, מונוציטים ולימפוציטים מסוג B, נוצרים במח העצם מתאי קדם יוצרי דם ובכמה איברים מיוחדים אחרים. הם מוחזקים במח העצם עד שהם משתחררים למחזור הדם.
ישנם שני תאים לויקוציטים בדם וברקמות ההיקפיות, אשר מראים שינויים בגודל עם מצבי גוף משתנים. לדוגמה, כאשר הגוף נפצע, לחוץ או נגוע, מספר הלויקוציטים ברקמה הפגועה משתנה וחוזר לקדמותו ברגע שהאיום מוכל.
שלבי רגולציה מרובים לוקחים חלק בפירוק לויקוציטים וכן בתנועה לאתרים שונים שבהם הם נחוצים. מקורם במערכת העצבים המרכזית (CNS) בתגובה לאותות פריפריאליים, מווסתים על ידי מעגלים עצביים שבהם משתתפים גם מערכת העצבים הסימפתטית וגם ציר ההיפותלמו-יותרת המוח-אדרנל (HPA).
האותות הללו פועלים להגברת ההמופואזה של מח העצם, לגייס לויקוציטים לדם ולרקמות אחרות היכן שהם נדרשים, ולהבטיח שהם יחזרו לרמות נורמליות לאחר שהאתגר התגבר.
במצבי מחלה מסוימים, השליטה ההומאוסטטית הזו אובדת, ובכך מובילה לספירות חריגות, כגון אי ספיקת מח עצם מחד או לוקמיה חריפה מאידך. עם זאת, עדיין, מעט תרופות יכולות לעזור לתקן חוסר ויסות כזה על ידי שינוי קצב הייצור, הפירוק או ההגירה של לויקוציטים, בין אם בסרטן הדם, בדלקת כרונית או במצבי היפר-דלקת חריפים.
בין התרופות הזמינות ניתן למנות את משפחת גרנולוציטים מגרה (G-CSF), אנטגוניסטים ל-CXC-motif chemokine receptor 4 (CXCR4) כגון plerixafor/AMD3100), או מעכבי אינטגרין מאוד מאוחר אנטיגן 4 (VLA4). G-CSF משמש, למשל, לתיקון נויטרופניה בחולים המטופלים בכימותרפיה, אך הוא פחות שימושי בחולים עם מצבי חום חריפים הכוללים ספירת נויטרופילים נמוכה. יתר על כן, G-CSF יכול לגרום לתופעות לוואי בחלק מהחולים.
הצורך לדעת יותר על תחום זה של פרמקולוגיה הניע את המחקר הנוכחי. הוא מתמקד במולקולה קטנה הנקראת חלבון p300 הקשור ל-E1A (EP300 או p300), אשר נראה כי הוא נרכש לאחרונה במהלך השלב הלוקמי של מצב הנקרא נויטרופניה מולדת חמורה (SCN).
אובדן התפקוד של גן זה הוביל להפחתת ייצור תאי הדם אם נמחק לפני הלידה, אך ספירת לויקוציטים גבוהה או לויקומית בשלב מאוחר יותר בחיים. יש לזה חלבון אורתולוגי, מחזורי-אדנוזין-מונופוספט-תגובה-אלמנט קושר חלבון (CREBBP, הידוע גם בשם "CBP", עם 90% הומולוגיה של רצף. אחד מ-8 התחומים בגן זה אחראי להיסטון אצטילטרנספראז (HAT) פעילות ומכיל מוטציה ב-SCN הגורמת להתמרה לויקמית.
במקרה זה, תחום זה עשוי להיות ניתן לסמים כדי לייצר "לויקוציטוזיס לפי דרישה"על ידי שינוי הגדלים של תאים לויקוציטים שונים.
מה הראה המחקר?
המדענים מצאו שעיכוב תחום ה-CBP/p300 בפעילות ה-HAT שלו על ידי מעכב המולקולה הקטנה A485 הוביל לעיכוב תחרותי הפיך של פעילות האנזים HAT, במיוחד עבור CBP ו-p300 בהשוואה ל-HATs אחרים. כצפוי, זה הוביל לעלייה מהירה ברמות האצטיל CoA בתוך מקרופאגים של מח עצם במודלים של עכברים. התוצאה הייתה לויקוציטוזיס מהירה.
נמצא כי זו פעולה תלוית מינון ולא דעכה במתן חוזר. כאשר נעשה שימוש בסוג אחר של מעכבי CBP/p300 HAT (C646), נצפתה אותה השפעה, המאששת את מנגנון הפעולה. לעומת זאת, מעכבי קשירת DNA על ידי החלבון או של HAT אחר שנמצאו ביונקים לא הצליחו לגרום ללוקוציטוזיס.
רמות A485 בדם עלו במהירות כאשר הוזרקו לעכברים, והצטברו במח העצם, ברקמות השומן, בכבד, בטחול ובכליות, אך לא במוח. ספירת הלויקוציטים עלתה במקביל, כולל נויטרופילים, לימפוציטים ומונוציטים. שבוע לאחר מכן, לא נצפו עדויות למתן תרופה, מה שמצביע על השפעה חולפת.
העלייה בספירת הלויקוציטים הייתה דומה לזו שהושגה על ידי G-CSF, אם כי מהירה יותר עבור נויטרופילים. כאשר שניהם ניתנו, התוצאה הייתה ספירת נויטרופילים גבוהה יותר. עם זאת, לאחר 24 שעות, כל שלושת סוגי תאי הדם הועלו עם G-CSF לעומת A485.
זה מצביע על פעולה קצרה ושונה יותר של A485 בהשוואה ל-G-CSF.
כדי להרחיב את התצפיות לנבדקים אנושיים, החוקרים בחנו נתונים מקבוצה של חולים עם מחלה נדירה בשם תסמונת רובינשטיין-טיבי (RSTS), שם CREBBP ו EP300 מתרחשות מוטציות. לכשני שליש היו ספירת לויקוציטים גבוהה, כאשר 70% הראו מוטציות בתחום ה-HAT. כצפוי, קבוצה זו הייתה בעלת סיכוי גבוה יותר להראות לויקוציטוזיס מאשר הקבוצה השנייה, שבה נחסך HAT.
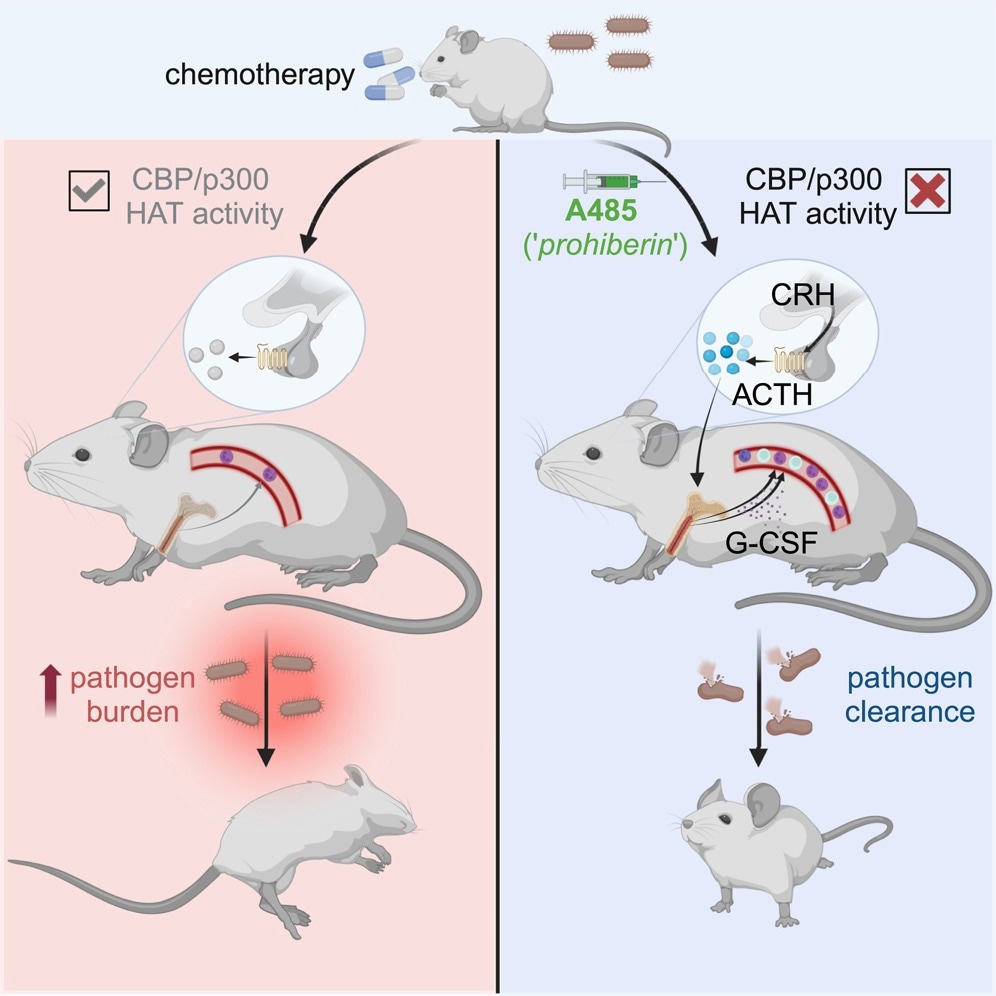
האם לתצפית זו יש תועלת קלינית? כדי לגלות, הם בדקו את ההשפעה של A485 בקבוצה של עכברים עם תסמונת מיאלודיספלסטית (MDS), ומצאו שהמולקולה הקטנה שמרה על ספירת הלויקוציטים תקינה. שנית, הם גרמו נויטרופניה חמורה על ידי קורס של כימותרפיה במודל של עכבר, מה שהראה כי A485 הוביל להתאוששות חריפה של ספירת לויקוציטים.
ואז, הם הציגו את האורגניזם חיידקי ליסטריה במינון מעורר אלח דם בעכברים עם pancytopenia הנגרמת על ידי כימותרפיה. נויטרופילים חיוניים להגנה החיסונית מפני חיידק זה. לאחר שהחלה זיהום, הם הזריקו A485 לעומת רכב בבקרות.
בעוד אלו שטופלו ברכב חלו ומתו מאלח דם, A485 במינון בודד הוביל להישרדות משופרת, עם פחות חיידקים שהחלימו מחיות שטופלו. A485 מגייס לויקוציטים ממח העצם, שהוא המנגנון של לויקוציטוזיס. לעומת זאת, לא הייתה hematopoiesis חירום במח העצם.
תת-קבוצות שונות של לויקוציטים הגיבו למסלולים שונים שהופעלו על ידי A485. אלה כוללים גם מסלולים תלויי G-CSF וגם מסלולים בלתי תלויים של נויטרופיליה, אך מסלולים אחרים ללימפוציטוזיס.
יתר על כן, A485 משתמש במסלולים נוירו-הומורליים, במיוחד בציר HPA, כדי לגרום לויקוציטוזיס, כפי שניתן לראות ברמות המוגברות של גלוקוקורטיקואידים בדם לאחר מתן A485. עם זאת, תגובת הלויקוציטוזיס המופעלת על ידי הפעלת HPA אינה מסתמכת על גלוקוקורטיקואידים, אלא מתרחשת בתגובה לאותות המווסתים על ידי CRHR1, כולל ההורמון האדרנוקורטיקוטרופי (ACTH), המתרחש עם אובדן אותות משוב HPA.
בעוד שהנויטרופילים עולים עם מתן ACTH, ספירת הלימפוציטים עולה רק עם חסימת גלוקוקורטיקואידים, מה שמעיד על כך ששניהם מוסדרים בצורה שונה.
מה ההשלכות?
"עיכוב תחרותי, הפיך, בתיווך מולקולה קטנה של תחום ה-CBP/p300 HAT מפעיל גיוס לויקוציטים אקוטי וחולף ממח העצםדרוש מחקר נוסף כדי לזהות אילו הקשרים קליניים הם אידיאליים לתרופה זו. A485 עשוי להיות טוב יותר אם נדרשת רק עלייה קצרה ומהירה של נויטרופילים, בעוד שהחלמה ארוכת טווח של ייצור תאי דם במח העצם עשויה לדרוש G- CSF.
יש להגדיר גם את העיתוי של מתן תוצאות טובות מכיוון שחולים עם אלח דם נויטרופני נמצאים בנקודות זמן ובשלבים שונים. יתרה מכך, הערך של תרופות כאלה באלח דם חיידקי או ויראלי, ולא ליסטריאלי, נותר בלתי נחקר.
עם זאת, כפי שדווח על ידי חוקרים קודמים, יש לו השפעות אנטי-גידוליות, מה שעלול להפוך אותו לבעל ערך בטיפול משלים לחולי סרטן. המחקר הנוכחי שופך אור גם על התפקיד של ACTH, ולא על מוצריו במורד הזרם, הגלוקוקורטיקואידים, על הומאוסטזיס לויקוציטים ופעילות G-CSF.