בסקירה שפורסמה לאחרונה בכתב העת חוות דעת על טבע סרטן, חוקרים מציגים טיעונים משכנעים מדוע הבנה בסיסית של הפוטנציאלים והמגבלות של יישומי בינה מלאכותית (AI) הופכת במהירות הכרחית במלחמה של היום נגד סרטן. הם מציגים בקצרה בינה מלאכותית והמודלים הקשורים לה (רשתות עצביות מלאכותיות (ANNs), למידה עמוקה ומודלים של שפה גדולה (LLM)), ומדגישים את ההתקדמות בתחום ויישומם בחקר הסרטן, ואת האתגרים העומדים בפני אימוץ טכנולוגיית AI בכל מקום. בלימודים מתמשכים.
סקירה זו נועדה לשמש קו מנחה מעשי לאימוץ בינה מלאכותית לחקר הסרטן המיינסטרים, ממוקד בעיקר לביולוגים סרטניים שאינם בעלי נטייה חישובית. הוא מספק דוגמאות רבות לאופן שבו הטכנולוגיה יכולה לזרז את התקדמות המחקר ולזהות דפוסים בלתי נראים לעין אנושית.
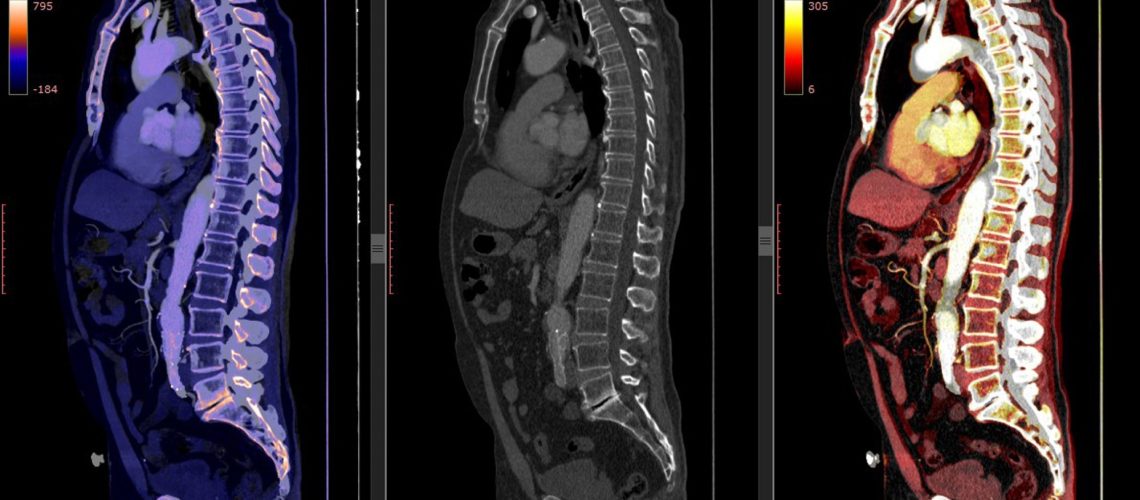
מאמר סקירה: מדריך לבינה מלאכותית עבור חוקרי סרטן. קרדיט תמונה: springsky / Shutterstock
מהו AI, ולמה זה צריך להיות חשוב בחקר הסרטן?
בינה מלאכותית (AI) היא כינוי גג לטכנולוגיות ויישומים רבים המנסים לדמות אינטליגנציה אנושית ועיבוד נתונים באמצעות אלגוריתמי מכונות בעלי דיוק גבוה. למרות שנחשבה נרחבת כמקורה במהלך כנס ב-1956 (קולג' דארטמות'), בינה מלאכותית נשארה מערכת מבוססת כללים תיאורטית במשך רוב קיומה, כאשר ה-AI המכונה כעת 'בינה מלאכותית סמלית' ו'למידת מכונה קלאסית' שולטות בתחום עד לאחרונה כמו 15 השנים האחרונות.
התפתחות חסרת תקדים ברשתות עצביות מלאכותיות פשטניות (ANNs), אלגוריתמים של התפשטות לאחור, ולאחרונה, רשתות עצביות עמוקות (DNNs) ומודלים של שפה גדולה (LLMs) הוציאו את התחום מהשורשים התיאורטיים שלו וראו את האימוץ הנרחב שלו על פני מחקר ויישומים תעשייתיים. . השחרור האחרון של יישומים המונעים על ידי LLM ולמידה עמוקה כמו Gemini AI ו-ChatGPT לציבור האיצה עוד יותר את צמיחת הבינה המלאכותית, כאשר המחקר הרפואי הופך להיות תלוי יותר ויותר בטכנולוגיות אלו לצורך אבחון, גילוי תרופות וניתוח נתונים.
"…אנו מניחים שכל חוקר סרטן בימינו צריך לרכוש רמה מסוימת של אוריינות בינה מלאכותית. כיום, חשוב להיות מסוגל להבין, לפרש ולהעריך באופן ביקורתי את תפוקת הבינה המלאכותית. בנוסף, חלק מחוקרי הסרטן ימצאו מועיל לרכוש הבנה עמוקה יותר של AI ופיתוח כלי תוכנה מבוססי AI משלהם.
חקר הסרטן אינו שונה, כאשר יישומים מבוססי בינה מלאכותית משמשים יותר ויותר בעיבוד תמונה סלולרי ומולקולרי, מחקר היסטופתולוגיה ורדיולוגיה. LLMs, במיוחד, משמשים יותר ויותר לאיסוף ולנתח נתונים קליניים, תוך שיפור ניכר בקצב עיבוד הנתונים ועוזר לזהות דפוסים ומגמות עדינות בתוך הנתונים שלעתים קרובות היו מתגעגעים במהלך חיפושים אנושיים ידניים.
לגבי הביקורת
הסקירה הנוכחית מבקשת לשכנע חוקרי סרטן, במיוחד אלה שאינם בעלי נטייה חישובית, ביתרונות של AI והטכנולוגיות הנלוות לה בהתקדמות ההבנה שלנו של המחלה וכיצד להילחם בה. המחברים מצטטים יותר מ-170 פרסומים רפואיים וחישוביים תוך התחקות אחר התפתחות הבינה המלאכותית מהשורשים התיאורטיים שלה לפני כמעט 70 שנה ועד ליישומים המעשיים המוכרים הרבה יותר שאנו מוצאים כיום.
לאחר מכן, הם צמצמו את היקף ההיכרות שלהם עם AI כדי להתמקד ביישומים הנוכחיים והפוטנציאליים של הטכנולוגיות במחקר ובטיפול בסרטן. הם הדגישו תוכנות 'מדף' נגישות בקלות, הזמינות לכל חוקר סרטן ללא קשר למיומנות חישובית ולסייגים שיש לזכור בעת פירוש התפוקות של חלק מהפלטפורמות הללו.
הבנת למידה עמוקה
כאן מציגים החוקרים את המסגרת התיאורטית השולטת באלגוריתמים קלאסיים של למידת מכונה וכיצד אלה התפתחו לטכנולוגיות הלמידה העמוקה של ימינו. הם מבדילים בין הסוגים השונים של למידה עמוקה (בפיקוח, ללא פיקוח וחיזוק) לבין היישומים הנוכחיים שלהם בחקר הסרטן. המרכיב המרכזי של סעיף זה הוא האוטומציה שמעניקות פלטפורמות למידה עמוקות חיזוק והחיסכון המשמעותי בזמן (פרודוקטיביות) שהן יכולות לספק על פני גישות אנליטיות קונבנציונליות, במיוחד במהלך ניסויים קליניים גדולים.
ניתוח תמונה ביו-רפואי
סעיף זה מדגיש שימוש בבינה מלאכותית בזיהוי תמונות, זיהוי ומיון. הוא עוקב אחר התפתחות היישום הרפואי שלו מתודולוגיות למידת מכונה קלאסיות של סוף שנות ה-90 ותחילת שנות ה-2000 לאלגוריתמים המורכבים יותר של היום. הראשון שימש לאיתור ומיון תמונות מיקרוסקופיה, בעוד שהנוכחי התקדם מספיק כדי שהם יכולים להשתמש בסמנים ביולוגיים כדי לאבחן את סוג הסרטן וחומרתו.
"משימות ניתוח תמונות רבות במחקר ביולוגי מבוצעות באופן מסורתי באופן ידני, אולם זה לא רק לא יעיל ונוטה לשגיאות, אלא גם יכול להפוך ניסויים לבלתי אפשריים אם יש לנתח אלפי תמונות פלט. באופן כללי, על ידי שימוש בלמידה עמוקה כדי לכמת קריאות ניסיוניות , הניתוח יכול להיעשות אובייקטיבי יותר, אמין ומהיר יותר. לדוגמה, בהקשר של זיהוי תאים במיקרוסקופ של ניגודיות, למידה עמוקה יכולה לזהות במהירות ובאמינות תאים בודדים ולסווג אותם כחיים או מתים בשימוש, למשל, באמצעות פלטפורמות מסחריות כגון מודול התוכנה Incucyte AI Cell Health Analysis (Sartorius AG)."
חלק זה מציג כלי למידה עמוקה זמינים מסחרית סטנדרטיים ליישום בינה מלאכותית בהיסטופתולוגיה ופתולוגיה חישובית, ובמקביל מציע שחלק מכלי למידה עמוקה שנבנו בהתאמה אישית אינם מורכבים לקוד כפי שאנשים שאינם בעלי נטייה חישובית בינינו עשויים להאמין. הסעיף מפרט עוד כמה מהאתגרים העומדים בפני אימוץ ניתוח התמונה הביו-רפואי של בינה מלאכותית, שהחשוב שבהם הוא "ההסברה" – בהתחשב בחידוש היחסי של הטכנולוגיה, לא ניתן (עדיין) להסביר חלק מהדפוסים שזוהו על ידי כלי בינה מלאכותית. עם זאת, שינויים אחרונים באלגוריתמי AI והשימוש בניסויים קליניים כדי לאמת חלק מהדפוסים הבלתי מוסברים הללו עוזרים להתגבר על האתגרים הללו.
גילוי סמים
דגמי שנאים גדולים, תת-מעמד חדש של טכנולוגיות בינה מלאכותית, עושים צעדים משמעותיים בתחום גילוי תרופות לסרטן. בניגוד ליישומים קונבנציונליים, מודלים אלה יכולים לחזות את פוטנציאל הקישור והיעילות של תרופות מועמדות לאזורים תפקודיים של חלבוני המטופלים, ובכך להפחית את מידת אי הוודאות הכרוכה בניסויים קליניים נוכחיים ועתידיים.
מסקנות
האתגר המשמעותי ביותר של AI בחקר הסרטן כיום הוא כריית נתונים מהעולם האמיתי (RWD), כולל EHRs, דגימות גידול ותמונות רפואיות. בניגוד לנתוני ניסויים קליניים, אשר בדרך כלל עוקבים אחר מתודולוגיות מוגדרות היטב, RWD הוא בדרך כלל אקראי הן במצב האיסוף והן בתיעוד שלו, מה שמגדיל משמעותית את מורכבות הניתוח שלו. עם זאת, למרות האתגרים, הצמיחה והאימוץ חסרי התקדים של AI מצייר עתיד מרגש לאונקולוגיה, ואוריינות בסיסית של אזהרותיה הופכת במהירות להכרח, לא לבחירה, עבור הביולוג הסרטן המתהווה.