סקירה חדשה מדגישה כיצד סוכרת ותרופות ירידה במשקל טירזפטטיד עלולות לשבש את מחלת האלצהיימר על ידי תיקון חילוף החומרים המוחי והפחתת הדלקת.
לִלמוֹד: Tirzepatide: גישה טיפולית חדשה למחלת אלצהיימרו קרדיט תמונה: atthapon raksthaput/shutterstock.com
בסקירה שפורסמה לאחרונה בפורסם ב מחלת מוח מטבוליתקבוצת מחברים בחנה את המנגנונים המולקולריים הפוטנציאליים שבאמצעותם מפעיל טירזפטיד (TRZ) השפעות נוירו -הגנות במחלת אלצהיימר (AD).
רֶקַע
AD משפיעה על למעלה מ 55 מיליון אנשים ברחבי העולם ונשארת הגורם המוביל לאובדן מתקדם של זיכרון ויכולות קוגניטיביות, המכונה בדרך כלל דמנציה. זה קשור למספר הפרעות מטבוליות כמו סוכרת מסוג 2 (T2D) והשמנת יתר, וגורמים לדלקת כרונית בדרגה נמוכה ולחץ חמצוני, שיכולים להוביל עוד יותר להתנוונות עצבית.
עדויות הולכות וגוברות מראות כי עמידות לאינסולין (IR) במוח יכולה לאתגר את התפקוד העצבי, וזו הסיבה שלעתים קרובות מכונה AD "סוכרת מסוג 3". תרופות נוכחיות כמו TRZ, המפעילות פפטיד 1 דמוי גלוקגון 1 (GLP-1) וגם קולטני פוליפפטיד מעכב קיבה (GIP), נבדקות על הפוטנציאל העצבי שלהם. יש צורך במחקר נוסף כדי לאמת את הפוטנציאל העצבי שלה בהגדרות קליניות.
הבנת מחלת האלצהיימר הפתופיזיולוגיה
AD מונע בעיקר על ידי שתי תכונות פתולוגיות: הצטברות פלאק עמילואיד חוץ תאי (Aβ) וסבכים נוירופיברילריים תוך -תאיים המורכבים מחלבון טאו. חריגות אלה משבשות את התקשורת העצבית, מקדמות דלקת ומוות מוות של תאים.
בעוד שמקרי ספירה בירושה נדירים נגרמים כתוצאה ממוטציות בגנים של מבשר עמילואיד (APP) ובגנים של presenilin, רובם מתרחשים באופן ספורדי. הם קשורים לגורמים כמו IR ודלקת לטווח הארוך. הכישלון לנקות כראוי את ה- Aβ מהמוח ושיבושים באיתות אינסולין הם מרכזיים בהתקדמות המחלה.
מנגנון הפעולה של טירזפטד
TRZ מאושר לניהול T2D והשמנת יתר. זה לא רק משפר את רמות הסוכר בדם אלא גם חוצה את מחסום הדם-מוח, מה שהופך אותו לטיפול מבטיח למחלות עצביות. במערכות היקפיות זה מפחית את משקל הגוף, משפר את פרופילי השומנים ומוריד סמנים דלקתיים. פעולות אלה מיטיבות בעקיפין את המוח על ידי צמצום התפקוד המטבולי התורם לספירה.
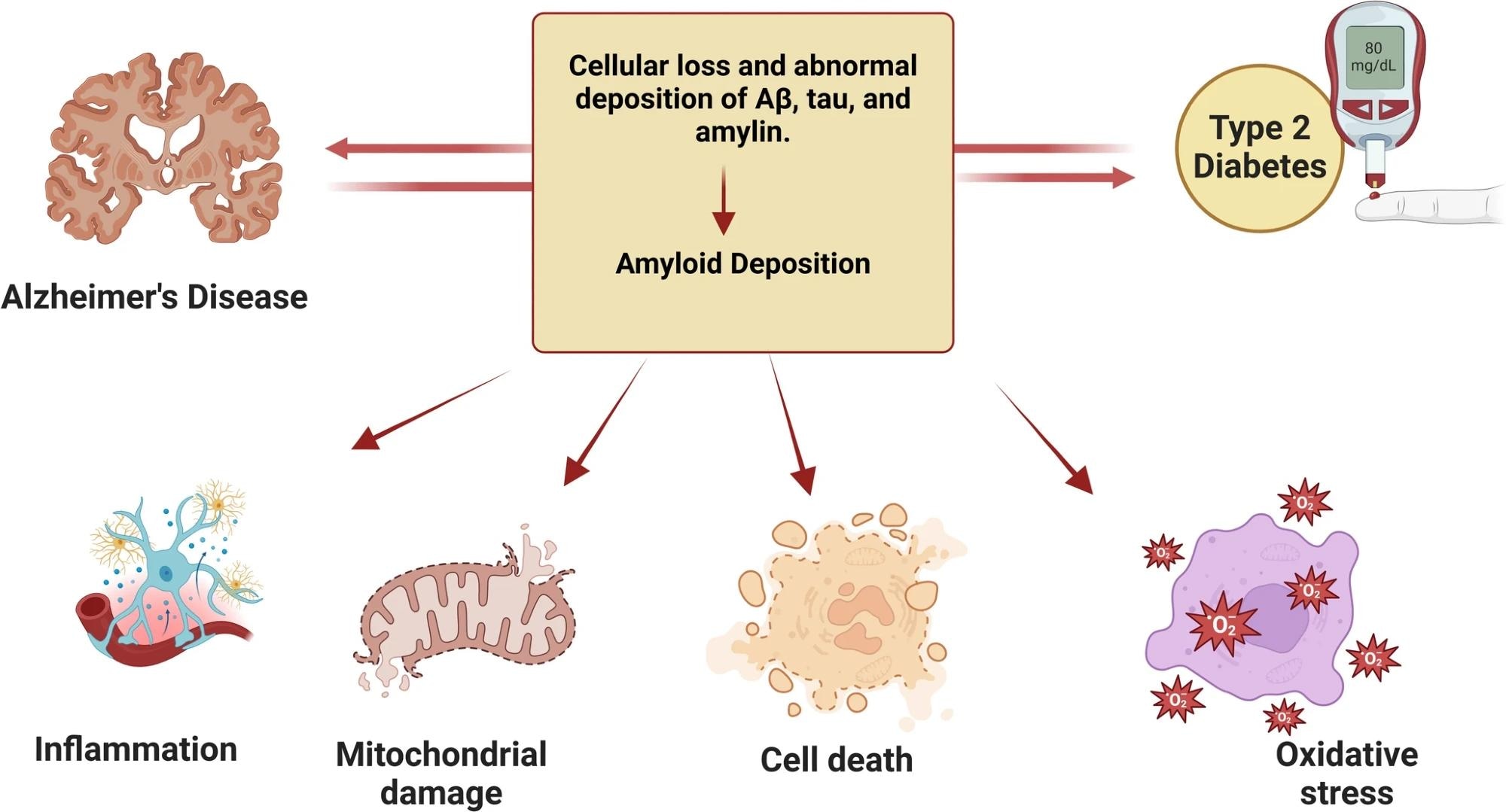
דלקת נוירואין ועמידות לאינסולין
מודעה מוכרת יותר ויותר כקשורה ל- IR במוח. במצב זה, איתות אינסולין בתוך מערכת העצבים המרכזית (CNS) נפגע, מה שמוביל לתפקוד סינפטי ולחסרון קוגניטיבי.
TRZ משפר את רגישות האינסולין במוח דרך הפוספואינוזיטד 3-קינאז/חלבון קינאז B/גליקוגן סינטאז קינאז שלוש בטא (PI3K/AKT/GSK3β) מסלול איתות. מחקרים פרה -קליניים הראו כי מסלול זה משחזר את חילוף החומרים הגלוקוזי בנוירונים, מצמצם את התצהיר ה- Aβ ושומר על תפקוד קוגניטיבי.
מעבר לשיפור איתות האינסולין, TRZ גם מסייע בהרגעת דלקת מוחית על ידי הפחתת הפעילות במסלולי דלקת עיקריים כמו NLRP3 דלקתית וגורם גרעיני קאפה B (NF-κB), שידוע כי הם מניעים הפעלה מיקרוגלית ודלקת נוירואין ב- AD.
עכברים שטופלו ב- TRZ הראו רמות מופחתות של סמנים אלה, מה שמצביע על כך שהתרופה יכולה לדכא את דלקת הנוירואין ואת התקדמות המחלה שעלולה לאט. עם זאת, הסקירה מציינת כי לא כל התוצאות הפרה -קליניות היו חיוביות באופן אחיד. מחקר אחד מצא כי TRZ והסמגלוטיד התרופה הקשורה לא הפחיתו את רובד העמילואיד או שיפרו את הגירעונות הקוגניטיביים במודלים של עכברים טרנסגניים ספציפיים של AD.
המחברים מציעים כי הבדלים בתכנון ניסיוני, במינון או במודלים של בעלי החיים הספציפיים ששימשו עשויים להסביר תוצאות מעורבות אלה. עם זאת, הדבר מדגיש את הצורך במחקר נוסף לפני שמסיימים מסקנות נחרצות.
השפעות על תפקוד מוחי הקשור להשמנה
השמנת יתר מעלה את הסיכון לספירה על ידי גרימת התנגדות לפטין, שיבוש שובע ותפקוד קוגניטיבי, ודלקת כרונית, מה שהופך את ההורמון ליעיל פחות בבקרת תפקוד התיאבון והמוח. TRZ משנה את הרגישות לפטין על ידי ויסות אדיפונקטין ושיפור ציר הלפטין-אדיפונקטין, ולשפר את תפקוד ההיפוקמפוס.
זה גם גורם לירידה במשקל, ומפחית בעקיפין ציטוקינים דלקתיים כמו אינטרלוקין -6 (IL-6) וגורם נמק הגידול-אלפא (TNF-α), המעורבים בשינויים עצביים.
מודלים פרה-קליניים מדגימים כי עכברים שמנים שטופלו ב- TRZ שיפרו את ביצועי הזיכרון ואת רמות המוח הנמוכות של פלאק עמילואיד. התרופה גם נורמלה את רמות הובילי הגלוקוז כמו טרנספורטר גלוקוז סוג 1 (GLUT1), טרנספורטר גלוקוז סוג 3 (GLUT3), וטרנספורטר גלוקוז סוג 4 (GLUT4), הקריטיים לאספקת אנרגיה עצבית. תוצאות אלה מדגישות את הפעולה הרב -גונית של TRZ בטיפול בשורשים המטבוליים של הירידה הקוגניטיבית.
Tirzepatide ו- Autophagy
Autophagy, מנגנון המוח לפינוי חלבונים ואברונים פגומים, נפגע משמעותית ב- AD. TRZ מפעיל גנים ואנזימים הקשורים לאוטופגיה, מקדם את אישור ה- Aβ ושיפור הבריאות העצבית. זה משיג זאת דרך מסלול PI3K/AKT, ומשפר את החוסן הסלולרי ללחץ ועיכוב הזדקנות עצבית. זה רלוונטי במיוחד אצל אנשים עם T2D, כאשר אוטופאגיה פגומה היא תכונה משותפת עם AD.
נוירוגנזה ובריאות סינפטית
TRZ תומך בהתחדשות עצבית ומגביר את ייצור הגורם הנוירוטרופי הנגזר במוח (BDNF) וחלבון מחייב אדנוזין מונופוספט מחזורי (CREB), חיוני לזיכרון וללמידה. זה מסדיר באופן חיובי את MicroRNAs (miRNAs), כגון miR-212-3p ו- miR-29c-5p, השולטים במסלולי אפופטוטי ועיבוד אפליקציות.
בנוסף, טיפול ב- TRZ מווסת חלבונים המעורבים בפלסטיות סינפטית, כמו חלבון 43 הקשור לצמיחה (GAP-43) וחלבון 2 הקשור למיקרו-צינור (MAP2).
שינויים מולקולריים אלה מראים כי TRZ מונע התנוונות עצבית ותומך בתיקון מוח. בעוד שרוב הממצאים הללו מגיעים ממודלים של בעלי חיים, הם מציעים תובנות משכנעות על פוטנציאל התרופה כטיפול המשנה למחלות לספירה.
הסקירה מדגישה כי המנגנונים המדויקים העומדים מאחורי ההשפעות העצביות של TRZ עדיין אינן מובנות לחלוטין, וממצאים אלה טרם הוחלו על חולים אנושיים.
מסקנות
TRZ מציעה שדרה טיפולית מבטיחה לספירה על ידי מיקוד למנגנונים היקפיים ומרכזיים כאחד. זה מפחית דלקת מערכית, מתקן IR במוח, מקדם אוטופאגיה ומשפר את הבריאות הסינפטית. השפעות רב -פקטורליות אלה מתייחסות למרכיבים המטבוליים והנוירו -ניווניים של המחלה בו זמנית.
למרות שהראיות הנוכחיות נובעות בעיקר ממודלים פרה -קליניים, ההשפעה של TRZ על מסלולי מחלות מפתח מצדיקה חקירה נוספת במחקרים קליניים. ראוי לציין כי הסקירה מזהירה כי מחקרים מסוימים בבעלי חיים לא הראו תועלת, ולכן הפוטנציאל הקליני של TRZ ל- AD עדיין אינו בטוח. אם תוקף, זה יכול לייצג אסטרטגיה טרנספורמטיבית בניהול AD לצד T2DM והשמנת יתר.
הורד את עותק ה- PDF שלך עכשיו!