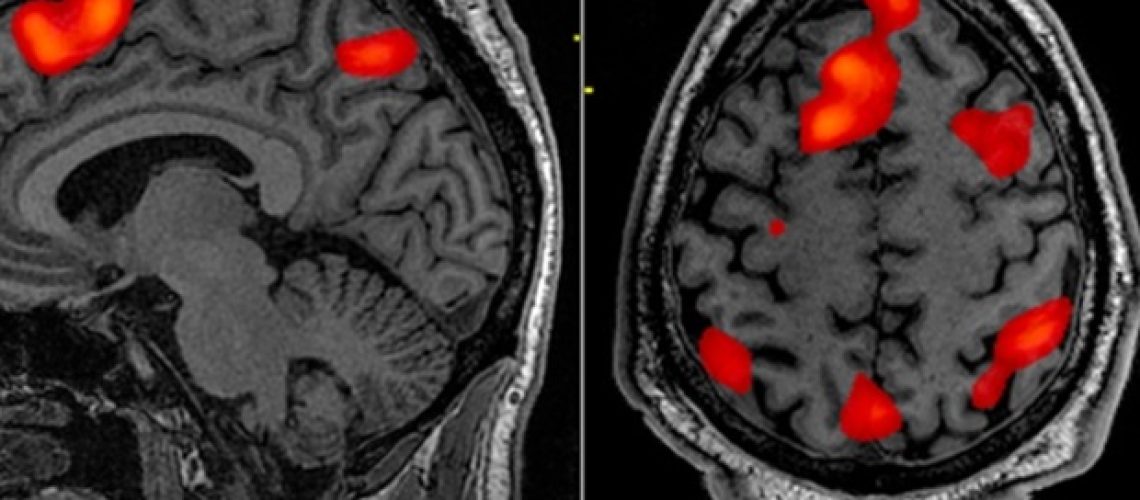
במאמר מקיף של עיתונות גנומית שפורסמה היום, חוקרים מאוניברסיטת פודן ואוניברסיטת שנחאי ברפואה סינית מסורתית הדגישו את ההתקדמות המדהימה בהתפתחות טומוגרפיה של פליטת פוזיטרון (PET) העקיבים המסוגלים לדמיין אגרגטים α-synuclein במוחם של חולים עם מחלת פרקינסון והפרעות קשורות.
ההצטברות הלא תקינה של חלבון α-synuclein היא תכונה פתולוגית מגדירה של מספר מצבים ניווניים-ניווניים הידועים באופן קולקטיבי בשם סינוקליינופתיות, כולל מחלת פרקינסון (PD), אטרופיה של מערכת מרובה (MSA) ודמנציה עם גופי Lewy (DLB). עד לאחרונה, אישור נוכחותם של אגרגטים חלבונים אלה נדרש לבדיקה לאחר המוות, מה שמגביל מאוד את האבחנה המוקדמת ויכולות ניטור טיפול.
"היכולת להמחיש אגרגטים חלבונים אלה בקרב חולים חיים מייצגת קפיצה משמעותית במחקר מחלות ניווניות," מסביר ד"ר פאנג שי, המחבר והחוקר המתאים במחלקה למרכז הרפואה הגרעינית והחיות המחמד בבית החולים Huashan, אוניברסיטת פודן.
רדיו מתאים שיכול למפות באופן לא פולשני במפונות סינוקליינופתיות באמצעות הדמיית PET יביא לפריצות דרך באבחון מוקדם, מעקב אחר התקדמות המחלה והערכת תגובות הטיפול. "
ד"ר פאנג שי, סופר וחוקר תואם, המחלקה לרפואה גרעינית ומרכז חיות מחמד בבית החולים Huashan, אוניברסיטת פודן
מאמר הפרספקטיבה סוקר בקפדנות את ההתקדמות האחרונה בפיתוח עקבות חיות מחמד, תוך תשומת לב מיוחדת למועמדים מבטיחים שהראו יעילות הן במסגרות המעבדות והן בקלינית. החוקרים מדגישים עוקבים כמו (18F) F-0502B, (18F) C05-05 ו- (18F) ACI-12589, שהדגימו תוצאות מעודדות בהבחנה בין חולים עם סינוקליינופתיות לבקרות בריאות.
פריצת דרך משמעותית במיוחד הגיעה כאשר (18F) C05-05 דמיין בהצלחה סינוקליינופתיות אצל עשרה חולים העומדים בקריטריונים לאבחון קליני למחלת פרקינסון או לדמנציה עם גופי לוי. עקבות זה הראה קשירה מוגברת בשטח המוח-אמצע-אזור נפוץ מפתולוגיות גוף לוי-וכריכה זו מתואמת היטב עם חומרת הסימפטומים המוטוריים.
מסלול מבטיח נוסף, (18F) ACI-12589, שפותח על ידי חברת הביוטק AC Immune, הראה תוצאות מדהימות בהבחנה בין אטרופיה של מערכת מרובה לבין מחלות עצביות אחרות. רדיו רדיו זה הציג שמירה רבה יותר בחומר הלבן המוח הקטן של חולי MSA בהשוואה לאלה עם בקרות PD, DLB או בריא.
למרות ההתפתחויות המעודדות הללו, המחברים מכירים בכמה אתגרים שנשארים בפיתוח עוקבי חיות מחמד אופטימליים α-synuclein. ההתפלגות ההטרוגנית והקונפורמציה של אגרגטים α-synuclein על פני סינוקליינופתיות שונות, יחד עם הצפיפות הנמוכה יחסית של תכונות פתולוגיות אלה, מסבכות את התפתחותם של חומרי הדמיה יעילים אוניברסלית.
ההשלכות הקליניות של ההתקדמות הללו נובעות מעבר לאבחון. האם כלי הדמיה אלה יכולים בסופו של דבר לסייע בריבוד המטופלים לניסויים קליניים על סמך הפרופילים הפתולוגיים הספציפיים שלהם? האם הם עשויים לשמש כסמנים ביולוגיים קריטיים להערכת היעילות של טיפולים המשנים מחלות המתעוררים הממוקדים לצבירת α-synuclein? שאלות אלה מדגישות את ההשפעה הפוטנציאלית המרחיקה לכת של טכנולוגיה זו על גישות רפואה בהתאמה אישית להפרעות ניווניות.
"התחום נע במהירות, ואנחנו עדים לתרגום תגליות מעבדה ליישומים קליניים", מציין ד"ר יינגפנג הוא, מוביל את המחבר מהמכון לרפואת קרינה באוניברסיטת פודן. "מה שהופך את ההתפתחויות הללו למרגשות במיוחד הוא הפוטנציאל שלהם לשנות את האופן בו אנו מאבחנים ומטפלים בהפרעות הרסניות אלה, שעלולות להתערב לפני שמתרחשת התנוונות עצבית בלתי הפיכה."
ככל שהאוכלוסייה הגלובלית מתיישנת, השכיחות של הפרעות עצביות צפויות לעלות באופן דרמטי. פיתוח של סמנים ביולוגיים של הדמיה אמינה לסינוקליינופתיות עשוי להשפיע באופן משמעותי על מאמצי ניהול קליני ועל מאמצי המחקר שמטרתם לפתח טיפולים המשנים מחלות.