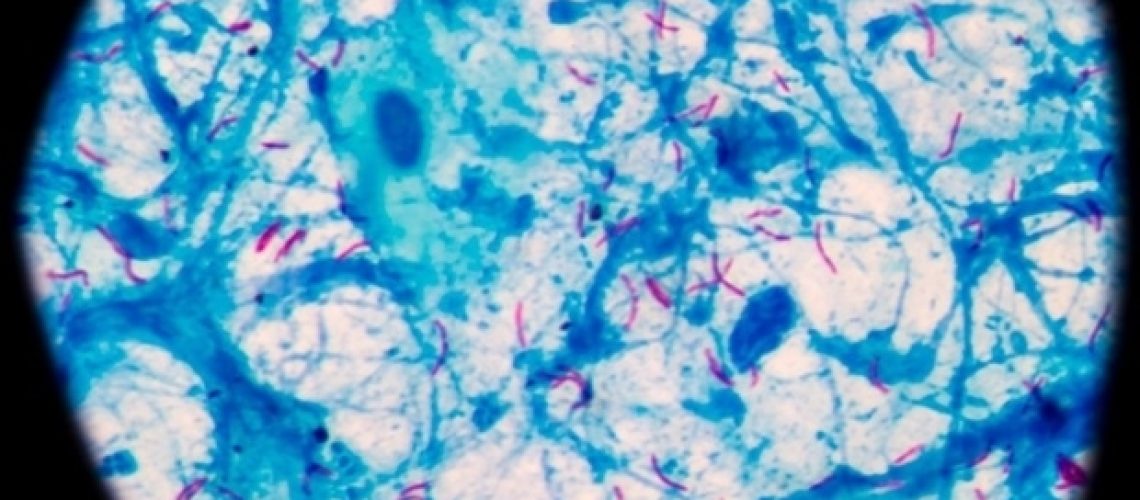
חוקרים ממכללת ביילור לרפואה ומוסדות משתפים פעולה גילו מנגנון שמניע את הירידה ארוכת הטווח בתגובה החיסונית הנצפית לאחר טיפול מוצלח בשחפת (TB). הממצאים שלהם, שפורסמו ב- הליכים של האקדמיה הלאומית למדעים, מציע דרך חדשה פוטנציאלית להחזיר את ההיענות החיסונית ולהפחית את הסיכון לתמותה לאחר זיהומים קשים.
"אלח דם, התגובה הקיצונית של הגוף לזיהום ושחפת קשורים לאובדן תגובות חיסוניות הגנה ולתמותה מוגברת לאחר טיפול מוצלח", אמר ד"ר אנדרו דינרדו, מחבר מקביל ופרופסור חבר במדור מחלות זיהומיות וחלוקה לרפואת ילדים. בריאות עולמית ומהגרים במכללת ביילור לרפואה ובבית החולים לילדים בטקסס. "במחקר הנוכחי, חקרנו מה תיווך את ההפרעה בתפקוד החיסוני לאחר זיהומים קשים".
החוקרים ידעו שזיהומים קשים וכרוניים בבני אדם ובעלי חיים מביאים לשינויים אפיגנטיים מתמשכים. שינויים אלה מתייחסים לשינויים בסימנים כימיים על ה-DNA שאומרים לתאים בגוף אילו גנים להפעיל או לכבות.
לדוגמה, שחפת מפחיתה את ההיענות החיסונית על ידי הוספת תגי מתיל כימיים נוספים (מתילציה של DNA) לגנים מסוימים המעורבים בתגובות החיסון. כתוצאה מכך, הגוף מייצר פחות חלבונים המתווכים הגנה חיסונית אשר מגבירה את הרגישות לזיהומים. עם זאת, המנגנונים הגורמים לשינויים אפיגנטיים בזיהומים לא היו ברורים.
TCA משחק תפקיד בשינויים אפיגנטיים
מחקרים קודמים זיהו את מחזור החומצה הטריקרבוקסילית (TCA), חלק מרכזי במטבוליזם התאי, כמניע מטבולי של הנוף האפיגנטי בסרטן. דינרדו ועמיתיו רצו לראות אם TCA מווסת גם את האפיגנטיקה, במיוחד מתילציה של DNA, לאחר סבילות חיסונית הנגרמת על ידי זיהום.
הצוות דיווח שתאי חיסון אנושיים שטופלו במעבדה בליפופוליסכריד חיידקי, מוצר חיידקי, ו Mycobacterium tuberculosisהחיידקים הגורמים לשחפת, הפכו לסבילות חיסונית.
הם גם מצאו שלחולים שאובחנו עם אלח דם וגם שחפת מוגברת הפעלת TCA, המתאם עם מתילציה של DNA. כאשר חולי שחפת קיבלו טיפול סטנדרטי של טיפול ואנטיביוטיקה, בתוספת אוורולימוס, מעכב הפעלת TCA, הופחתו השינויים המזיקים של המתילציה ב-DNA שלהם, מה שמצביע על כך שהוא יכול לעזור בשיקום המערכת החיסונית לאחר זיהומים קשים.
"שחפת היא מחלה מעניינת. עד שאדם מאובחן, יש לו תסמינים כבר למעלה משלושה חודשים. אבל לראות שהוספת אוורולימוס לטיפול אנטיביוטי סטנדרטי בשחפת מפחיתה את מספר סימני המתילציה המזיקים של DNA שישה חודשים לתוך המחלה, מבטיחה ש אנחנו יכולים לגרום לריפוי אפיגנטי", אמר דינרדו.
מה שמצאנו הולך להוביל לשינוי פרדיגמה. הגישות שלנו אינן מוגבלות לשחפת. הראיות שיש לנו ומה שאנחנו מנסים לבנות עליהן מצביעות על כך שאסטרטגיות אלה עשויות למלא תפקיד במחלות זיהומיות אחרות."
ד"ר כריסטיאן קוארפה, מחבר שותף ופרופסור חבר לביולוגיה מולקולרית ותאית בביילור
השלב הבא של החוקרים הוא לזהות אילו סימנים אפיגנטיים לאחר שחפת מובילים לעלייה בתחלואה ותמותה. משם, הם היו רוצים לקבוע אילו אנשים ירוויחו הכי הרבה מטיפול מכוון מארח שיכול לרפא צלקות אפיגנטיות.
תורמים נוספים למחקר זה כוללים את Abhimanyu, Santiago Carrero Longlax, Tomoki Nishiguchi, Malik Ladki, Daanish Sheikh, Amera L. Martinez, Emily M. Mace, Sandra L. Grimm, Thaleia Caldwell, Alexandra Portillo Varela, Rajagopal V. Sekha, Anna M. Madalakas, Mandla Mlotshwa, Sibuse Ginidza, Jeffrey Cirilo, Robert S. Wallis, Mihai G. Netea ו-Reinout van Crevel. המחברים קשורים לאחד או יותר מהמוסדות הבאים: Baylor College of Medicine, Texas Children's Hospital, Columbia University Irving Medical Center, UTHealth School of Public Health-Houston, Research Center Borstel, the Aurum institute, Radboud University Medical Center, University מבון, אוניברסיטת אוקספורד, אוניברסיטת קייס ווסטרן רזרב, אוניברסיטת ונדרבילט, אוניברסיטת יוהנסבורג ובית הספר לרפואה של טקסס A&M.