במחקר שפורסם לאחרונה בכתב העת Acta Neuropathologicaחוקרים זיהו שינויים גנטיים מגנים בנשאי APOEε4 נגד מחלת אלצהיימר (AD) באמצעות ריצוף גנום שלם (WGS) וניתוח מסלולים.
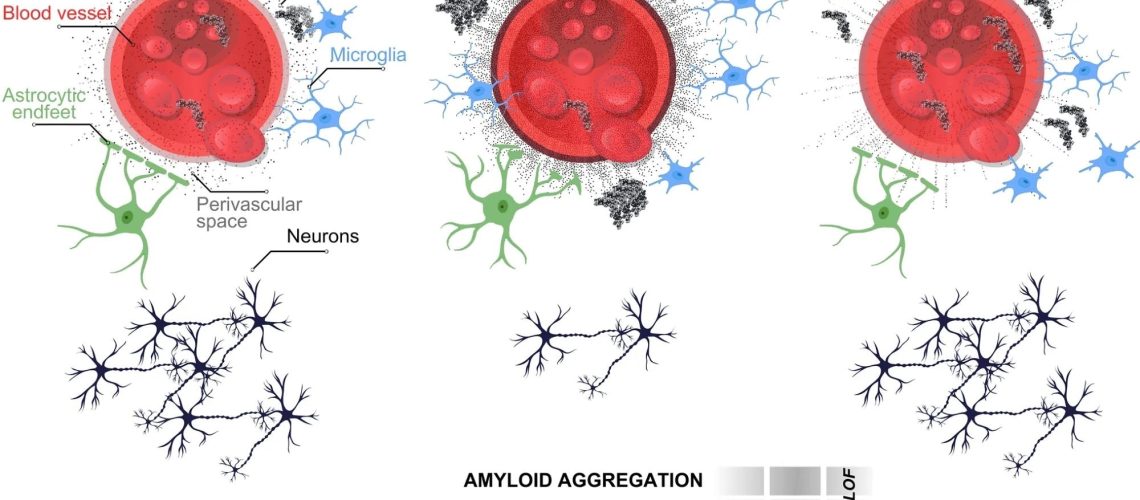
תקציר סכמטי לאפקט המגן של גרסאות FN1. לימוד: שונות גנטית נדירה בפיברונקטין 1 (FN1) מגינה מפני APOEε4 במחלת אלצהיימר
רקע כללי
AD מאופיינת באובדן זיכרון מתקדם וירידה קוגניטיבית, לרוב ללא תסמינים למשך תקופה ממושכת. בנתיחה שלאחר המוות, מוחות AD חושפים בדרך כלל רובדי β-עמילואיד וסבך נוירו-פיברילרי של חלבון טאו. למרות התקדמות ההבנה, AD נותרת ברובה בלתי ניתנת לטיפול, כאשר התרופות הקיימות מספקות הקלה מינימלית, בעיקר בשל ידע לא מלא של המנגנונים הפתולוגיים שלה. גורמים גנטיים, בעיקר האלל APOEε4, משפיעים באופן משמעותי על השונות של המחלה בין פרטים וקבוצות אתניות. ההשפעות של אלל זה משתנות, כאשר חלק מהנשאים חווים סימפטומים מתונים או מאוחרים יותר, מה שמדגיש את הצורך במחקר נוסף כדי להסביר את האינטראקציות הגנטיות המורכבות הללו ולפתח טיפולים ואבחון טובים יותר.
לגבי המחקר
כל הדגימות האנושיות במחקר זוהו, מה שהבטיח שהחוקרים לא יוכלו להסיק או לקבל מידע אישי מהתורמים. לפני הפקת נתונים קליניים, התקבלו אישורים מוועדת הביקורת המוסדית הן במרכז הרפואי של אוניברסיטת קולומביה, והן ב- Mayo Clinic. המחקר כלל גם ניסויים בבעלי חיים, אשר דבקו בהנחיות הוועדה לטיפול ושימוש בבעלי חיים (IACUC) באוניברסיטת קולומביה תחת הפרוטוקול המאושר ACAABN3554. תוכנית זו עומדת בסטנדרטים המוסמכים של AAALAC בינלאומיים ומקיימת הבטחת רווחת בעלי חיים עם שירות הבריאות הציבורי.
למחקרי דג הזברה, הן זני AB מסוג פרא והן fn1b−/− נעשה שימוש בקווי דגי נוקאאוט הומוזיגוטיים, בני 8 עד 10 חודשים ומשני המינים. בעלי חיים הוקצו באופן אקראי לתנאי ניסוי מאותו מצמד כדי להבטיח עקביות.
קבוצות אנושיות שהופיעו במחקר זה כללו את ה-NIA-AD Family Based Study (NIA-AD FBS), שכלל משפחות מרובות ברחבי ארה"ב. משפחות נבחרו בהתבסס על נוכחות של לפחות חבר אחד שאובחן עם AD מובהק או סביר לאחר גיל 60 ואח עם הופעה דומה. נתונים דמוגרפיים וקליניים מפורטים היו זמינים עבור משתתפים אלה. פרויקט ההזדקנות של Washington Heights/Inwood Columbia (WHICAP) גייס אנשים בני 65 ומעלה מצפון מנהטן כדי לחקור גורמי סיכון קליניים וגנטיים לדמנציה. ה-Estudio Familiar de Influencia Genetica en Alzheimer (EFIGA) כיוון לקבוצה אתנית אחרת, כולל משפחות מפורטו ריקו, הרפובליקה הדומיניקנית וניו יורק, כדי לזהות אללים מגנים בנשאים בריאים של APOEε4.
כל ההליכים, מהטיפול והשימוש בבעלי חיים ועד לטיפול בדגימות S, בוצעו תחת סטנדרטים אתיים ופרוטוקולים שאושרו על ידי הרשויות הרלוונטיות, מה שמבטיח רמה גבוהה של יושרה מדעית וכבוד לנבדקים של בני אדם ובעלי חיים המעורבים במחקר.
תוצאות המחקר
המחקר הנוכחי ניגש לנתוני WGS מ-3,578 פרטים על פני למעלה מ-700 משפחות ממוצא לבן והיספני לא היספני, כולן מושפעות מ-AD. באמצעות הרמוניזציה ובקרת איכות של נתוני ה-WGS, החוקרים זיהו גרסאות קידוד נדירות בנשאי APOEε4 שלא הושפעו קוגניטיבית וקשישים. לנשאים אלו, הן הומוזיגוטים והן הטרוזיגוטיים, היו גרסאות נדירות שלא נמצאו אצל לא נשאים. המחקר נתן עדיפות לגרסאות שעלולות להזיק למוצרי חלבון, וגילה 510 וריאנטים ב-476 גנים, המצוינים במיוחד בגן פיברונקטין 1 (FN1), בין היתר.
ניתוח אונטולוגיה של גנים גילה עוד העשרה חזקה לתהליכים הקשורים למטריצה חוץ-תאית (ECM) בגרסאות שזוהו. זה הצביע על כך ששינויים תפקודיים בהרכב ה-ECM יכולים להציע מנגנוני הגנה בנשאי APOEε4, מה שמצביע על כך שניתן לנטרל עליות הקשורות ל-APOEε4 ברכיבי ECM על ידי וריאנטים של אובדן תפקוד בגנים אלה. שני גנים משמעותיים, קולגן מסוג VI אלפא 2 שרשרת (COL6A2) ו-FN1, נבדקו עבור וריאנטים שעשויים להשפיע על יציבות ECM באמצעות שינויים בשאריות הטעונות, על פי ההשערה להשפיע על תפקוד החלבון.
ניתוחים נוספים כללו קבוצה עצמאית ממאגרי מידע כגון הקונסורציום הגנטי של מחלת אלצהיימר (ADGC) וה-Biobank של בריטניה (UKB), תוך התמקדות באנשים לבנים שאינם היספנים כדי לבדוק את שכפול הממצאים. הווריאציה rs140926439 ב-FN1 הראתה סיכון מופחת משמעותית ל-AD בנשאים הומוזיגוטים APOEε4, מה שמאשר את ההשפעה המגנה של וריאנט זה כנגד AD. בנוסף, ניתוחי רגישות אישרו את הממצאים הללו, וחיזקו את הפוטנציאל של הווריאציה כגורם מגן בהתקדמות AD.
המחקר גם חקר את המתאם בין מינון APOEε4 לבין שקיעת FN1 במחסום הדם-מוח. ניתוחי צביעת אימונו ברקמות המוח של אנשים עם גנוטיפים שונים של APOE הראו שרמות FN1 עלו עם מינון APOEε4, במיוחד בנשאים הומוזיגוטים.
לבסוף, התפקיד הפוטנציאלי של FN1 באפנון תגובות לרעילות עמילואיד נבדק באמצעות מודל של דג זברה. אובדן תפקוד FN1 בדג הזברה הוביל להפחתת אינטראקציות גליווסקולריות וירידה בתגובה גליוטית לאחר טיפול עמילואיד, מה שמצביע על כך שפיברונקטין יכול למלא תפקיד מכריע בוויסות פינוי בטא עמילואיד. זה מתיישב עם ההשערה שגרסאות אובדן תפקוד של FN יכולות להגן מפני פתולוגיה של AD על ידי שיפור פינוי אגרגטים של חלבון רעיל ומווסת פעילות מערכת החיסון.