במחקר שפורסם לאחרונה בכתב העת npj רפואה דיגיטליתחוקרים פיתחו מודל תאומים דיגיטליים המדמה צריכת אלכוהול מהחיים האמיתיים ומקשר אותה לסמנים ביולוגיים קליניים ארוכי טווח, ובכך משפרים אסטרטגיות eHealth להפחתת הרגלי שתייה מסוכנים.
לימוד: תאום דיגיטלי מבוסס פיזיולוגית לצריכת אלכוהול – חיזוי תגובות שתייה בחיים האמיתיים ו-PEth פלזמה לטווח ארוך. קרדיט תמונה: niksdope / Shutterstock.com
גישות להפחתת שימוש לרעה באלכוהול
צריכת אלכוהול מהווה כ-5% ממקרי המוות העולמיים ועלולה להגביר את הסיכון לבעיות בריאותיות משמעותיות כמו מחלות כבד וסרטן. שתייה כרונית ושתייה מוגזמת, שניהם הרגלים תכופים בקרב מבוגרים צעירים, עלולה לגרום הן לפציעות מיידיות והן לבעיות בריאות ארוכות טווח.
יישומי EHealth, כולל כלים כמו מחשבוני ריכוז אלכוהול מוערך בדם (eBAC), הראו הבטחה בהפחתת שתייה מופרזת. עם זאת, מודלים כמו משוואת Widmark, שמעריכה את רמות האלכוהול בדם, לא מצליחים לתפוס את המורכבות של דפוסי השתייה בחיים האמיתיים, כולל אינטראקציות עם סוגי משקאות שונים ומזון.
לפיכך, מדידה מדויקת של צריכת אלכוהול באמצעות סמנים כמו phosphatidylethanol (PEth) חיונית להתערבויות טובות יותר. עם זאת, דרוש מחקר נוסף כדי לשפר את המודלים הניבויים הללו ולקשר אותם לתוצאות בריאותיות.
לגבי המחקר
במחקר הנוכחי, מודל התאומים הדיגיטליים משתמש בסדרה של משוואות כדי לתאר את התהליכים הפיזיולוגיים המעורבים בשימוש באלכוהול. בתחילה, המודל ממנף משוואות דיפרנציאליות רגילות (ODEs), הממחישות כיצד משתנה המצב משתנה בתגובה לקצבי תגובה ותשומות.
המודל מפרט באופן מורכב את הדינמיקה של ריקון הקיבה על ידי שילוב משתנים כמו נפח המשקה ותכולת הקלוריות, שניהם משפיעים על נפח הקיבה וקצב ההתרוקנות. הדינמיקה הזו מושפעת מהתכולה הקלורית של נוזלים ומהנוכחות של מזון מוצק, כאשר משוואות ספציפיות מדגימות כיצד קלוריות ממזון מאטות את ריקון הקיבה.
המודל מתייחס גם לחילוף החומרים של אתנול, ומפרט כיצד אתנול יוצר אינטראקציה עם ארוחות בקיבה. ליתר דיוק, אתנול מובלע באופן זמני בתוך מזון, ובכך משנה את זמינותו לספיגה. המודל מתאר אינטראקציה זו, כמו גם שחרור אתנול ומטבוליזם שלאחר מכן דרך מסלולים אנזימטיים בכבד, כגון אלכוהול דהידרוגנאז (ADH) וציטוכרום P450 2E1 (CYP2E1), אשר מייצרים גם מטבוליטים כמו אצטט ו-PEth.
התנאים ההתחלתיים מניחים שהאדם מתחיל בצום ללא שאריות אתנול. הפרמטרים של המודל מוגדרים בקפידה, וערכים אופטימליים מוערכים מנתונים אמפיריים כדי להבטיח את דיוקם ומהימנותם.
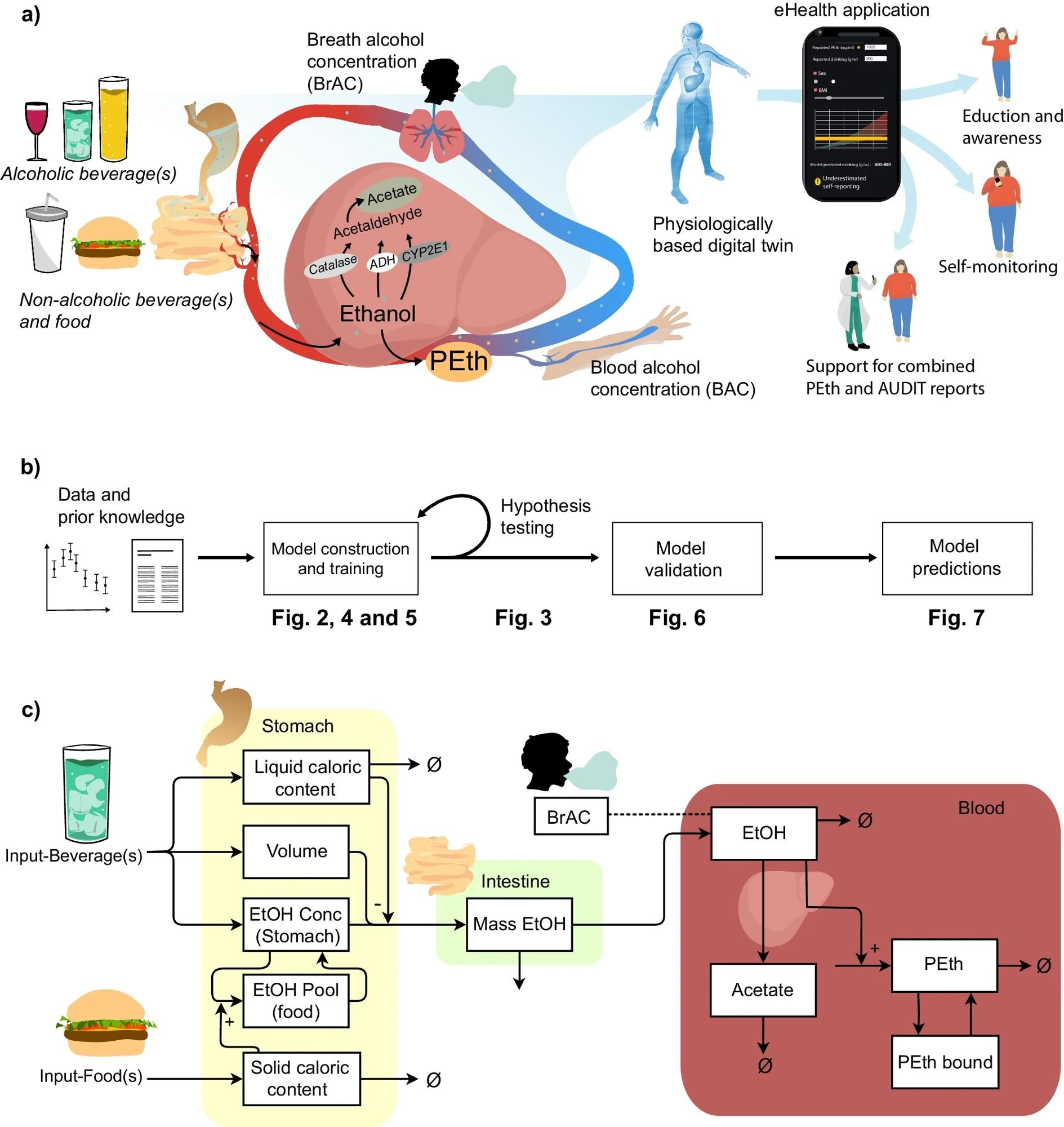 א סקירה קצרה של התהליך הפיזיולוגי שהמודל מתאר. אתנול נכנס לגוף דרך הקיבה, שם כבר כמות קטנה יכולה להיכנס לפלסמה. דרך התרוקנות הקיבה האתנול נכנס למעי. כאן, רוב האתנול נלקח באמצעות ספיגה. רוב האתנול עובר חילוף חומרים בכבד, וכמות קטנה מופרשת דרך מסלולי כליות. בכבד, אתנול הופך לאצטאלדהיד באמצעות שלושה מסלולי חמצון הנשלטים על ידי האנזימים: אלכוהול דהידרוגנאז (ADH), קטלאז וציטוכרום P450 2E1 (CYP2E1). אצטלדהיד הופך עוד יותר לאצטט ולאחר מכן לאצטיל-COA. קיימים גם מסלולים לא חמצוניים, האחראים לכמות זעירה של פירוק אתנול, למשל, לפוספטידילאתנול (PEth). לאחר מכן, נמדד ריכוז האלכוהול בדם (BAC), או ריכוז האלכוהול בנשימה (BrAC). ניתן לתאר תהליכים פיזיולוגיים אלו באמצעות מודל מתמטי, תאום דיגיטלי מבוסס פיזיולוגית. התאום הדיגיטלי יכול לשמש למספר מקרי שימוש, כגון לחינוך ומודעות, בדיווח עצמי ובניטור צריכת אלכוהול, וככלי לתמיכה בשילוב של דוחות AUDIT ו-PEth. ב סכמטי על גישת הדוגמנות. ג סכמטי המראה את מבנה המודל.
א סקירה קצרה של התהליך הפיזיולוגי שהמודל מתאר. אתנול נכנס לגוף דרך הקיבה, שם כבר כמות קטנה יכולה להיכנס לפלסמה. דרך התרוקנות הקיבה האתנול נכנס למעי. כאן, רוב האתנול נלקח באמצעות ספיגה. רוב האתנול עובר חילוף חומרים בכבד, וכמות קטנה מופרשת דרך מסלולי כליות. בכבד, אתנול הופך לאצטאלדהיד באמצעות שלושה מסלולי חמצון הנשלטים על ידי האנזימים: אלכוהול דהידרוגנאז (ADH), קטלאז וציטוכרום P450 2E1 (CYP2E1). אצטלדהיד הופך עוד יותר לאצטט ולאחר מכן לאצטיל-COA. קיימים גם מסלולים לא חמצוניים, האחראים לכמות זעירה של פירוק אתנול, למשל, לפוספטידילאתנול (PEth). לאחר מכן, נמדד ריכוז האלכוהול בדם (BAC), או ריכוז האלכוהול בנשימה (BrAC). ניתן לתאר תהליכים פיזיולוגיים אלו באמצעות מודל מתמטי, תאום דיגיטלי מבוסס פיזיולוגית. התאום הדיגיטלי יכול לשמש למספר מקרי שימוש, כגון לחינוך ומודעות, בדיווח עצמי ובניטור צריכת אלכוהול, וככלי לתמיכה בשילוב של דוחות AUDIT ו-PEth. ב סכמטי על גישת הדוגמנות. ג סכמטי המראה את מבנה המודל.
ממצאי המחקר
מודל התאומים הדיגיטליים המבוסס פיזיולוגית עבר הכשרה קפדנית ואושר באמצעות מגוון רחב של נתונים ניסויים שפורסמו. מסגרת מודל זו מתיישרת בהצלחה עם כל הנתונים ממערך הנתונים של האומדן באמצעות פרמטרים עקביים. יתר על כן, הוא חוזה במדויק תוצאות מנתוני אימות בלתי תלויים, מאושרים על ידי χ2-בדיקות תחת רמת ביטחון של 0.05.
מודל מכניסטי חדש זה מצטיין בייצוג דינמיקה של ריקון קיבה בתנאי ניסוי שונים. יש לציין כי מחקרים קודמים הוכיחו כי בעוד שתכולת הקלוריות משפיעה באופן משמעותי על קצב ריקון הקיבה, סוג הקלוריות לא.
המודל לוכד תופעה זו על ידי תיאור קצבי ריקון עקביים על פני סוגי קלוריות שונים אך קצבים מגוונים המבוססים על תכולת קלוריות כוללת. התנהגות ריקון קיבה זו, ללא קשר לצפיפות הקלורית, מעוצבת ביעילות, ובכך מציעה הבנה מפורטת של התהליכים הפיזיולוגיים המעורבים.
תוך כדי בחינת האינטראקציה בין ארוחות לדינמיקה של אתנול בפלזמה, המודל העריך ארבע השערות לגבי האופן שבו מזון משפיע על חילוף החומרים של אתנול. מבין אלה, רק ההשערה שאוכל עוטף אלכוהול ומשחרר אותו כשהמזון מתעכל יכולה להתאים בצורה נאותה לנתונים האמפיריים. תצפית זו משקפת הבנה מעודנת של שינויים הנגרמות על ידי ארוחה בספיגת אתנול ומטבוליזם.
היקף המודל מתרחב לתרחישים מפורטים של דינמיקה של אתנול בפלזמה בעקבות צריכת אלכוהול עם או בלי מזון. יתר על כן, הוא משקף במדויק את ההשפעה של משקאות אלכוהוליים שונים על BAC על ידי לכידת וריאציות ברמות האתנול הנגרמות על ידי נוכחות מזון. זה כולל נתונים ממחקרים המראים כיצד ארוחות יכולות לווסת את השיא וההתקדמות של BAC.
המודל מתאר גם את המסלולים המטבוליים של אתנול, כולל תהליכים חמצוניים ולא חמצוניים כאחד. תוצאות אלו היו דומות לנתונים ניסויים קודמים על פלזמה אצטט ו-PEth, שניהם סמנים חשובים לחקר השפעות צריכת אלכוהול.
יכולת חיזוי זו משתרעת על תרחישים מותאמים אישית שבהם המודל שוקל נתונים אנתרופומטריים בודדים כדי לחזות את ההשפעות של דפוסי שתייה שונים על רמות BAC ו-PEth. באמצעות פרמטרים שונים כמו מדד מסת הגוף (BMI), המודל מציע תובנות מותאמות לגבי האופן שבו הרגלי שתייה ספציפיים משפיעים באופן שונה על אנשים, ובכך משפר את היישום שלו ברפואה מותאמת אישית ובאסטרטגיות בריאות הציבור.
מסקנות
המודל שפותח במחקר הנוכחי משקף סימולציות מתקדמות בחקר אלכוהול ומשמש ככלי מרכזי לפיתוחים עתידיים ביישומי eHealth שמטרתם ניהול והבנת צריכת אלכוהול. יכולתו לשלב אינטראקציות ביולוגיות מורכבות במסגרת קוהרנטית הופכת אותו למשאב רב ערך עבור קלינאים וחוקרים המעוניינים להפחית נזקים הקשורים לאלכוהול באמצעות התערבויות ממוקדות וגישות מותאמות אישית.



