בסקירה שפורסמה לאחרונה בכתב העת רפואה ניסויית ומולקולרית, חוקרים סקרו ספרות זמינה על התפקיד והמנגנונים (מולקולריים ופתולוגיים) שבאמצעותם חוסר איזון כולסטרול במוח תורמים להפרעות ניווניות כמו מחלת אלצהיימר (AD), מחלת הנטינגטון (HD) ומחלת פרקינסון (PD).
הם סוקרים למעלה מ-80 פרסומים על מנגנונים קריטיים, כולל הפרעות בתפקוד הסינפטי, אוליגומרים של חלבון עמילואיד בטא (Aβ), צבירת חלבונים ושינויים במבנה הממברנה, והצטברות α-synuclein. הממצאים שלהם מצביעים על כך ששינוי סינתזה וחילוף חומרים של כולסטרול הם מאפיינים משותפים לרוב המחלות הנוירודגנרטיביות שנחקרו. בעוד שתרופות להורדת כולסטרול יכולות להפחית חלקית את הסיכון למחלות אלו, נדרש מחקר נוסף כדי לפתח התערבויות תרופתיות ממוקדות עתידיות נגד מצבים אלו.
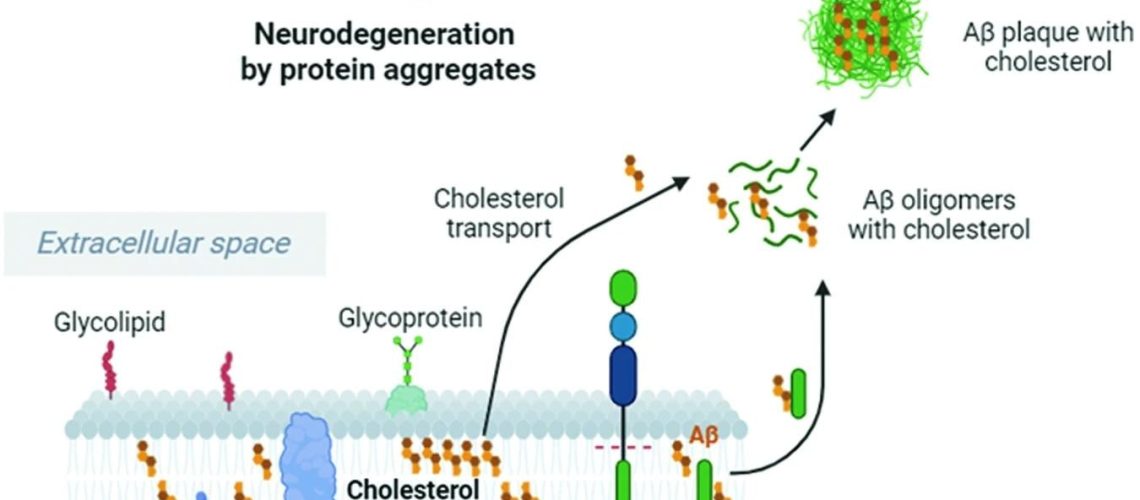
כולסטרול משפר ומאיץ את מחשוף APP על ידי Bace1, מה שמוביל להגברת אוליגומר Aβ ויצירת פלאק. כולסטרול נקשר ל-Aβ ומגביר את העמידות של סיבים ואוליגומרים של Aβ לפירוק. חוסר איזון של כולסטרול ורמות גבוהות של כולסטרול חוץ-תאי יכולים לעורר את הייצור וההצטברות של פפטידים Aβ, הגורמים להיווצרות ולהצטברות של אוליגומר Aβ במוח, וכתוצאה מכך לנזק נוירוני. תמונה זו נוצרה עם BioRender.com. מחקר: חוסר איזון כולסטרול פגמים בהולכה עצבית בניוון עצבי.
רקע כללי
כולסטרול הוא חומר שעווה דמוי שומן המצוי בקרום התא של כל תאי האדם. הוא ממלא תפקיד אינטגרלי באיתות עצבי ובחיבורים סינפטיים, במיוחד במוח. יש לציין כי המוח מכיל בין 20-25% מכל מאגרי הכולסטרול בגוף, מה שהופך אותו לאיבר עם ריכוז הכולסטרול הגבוה ביותר בגוף האדם. מעניין שכולסטרול היקפי (כולסטרול שנספג מהתזונה שמסתובבת בזרם הדם) אינו מסוגל לחצות את מחסום הדם-מוח (BBB). כתוצאה מכך, כמעט כל מאגרי הכולסטרול במוח נובעים מסינתזה דה-נובו (בגליה ובנוירונים).
ככל שבני האדם מזדקנים, היעילות של גליות ונוירונים מסינתזת כולסטרול פוחתת, מה שמפחית את מאגרי הכולסטרול במוחם וכתוצאה מכך לפגיעה בפלסטיות הסינפטית ואובדן סינפטי כולל. אובדנים אלו הוצעו כתורמים מאוד לסיכון מוגבר למחלות נוירודגנרטיביות, כולל מחלת אלצהיימר (AD), מחלת הנטינגטון (HD) ומחלת פרקינסון (PD). לרוע המזל, המנגנונים המולקולריים והפתולוגיים העומדים בבסיס התצפיות הללו נותרו לא נחקרו.
לגבי המחקר
המחקר הנוכחי מאסף וסוקר יותר מ-80 פרסומים על כולסטרול כדי להבהיר ארבעה מנגנוני מפתח מולקולריים המבססים את הקשר בין חוסר איזון של כולסטרול ותוצאות שליליות נוירודגנרטיביות שליליות. מנגנונים אלו כוללים: 1. חוסר תפקוד סינפטי, 2. צבירה עמילואיד בטא (Aβ), 3. צבירת חלבונים, שינויים במבנה הממברנה ו-4. צבירה של α-synuclein (α-syn).
מנגנונים מולקולריים
1. חוסר תפקוד סינפטי – כולסטרול נצפה כמרכיב עד 80% מממברנת הפלזמה של הסינפסות והוא חיוני הן ביצירתן ותפקודן. מחקרים הדגישו שחוסר איזון של כולסטרול יכול לשנות באופן משמעותי את יכולתן של סינפסות לשתף העברות עצביות ביעילות, ולבסוף לגרום למחלות ניווניות. מודלים מולקולריים גילו שחוסר איזון של כולסטרול משפיע לרעה על היתוך שלפוחית תלויה Ca2+, ומשנה את גמישות הממברנה. במקרים קיצוניים, זה יכול לגרום לכיפוף לא רצוי של הממברנה ולשינויים בעקמומיות, הגדלת האנרגיה הדרושה לאיחוי ממברנה/שלפוחית ופגיעה בהולכה עצבית.
2. אוליגומרים של חלבון Aβ – חלבון הקדם עמילואיד (APP) הופך לחלבון Aβ באמצעות מחשוף אנזימטי המזוזז על ידי β-secretase Bace1. בהתחשב בתפקידו האינטגרלי בצבירה וקיפול חלבונים, ההמרה המוצלחת של APP לחלבון Aβ מסתמכת על רמות כולסטרול תקינות במוח, כאשר שינויים באחר נצפו כגורמים לקיפול שגוי בראשון. קיפול שגוי של חלבון Aβ גורם ליצירת פלאקים Aβ, שהצטברותם היא סימן היכר של פתולוגיית AD. "חוסר איזון בכולסטרול ורמות חוץ-תאיות מוגברות של כולסטרול יכולים לקדם את הייצור וההצטברות של פפטידים Aβ, אשר גורמים ליצירת אוליגומרים Aβ במוח, ובכך לתרום לנזק נוירוני ולירידה קוגניטיבית". צבירה של טאו (במיוחד, hyperphosphorylated tau), סימן היכר נוסף של פתולוגיית AD, מותנית גם בריכוזי כולסטרול, בהתחשב בתכונות עקמומיות הממברנה של האחרון. מחקרים אחרונים הבהירו שממברנות נטולות כולסטרול אינן יכולות ליצור סיבים של טאו, בעוד שממברנות המכילות כולסטרול משפיעות על היווצרות סיבים של טאו תלוי בריכוז הכולסטרול ובעקמומיות הממברנה הקשורה אליו. למרבה הצער, ההשפעות של כולסטרול על גרעין טאו נותרו לא נחקרות ולא ידועות כרגע.
3. מקבץ חלבונים ומבנה הממברנה – הוכח כי כולסטרול ממלא תפקידים אינטגרליים בוויסות העקמומיות, המבנה והנזילות התקינים של הממברנה. עקמומיות ועיוות חיוניים לתפקוד שלפוחית וייצוב נקבוביות היתוך, המאפשרים התפשטות נוירוטרנסמיטר על פני מערכת העצבים המרכזית. מחקרים אחרונים גילו עוד כי כולסטרול הוא קריטי בצבירת החלבונים ובארגון התוך תאי של חלבונים מסיסים ל-N-ethylmaleimide-sensitive factor attachment receptor (SNARE). תקשורת בין חלבוני SNARE שונים (סינטקסין-1A, SNAP-25 ו-VAMP-2) מורכבת יחד את קומפלקס הליבה של SNARE, המתווך היתוך שלפוחית, ובתמורה, שחרור נוירוטרנסמיטר בתוך סינפסה.
4. צבירה של α-syn – היצירה וההתקדמות של PD מאופיינים בהצטברות של חלבוני α-syn שגויים מקופלים בגופי Lewy (LBs). היסודות המכניסטיים של תהליך זה הם תוצאה של קישור α-syn לשומני הממברנה. כולסטרול לא מאוזן מאיץ את הצטברות α-syn ויצירת LB, מה שמגביר את הסיכון ל-PD.
התערבויות טיפוליות עתידיות
משפחת החלבונים העצבים החיונית ביותר המעורבת בהובלה ובמטבוליזם תקין של כולסטרול היא משפחת האפוליפופרוטאין E (ApoE) (ApoE2, ApoE3 ו-ApoE4). ApoE4 זוהה עוד כגורם סיכון מכריע בהופעה האחרונה של AD. לרוע המזל, התרומות המולקולריות של משפחת ApoE מובנות בצורה גרועה ודורשות חקירה נוספת. עם זאת, לאור התפקיד והחשיבות של ApoE4 הן בהומאוסטזיס של כולסטרול והן בפתולוגיה של AD, הוא עשוי להיות מודגש כיעד לניסויים קליניים ולהתערבויות תרופתיות עתידיות.
מסקנות
היסודות המכניסטיים של כולסטרול על מחלות ניווניות שונות תלויות הקשר. עם זאת, המחקר הנוכחי מדגיש כיצד חוסר איזון ברמות הכולסטרול, במיוחד במוח, יכול להגביר את הסיכון למחלות אלו ומציע אסטרטגיות אפשריות לניהולן.
"בעוד שתרופות להורדת כולסטרול, כמו סטטינים, הראו פוטנציאל מסוים בהפחתת הסיכון למחלות ניווניות מסוימות, נדרש מחקר נוסף כדי להבין היטב את תפקידו של הכולסטרול ולפתח התערבויות טיפוליות ממוקדות".