לאחרונה הזדקנות הטבע המחקר מעריך את היעילות של טיפול סנוליטי המבוסס על תאי T של קולטן אנטיגן כימרי (CAR). בטיפול זה, תאי CAR T סנוליטיים מכוונים לתאים חיוביים לקולטן פלסמינוגן לאורוקינאז (uPAR), אשר מצטברים במהלך ההזדקנות.
לימוד: יעילות מניעתית וארוכת טווח של תאי CAR T סנוליטיים נגד הפרעות בתפקוד מטבולי הקשור לגיל. קרדיט תמונה: Juan Gaertner / Shutterstock.com
רקע כללי
הזדקנות תאית היא עצירה בלתי הפיכה של מחזור התא המושרה בתגובה ללחץ. בתנאי לחץ, מיוצרים אנזימים לעיצוב מטריקס וציטוקינים פרו-דלקתיים, המכונים פנוטיפ הפרשה הקשור להזדקנות (SASP).
באנשים צעירים עם מצבים פיזיולוגיים, כגון דיכוי גידול וריפוי פצעים, SASP מסייע בגיוס תאי חיסון, המקלים על שיקום רקמות ופינוי תאים מזדקנים. אצל אנשים מבוגרים, תאים מזדקנים מצטברים עקב תפקוד מופחת של מערכת החיסון ונזק גבוה יותר לרקמות.
עד כה, רוב הטיפולים הסנוילטיים כללו תרופות בעלות מולקולות קטנות הדורשות מתן חוזר ומכוונות בצורה גרועה לאזור הפגוע. באופן השוואתי, תאי CAR T דורשים אנטיגן מטרה יחיד שמתבטא בצורה דיפרנציאלית בהשוואה לרקמות רגילות. בנוסף, תאי CAR T הם 'תרופות חיות' בניהול יחיד, אשר נמשכות שנים רבות ומתווכות את השפעותיהן.
לגבי המחקר
בעבר, הוכח כי תאי CAR מתמקדים בחלבון uPAR משטח התא ומדללים ביעילות תאים מזדקנים. המחקר הנוכחי בוחן האם תאי CAR מסירים ביעילות ובבטחה תאים מזדקנים בעכברים מבוגרים, ובכך מווסתים את תוחלת הבריאות.
עכברים משני המינים, 8-12 שבועות ו-18-20 חודשים, נכללו במחקר. הם הוחזקו בדיור קבוצתי ובתנאים ללא פתוגנים.
נעשה שימוש במחזור אור/חושך של 12 שעות ותנאי הטמפרטורה והלחות היו סטנדרטיים. עכברים מזדקנים צרכו דיאטה רגילה, בעוד שתת-קבוצה של עכברים צרכה דיאטה עתירת שומן (HFD).
לצורך ניתוח ציטומטריית זרימה, הכבדים נותקו וסוננו, ולאחר מכן התמזגו תאי דם אדומים. בוצע ריצוף של חומצה ריבונוקלאית חד-תאית (RNA), ולאחר מכן הרחבה, בידוד והתמרה של תאי T של עכבר. נערכו מדידות דם מלאות ובוצעה ניתוח שלאחר המוות של מספר איברים.
ממצאי מפתח
הוכח כי טיפולים בתאים סנוליטיים מקלים על תסמינים הקשורים להזדקנות פיזיולוגית, כולל הפרעות בתפקוד מטבולי. לשם כך, שיעור התאים החיוביים ל-uPAR עולה לעתים קרובות ככל שהגיל מתקדם; לכן, תאים חיסוניים וגם תאים שאינם חיסוניים ל-uPAR חיוביים עשויים להקל על נטל ההזדקנות ברקמות מיושנות.
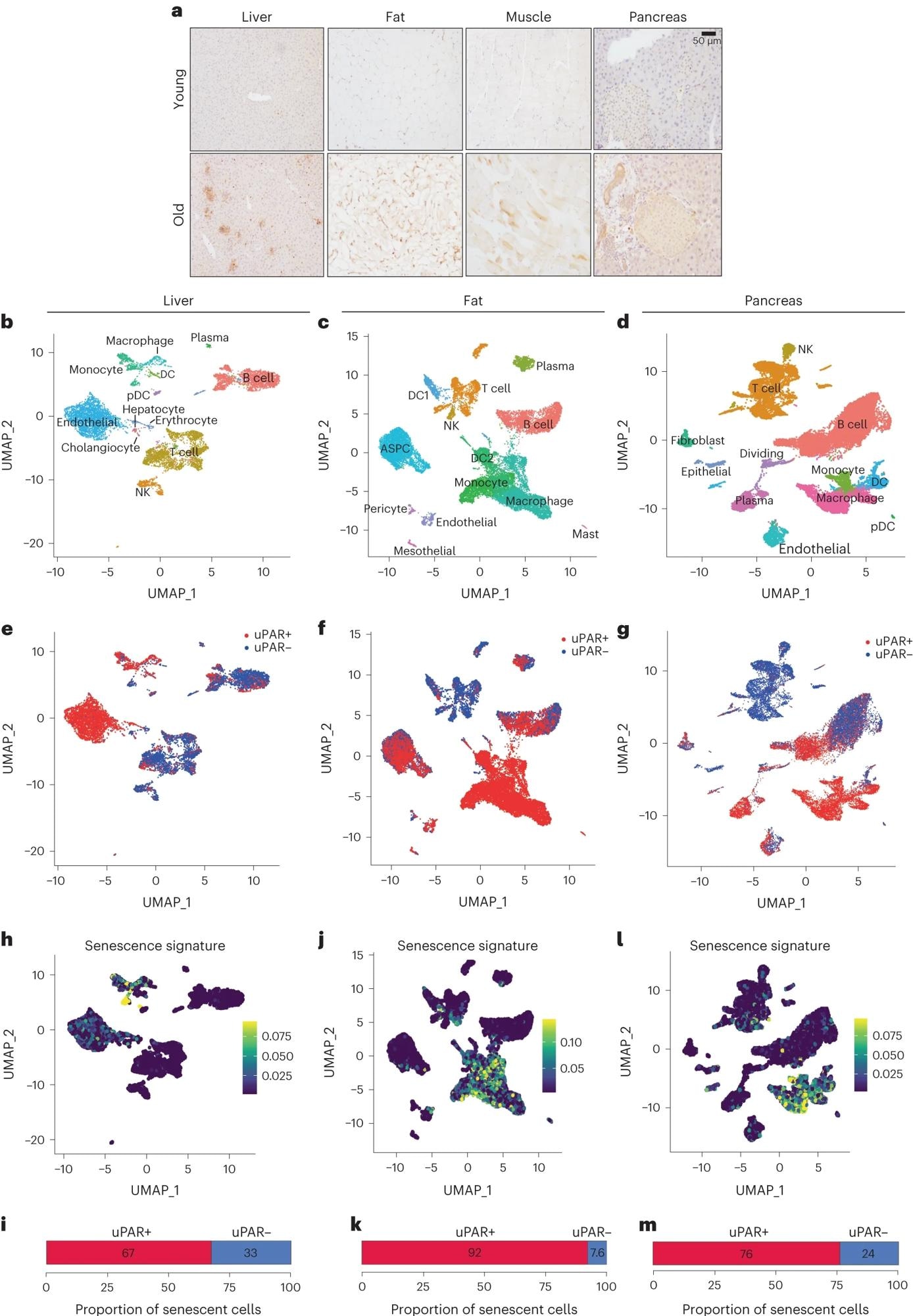
אצביעה אימונוהיסטוכימית של uPAR עכבר בכבד, רקמת שומן, שריר ולבלב מעכברים צעירים (גיל 3 חודשים) או מבוגרים (גיל 20 חודשים) (n = 3 לגיל). ב–M, ניתוח תא בודד של ביטוי uPAR והזדקנות. תאים חיוביים ל-uPAR ותאים שליליים ל-uPAR מוינו מהכבד, רקמת השומן והלבלב של עכברים בני 20 חודשים ועברו ל-RNA-seq של תא יחיד לפי פרוטוקול כרום פי 10 (n = רצף של ארבעה עכברים שבהם שתי נקבות היו אוחדו לשכפול אחד ושני זכרים שולבו לשכפול אחר). בהדמיה של קירוב והקרנה סעפת אחידה (UMAP) של סוגי תאי כבד. גהדמיית UMAP של סוגי תאי רקמת שומן. דהדמיית UMAP של סוגי תאי לבלב. ההדמיית UMAP של סוגי תאים uPAR שליליים ו-uPAR חיוביים בכבד. והדמיית UMAP של סוגי תאים בעלי uPAR שלילי ו-uPAR חיובי. זהדמיית UMAP של סוגי תאים שליליים ו-uPAR חיוביים של הלבלב. ח,י,להדמיות UMAP עם ציוני חתימת הזדקנות24 בכל תא המצוין בסולם הצבעים. אני,ק,Mכימות של השיעור של תאים חיוביים ל-uPAR ו-uPAR שליליים התורמים לחתימת ההזדקנות המתאימה. ח,אניכבד ; י,קרקמת שומן; ל,M, לבלב. התוצאות הן מניסוי אחד עצמאי (א–M). DC, תא דנדריטי; NK, רוצח טבעי; pDC, plasmacytoid dendritic cell; ASPC, אבות שומן ותאי גזע.
היעילות של תאי T uPAR CAR בהסרת תאי מזדקן חיוביים ל-uPAR הודגשה גם היא. לשם כך, היעילות של תאי T uPAR CAR אינה קשורה לפתולוגיה של רקמות או לשינויים בפרמטרים הכלייתיים והכבדיים בעכברים מבוגרים.
פעולתם של תאי T uPAR CAR נמצאה קשורה לכושר מטבולי ולהומאוסטזיס גלוקוז מוגבר בעכברים מזדקנים רגילים ובעכברים שניזונים HFD. חשוב לציין, לא נצפתה רעילות לאחר מתן תאי uPAR CAR T במינונים מומלצים.
הפוטנציאל של תאי T uPAR CAR לפעול באופן מניעתי כדי להפחית את הירידה המטבולית הקשורה לתזונה וקשורה לגיל הייתה תצפית בולטת נוספת. יתרה מכך, לתאי UPAR CAR השפעות ארוכות טווח על שיטות סנוליטיות המבוססות על מולקולות קטנות. לאחר מתן יחיד, תאים אלה פגעו בתסמונת המטבולית הקשורה ל-HFD או הנגרמת על ידי גיל בעכברים שקיבלו HFD או כאלה שטופלו במהלך הנעורים.
ביחס לסבילות לגלוקוז, מחקרים סנוליטיים זיהו הסרה של תאי בטא בלבלב מזדקנים. עם זאת, הזדקנות תאי חיסון יכולה הייתה למלא גם תפקיד.
חיסול מקרופאגים עם מאפיינים מזדקנים הוצע גם כדי להקל על ירידת רקמות בעכברים. זה עולה בקנה אחד עם תצפיות המחקר, שבהן חלק ממקרופאגים המבטאים uPAR מבטאים יחד חתימות שעתוק הקשורות להזדקנות ול-β-galactosidase (SA-β-gal) הקשורים להזדקנות.
מסקנות
מנגנון הפעולה של מולקולות קטנות לרוב אינו מובן היטב; עם זאת, לתאי CAR סנוליטיים יש מנגנון בסיסי ברור עקב ביטוי של אנטיגנים ספציפיים על פני השטח. גישה זו קשורה ליתרונות רבים בהשוואה לגישות חיסון או מולקולות קטנות, שכן טיפולים סלולריים מווסתים את ההתמדה באמצעות עיצובי CAR מגוונים ומצוידים במתגי בטיחות מסוימים.
בעתיד, טיפול תאי יכול למקד את האנטיגנים הללו לטיפול בפנוטיפים שונים. העמידות של ההשפעות וההתמדה של תאי CAR T ממוקדי uPAR לאחר מתן יחיד מבשרת טובות עבור הגישה הסנוליטית של תאי T CAR לטיפול בפתולוגיות כרוניות.