מחקר פורץ דרך מגלה כיצד גרסת גנים בודדת מעצבת את הנוף החיסוני של המוח והדם, ומפתיחה הזדמנויות חדשות לגילוי והתערבות מוקדמת ברחבי אלצהיימר, פרקינסון והפרעות עצביות אחרות.
מחקר: נושאי APOE ε4 חולקים שינויים פרוטאומיים הקשורים לחיסון על מחלות ניווניות. קרדיט תמונה: אנדריי וודולאשסקי / Shutterstock
במחקר שפורסם לאחרונה בכתב העת רפואת טבעהחוקרים זיהו חתימה חיסונית שמור הקשורה לגרסת אפוליפופרוטאין E ε4 (Apoe ε4) על פני נוזל מוחי (CSF), מוח ופלזמה, ללא קשר לנוכחות מחלה נוירו -ניוונית.
THE Apoe ε4 הגן הוא גורם הסיכון הגנטי המשמעותי ביותר למחלת אלצהיימר מאוחרת (AD). עם זאת, ראיות מתגברות מצביעות על Apoe ε4 הובלה עשויה למלא תפקיד במחלות עצביות אחרות. Apoe ε4 נקשר לגיל נמוך יותר של הופעה ולסיכון גבוה יותר למחלת פרקינסון (PD), טרשת רוחבית אמיוטרופית (ALS) ודמנציה פרונטוטפורלית (FTD). Apoe ε4 נקשר גם לקוגניציה לקויה ולירידה קוגניטיבית מהירה יותר ב- PD, והעלאת סיכון של דמנציה PD (PDD).
לַמרוֹת ApoE ε4 השפעה מזיקת, מעט מאוד ידוע על המנגנונים הביולוגיים שלה ועל האם וכיצד הוא משתנה במחלות ניווניות. העיתון ממסגר זאת במסגרת התפיסה האבולוציונית של "פליוטרופיה אנטגוניסטית", מה שמרמז כי ההשפעות הפרו-דלקתיות של הגן עשויות להועיל כנגד מחלות זיהומיות בקרב בני נוער אך מזיקים לגיל. בעבר, המחברים דיווחו על כך Apoe ε4 ספקים חלקו חתימה פרוטאומית פרו-דלקתית ב- CSF ללא קשר למצב הקוגניטיבי בלקות קוגניטיבית קלה ו- AD. האם זה חל על מחלות ניווניות אחרות שנותרו לא ידועות.
המחקר והממצאים
המחקר הנוכחי בדק שינויים פרוטאומיים מערכתיים ב Apoe ε4 נשאים עם מחלות ניווניות. ראשית, נתונים פרוטאומיים סומסקניים ממסד הנתונים העולמי של פרוטאומיקה נוירו-התנצלות עצבית (GNPC), המשקף את ההטרוגניות הקלינית בעולם האמיתי, שימשו לפרופיל הפרוטאום של CSF של אנשים עם מצב AD, PD או שליטה (לא-מזויף). באמצעות מידע הדדי, 229 חלבוני CSF הקשורים ל- Apoe ε4 זוהו בפקדים שאינם לקוי.
דגמי עצי סיווג ורגרסיה (CART) הראו כי 229 חלבונים אלה יכולים להבדיל Apoe ε4 נשאים מלהיות נשאים ברחבי PD ו- AD. ניתוח העשרה פונקציונלי של CSF Apoe ε4 חלבונים הצביעו על העשרה משמעותית לאפופטוזיס, תהליכים ויראליים, קיפול חלבון וזרחן, תהליכי RNA/DNA, תהליכים סלולריים וקצביות.
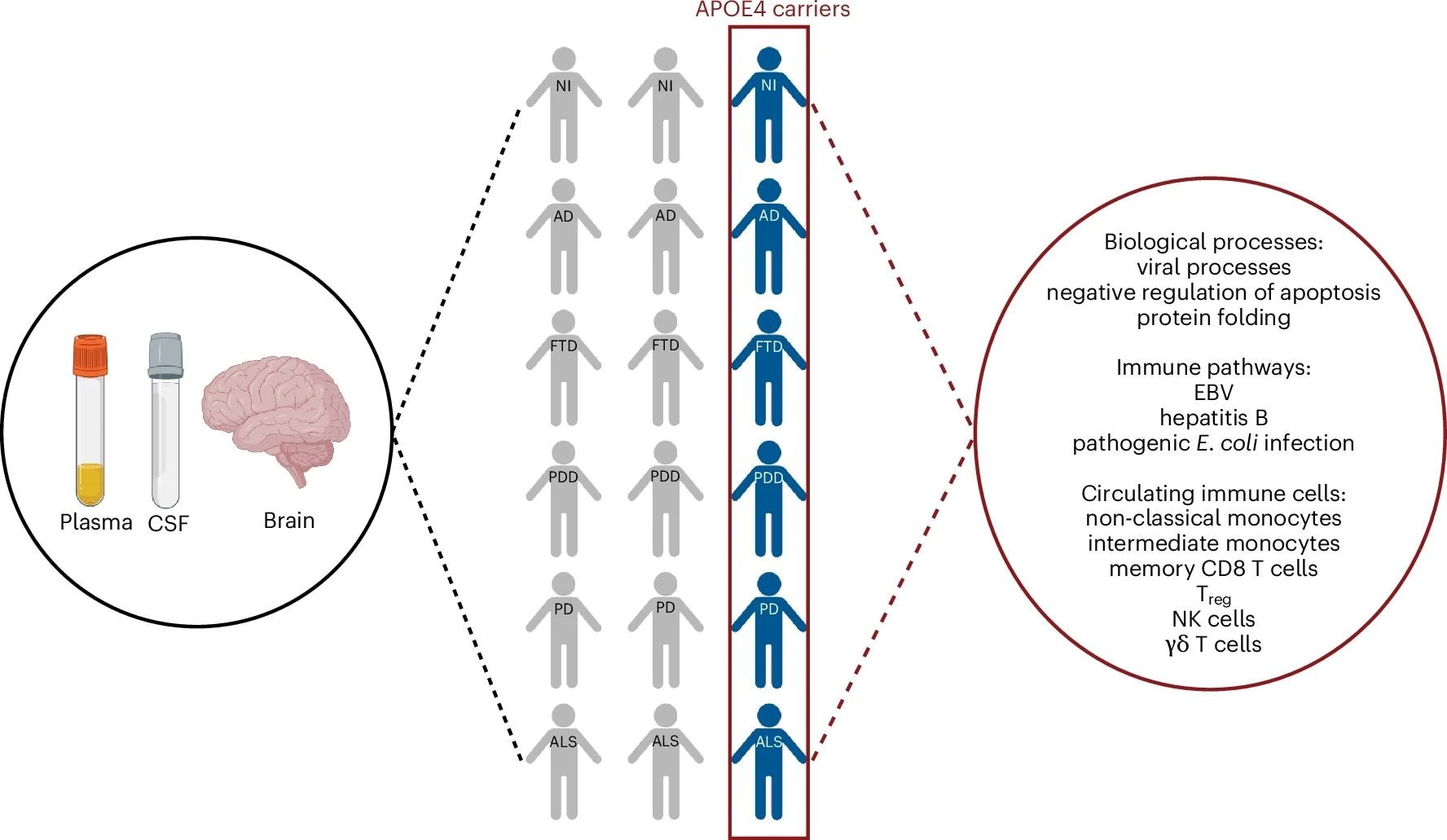 נשאי APOE ε4 על פני מחלות נוירו-ניווניות שונות חולקות שינוי פרוטאומי מערכתי נפוץ המשקף את ההפרעה החיסונית הפרו-דלקתית. הדמות נוצרת עם Biorender.comו
נשאי APOE ε4 על פני מחלות נוירו-ניווניות שונות חולקות שינוי פרוטאומי מערכתי נפוץ המשקף את ההפרעה החיסונית הפרו-דלקתית. הדמות נוצרת עם Biorender.comו
ניתוח נוסף לתהליכים ספציפיים לחיסון שנחשף Apoe ε4 העשרה בנתיבים שונים הקשורים לזיהום, כולל הרפס, שפעת A, דלקת כבד, חצבת ונגיף אפשטיין-באר (EBV). העשרה משמעותית נצפתה גם עבור מפל תאי B, תאי T ואיתות דלקתית. בשלב הבא, ניתוח העשרה תת -תאי חיסוני חשף הכי הרבה Apoe ε4 העשרה במונוציטים ביניים ולא קלאסיים בקרב תאי חיסון מולדים.
בין תאי חיסון אדפטיביים, אשכול זיכרון של בידול 8 (CD8) תאי T, תאי T (TREG) ותאי CD4 T של הזיכרון היו המועשרים ביותר. חוץ מזה, תאי t γδ ותאי רוצח טבעי (NK) הראו Apoe ε4 הַעֲשָׁרָה. בכבד, ניתוח העשרה ספציפי לתאים חשף הכי הרבה Apoe ε4 העשרה בתאי קופפר והפטוציטים.
בשלב הבא החוקרים בדקו אם Apoe ε4 שינויים בפרוטאום של CSF באו לידי ביטוי בפלזמה והשתמשו במערך הנתונים של GNPC לפרופיל פרוטאום פלזמה של בקרות AD, PDD, FTD, PD, ALS ובקרות שאינן מקומות. חמישים ושמונה חלבוני פלזמה הקשורים ל- Apoe גנוטיפ זוהו בבקרות שאינן לקוי. דוגמנות עגלה חשפה כי 58 חלבונים אלה יכולים להבדיל מאוד בין Apoe ε4 נשאים ואינם נשאים על מחלות ניווניות, וחתימה זו נמצאה עקבית בין מינים וקבוצות גזעיות שונות.
Apoe ε4 תהליכי פלזמה הראו העשרה משמעותית בתהליכים ביולוגיים, כולל תהליכי חלבון, תהליכים סלולריים, תהליכים ויראליים, תהליכי DNA/RNA ואפופטוזיס. תהליכים ויראליים היו המועשרים ביותר הן בפלזמה והן ב- CSF. זה נתמך על ידי העשרות דומות בזיהום ובמסלולי חיסון, כולל דלקת כבד ו- EBV. מונוציטים ובזופילים ביניים ולא קלאסיים הועשרו Apoe ε4 חלבונים בין תאי חיסון מולדים.
תאי NK, תאי T T, תאי CD8 T של זיכרון ותאי CD8 T נאיביים הועשרו עבור Apoe ε4 חלבונים בין תאי חיסון אדפטיביים. בכבד תאי T ותאי קופפר הועשרו בעיקר, ואילו הפטוציטים הראו העשרה מועטה. נתונים אלה מצביעים על כך ששינויים פרוטאומיים ספציפיים לגנוטיפ שהתגלו ב- CSF באו לידי ביטוי גם בפלזמה ב- Apoe ε4 נשאים ולא נשאים.
יתר על כן, הצוות בדק האם שינויים פרוטאומיים היקפיים השתקפו במוחם של Apoe ε4 נשאים ולא נשאים. לשם כך הם השתמשו בנתונים הפרוטאומיים של קליפת המוח הקדמית הדורסולטרלית (DLPFC) מאנשים עם AD, FTD, PD, PDD, ALS, ואנשים שאינם מקובלים, כחלק ממחקר הפרוטאומיקה של AD (AMP-AD). באמצעות מידע הדדי, 248 Apoe ε4 חלבונים זוהו ב- DLPFC.
ניתוחי העשרה פונקציונליים הראו כי שלושת התהליכים הביולוגיים העיקריים (תהליכים ויראליים, אפופטוזיס וקיפול חלבון) שזוהו בפלזמה וב- CSF הועשרו באופן משמעותי גם ב- DLPFC של Apoe ε4 נשאים על מחלות ניווניות. זוהו גם ארבעה מהמסלולים החיסוניים המועשרים באופן משמעותי ביותר בפלזמה ו- CSF Apoe ε4 נשאים מחלות-באופן בלתי תלוי: הפטיטיס B, EBV, Escherichia coli זיהום וסרטן ויראלי. באופן חיוני, המחקר מצא כי חתימת מוח זו לא הייתה תלויה בפתולוגיות הניווניות הנוירו-ניווניות, כולל עמילואיד-β, TAU, TDP-43 ו- α-synuclein, ומחזקת את זה Apoe ε4 ההשפעה היא פגיעות בסיסית ולא תוצאה ישירה של צבירת חלבון ספציפית למחלות.
ממצא בלתי צפוי מאתגר סמן ביולוגי מפתח
בממצא בולט ו"ממצא בלתי צפוי ", המחקר חשף כי רמות האור הנוירופילמנט בפלזמה (NEFL), סמן ביולוגי בשימוש נרחב של התנוונות עצבית, היו נמוכים בעקביות ב- Apoe ε4 נשאים. הכותבים מציינים כי הדבר סותר כמה מחקרים קודמים ו"עלים שאלות חשובות לגבי אמינות ה- NEFL כסמן ביולוגי עצמאי ", מה שמצביע על רמותיו להשפיע על ידי רמותיו Apoe ε4גורמים מטבוליים הקשורים או מרווח על מחסום הדם-מוח.
לבסוף, בוצע ניתוח רשת מתאם כדי לחקור את הקשר בין Apoe ε4 חלבונים וגורמים קליניים, דמוגרפיים ואורח חיים ב- PDD, PD, AD ולא לקויי Apoe ε4 נשאים. הם זיהו קשרים ספציפיים למחלות עם APOE במחלות ניווניות. APOE היה קשור לגזע ומין ב- AD, סוכרת ב- PD, גיל, יתר לחץ דם ומדד מסת גוף בביקורות שאינן מקומות, ומחלות ריאות חסימתיות כרוניות ומנוחה דופק במנוחה ב- PDD. עם זאת, הכותבים מזהירים כי מכיוון שהמחקר הוא חתך רוחבי, הם "אינם יכולים להסיק סיבתיות", מכיוון שגורמים קליניים אלה יכולים להיות תוצאה של המחלה הנוירו-ניוונית ולא סיבה.
מסקנות
הממצאים הראו זאת Apoe ε4 ספקים חולקים חתימה פרוטאומית ייחודית על פני הפלזמה, CSF ומוח, ללא קשר למחלה ניוונית. חתימה זו הייתה קשורה להעשרה לצורך סיבוב תאי חיסון והפרעת חיסונית פרו-דלקתית. הכותבים מציעים מנגנון ספציפי לכך, ומציעים כי תאי חיסון היקפיים היפראקטיביים עשויים לקיים אינטראקציה ולשבש את מחסום הדם-מוח (BBB) ובכך להניע דלקת נוירו. עם זאת, חלבונים בחתימה זו היו בקורלציה ייחודית עם גורמים קליניים, דמוגרפיים ואורח חיים באופן ספציפי למחלות עצביות.
זה מצביע על כך Apoe ε4 מעניקה פגיעות ביולוגית מערכתית שהיא חיונית אך אינה מספיקה להתנוונות עצבית, ומדגישה את הצורך להסביר אינטראקציות בין גנים-סביבתית. המחברים מודים גם במגבלות, כולל "היעדרם של סמנים ביולוגיים מאומתים" כדי לאשר את כל האבחנות הקליניות ו"היעדר מדדים ישירים של סמנים דלקתיים שגרתיים כמו חלבון תגובתי C ", אשר יש לטפל בהם במחקרים עתידיים.
בסך הכל, התוצאות רעננות Apoe ε4 כמודולטור חיסוני פליוטרופי, ולא כגן סיכון ספציפי לספציפיות, ומספק בסיס לאסטרטגיות התערבות מוקדמות והתפתחות דיוקתית של סמן ביולוגי על פני מחלות ניווניות. המחקר מסכם בקריאה לשינוי רעיוני בתחום, עובר פשוט מזיהוי לוקוסים של סיכון גנטי "לקראת אפיון פונקציונלי של גרסאות מבוססות", וביסוס מפת דרכים למחקר עתידי על אינטראקציות מורכבות אלה.