מגוון העור למוטציות נדירות, מדענים חושפים כיצד הגנים שלך משפיעים על רמות ויטמין D, ומדוע תוספי מזון סטנדרטיים עשויים שלא לעבוד זהים עבור כולם.
סקירה: גרסאות גנטיות המשפיעות על מצב ויטמין D אינדיבידואלי. קרדיט תמונה: Zerbor / Shutterstock
במחקר שפורסם לאחרונה בכתב העת חומרים מזיניםחוקרים בקנדה סקרו את המנגנונים הגנטיים התורמים לשונות אינדיבידואלית ברמות ויטמין D (VD) במחזור הדם.
בני אדם יכולים לסנתז ביעילות את VD, הדורש חשיפה לקרינה Ultraviolet B (UVB) בצורה של אור שמש. עם זאת, ברוחב הרוחב הדרומי והצפוני המרוחק לקו המשווה, אור השמש וטמפרטורת העור אינם מספקים לסינתזה של cholecalciferol (VD3) במשך מספר חודשים של השנה. כיוון שכך, הדבר עלול לגרום למחסור ב- VD ולתוצאות בריאותיות שליליות בהיעדר מקורות תזונתיים.
מחקרים מראים כי רמות קלצידיול (רמות מטבוליט VD עיקריות) של 60 ng/ml עשויות להיות קשורות לסיכון נמוך יותר לתנאים בריאותיים מסוימים. עם זאת, סטטוס ה- VD האופטימלי מתלבט, והספים המוצעים משתנים בין מחקרים וקבוצות מומחים. חשוב לציין כי מרבית הספים נגזרים מקבוצות אירופאיות, ויישומם על פני אבות אבות נותר מתלבט. מלבד גורמים תזונתיים ועונתיים, גנטיקה תורמת לשונות אינדיבידואלית ב- VD. אינטראקציות בין גנים אחר-סביבה, כולל גוון עור ורוחב רוחב, עשויות גם להשפיע על תוצאות אלה. כיוון שכך, המחקר הנוכחי סקר את הגרסאות הגנטיות המשפיעות על מצב VD אינדיבידואלי.
סינתזת VD, ויסות ומטבוליזם
ניתן לרכוש VD מתזונה, תוספי מזון וסינתזה אנדוגנית. בדרך כלל הוא נצרך כ- VD3 מתוספי תזונה ומזונות מבוססי בעלי חיים ו- Ergocalciferol (VD2) ממזון על בסיס צמחי. VD מיוצר באופן אנדוגני בבני אדם בתנאים אידיאליים. חשיפה לעור לאור UVB מובילה להמרה של 7-dehydrocholesterol (7-DHC) ל- Pre-VD3, שאחרי איזומריזציה תרמית מייצרת VD3.
יתר על כן, הקרנת UVB ממירה טרום VD3 ל- Tachysterol ו- Lumisterol, ו- VD3 לסופרסטרולים לא פעילים. זה מאפשר ויסות VD בעור ומונע רעילות. נוכחותם של שומנים משפרת את ספיגת ה- VD. הפרשת ליפאז קיבה נדרשת להדרוליזת VD מועברת על ספיגתו. לאחר מכן, ליפאזים בלבלב וחומצות מרה במעי הדק מקדמים היווצרות של מיקרונים הממיסים VD.
לאחר הספיגה, VD נארז ומועבר לווריד הפורטל או בעקיפין דרך מערכת הלימפה לדם. במחזור, VD3 נקשר להובלת חלבונים הנושאים אותו לכבד. חלבון מחייב VD (DBP) מהווה את מרבית הובלת ה- VD (85%) בגלל זיקה מחייבת גבוהה, ואילו אלבומין מעביר כ- 15% מ- VD, ומשאירים כ- 0.4% VD בחינם במחזור.
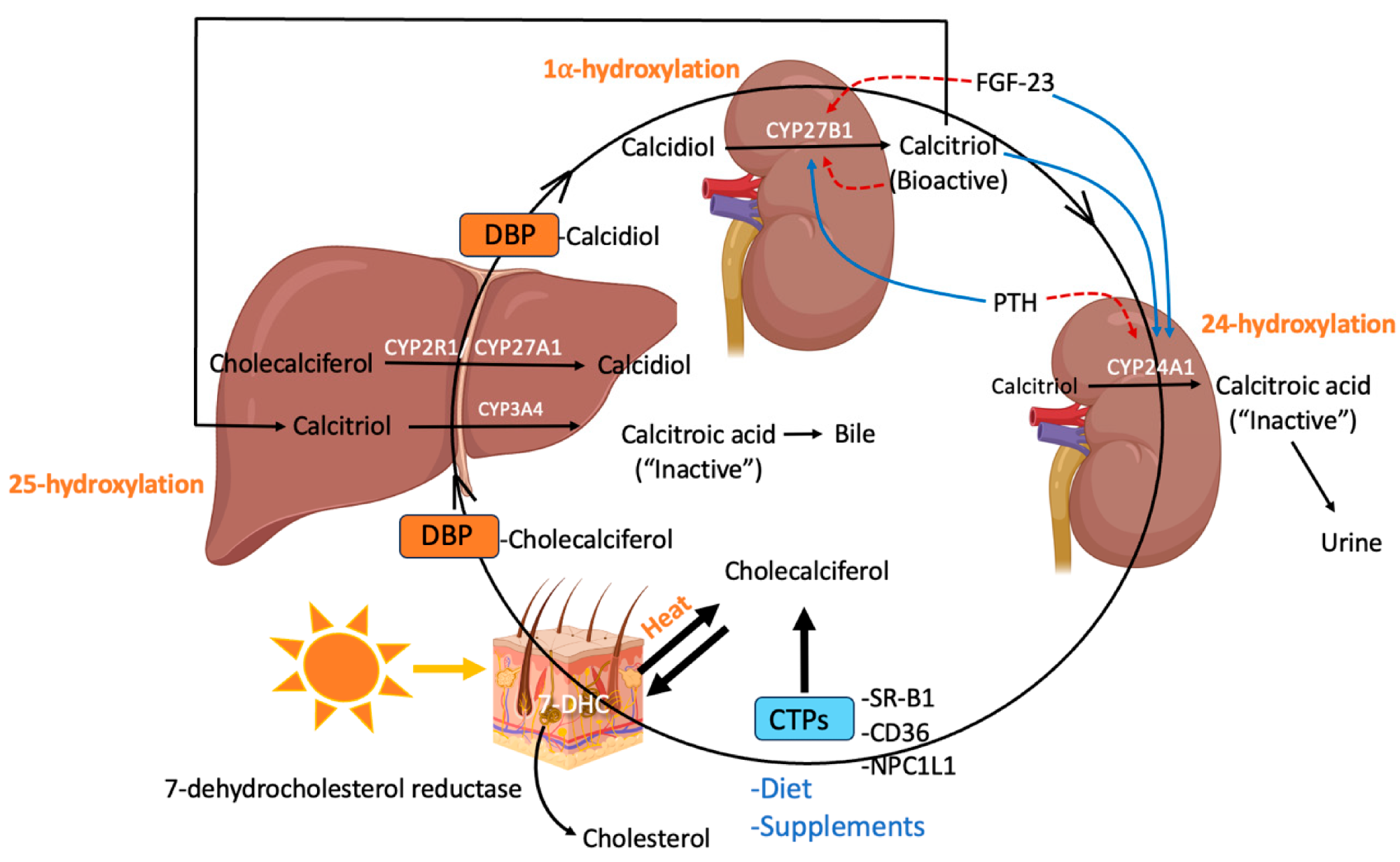 סינתזה, הובלה ומטבוליזם של ויטמין D בכל הגוף (נוצר באמצעות ביורנדר): 7-dehydrocholesterol (7-DHC), חלבונים מחייבים כולסטרול (CTPS), קולטן חפצים מסוג B (SR-BI), Niemann-Pick C1 Like 1 (NPC1L1), DOGINDO CORTINGO PRATINO CORTINGO (DBSINGRO CORDINSIN, DBSINGRO) (DBPRO) (DBPRO 1) (DBSINGRO) (DBPRO1) (DBPRO1) (DBPRO1) (DBPRO1) (DBPRO1). (FGF) -23 (FGF-23), הורמון פרתירואידי (PTH).
סינתזה, הובלה ומטבוליזם של ויטמין D בכל הגוף (נוצר באמצעות ביורנדר): 7-dehydrocholesterol (7-DHC), חלבונים מחייבים כולסטרול (CTPS), קולטן חפצים מסוג B (SR-BI), Niemann-Pick C1 Like 1 (NPC1L1), DOGINDO CORTINGO PRATINO CORTINGO (DBSINGRO CORDINSIN, DBSINGRO) (DBPRO) (DBPRO 1) (DBSINGRO) (DBPRO1) (DBPRO1) (DBPRO1) (DBPRO1) (DBPRO1). (FGF) -23 (FGF-23), הורמון פרתירואידי (PTH).
גרסאות גנטיות המשפיעות על מצב VD
מחקרי אסוציאציה רחבי גנום (GWASS) ומחקרי איגוד הגנים של המועמדים (CGASS) חקרו פולימורפיזם בגן VD (VDR) הקשורים לבריאות שאינם שלד ושלד. עם זאת, מידע על הקשר עם גנים הקשורים לסינתזת VD, חילוף חומרים ותחבורה חסר. GWASS דיווחו על אסוציאציות עם פולימורפיזמות חד-נוקלאוטידים (SNPs) ברדוקטאז 7-DHC (DHCR7) ורמות VD.
מספר מוטציות של DHCR7 המפחיתות את ביטויו במהלך התפתחות העובר אחראיות למחלה רצסיבית אוטוזומלית נדירה, תסמונת סמית-למלי-אופיץ. מוטציות של אובדן פונקציה בשתי האללים של DHCR7 (מוטציות מסגרות דו-אלליות) גורמות לפגיעה בביוסינתזה של כולסטרול. SNPs נפוצים ב- DHCR7, כגון RS12785878, קשורים ל- VD בסרום נמוך יותר והם נפוצים יותר באוכלוסיות הצפון, מה שמרמז על הסתגלות אבולוציונית פוטנציאלית לרוחב רוחב. בהקשר של סינתזת VD, רמות DHCR7 פונקציונליות נמוכות יותר יפחיתו את המרת 7-DHC לכולסטרול, מה שמגדיל את הזמינות של 7-DHC לסינתזת VD.
הגן GC מקודד DBP, הטרנספורטר העיקרי של מטבוליטים VD. שני SNPs Missense מגדירים את האיזופורמים הנפוצים של GC: GC1S, GC2 ו- GC1F, השונים בזיקה מחייבת VD וריכוז DBP. האלל GC1F נקשר לרמות סרום נמוכות יותר של קלצידיול והגברת הסיכון להיפוביטמינוזיס D אצל תינוקות.
אף על פי שאינו נחקר היטב כמו GC, הוצעו מספר חלבוני הובלה מועמדים (CTP) להשפיע על ספיגת והפצת VD. חלבוני כולסטרול-טרנספורט (CTPS) הובלת VD, ויטמין K, α-tocopherol, וקרוטנואידים, בין היתר, בכל הגוף. מחקר מצא כי עכברים חסרי CTP, קולטן נבלות מסוג B 1 (SCARB1), היו בעלי רמות גבוהות של VD3 בסרום, לב, רקמת שומן ובכליות, אך הפחיתו את הרמות של קלצידיול מדויב בכליות, סרום וכבד. אמנם חסרות קשרים ישירים בין גרסאות CTP אנושיות לבין קלצידיול בסרום, אך השפעות מבוססות על הובלת ויטמינים אחרים המסיסים בשומן מעידים כי מעורבותם מתקבלת על הדעת. מחקר מתפתח מדגיש גם תפקידי תחבורה דומים עבור CD36 ו- NPC1L1, אם כי יש צורך בראיות נוספות כדי לאשר את תרומתם למצב VD. בסך הכל, בעוד שתפקידם של CTPs בוויסות VD נותר מתקבל על הדעת, נדרש אימות נוסף במחקרי אדם.
Cytochrome P450 Family 2 Subfamily R חבר 1 (CYP2R1) אחראי על ההידרוקסילציה של VD3 ל- calcidiol. GWASS ו- CGASS שונים חשפו אסוציאציות בין SNPs במצב CYP2R1 ו- VD. מחקר דיווח כי 21 פולימורפיזמות שאינן שם נרדמות ב- CYP2R1 ירידו בפעילות CYP2R1, בעוד ששני SNPs הגדילו את הפעילות. על פי הדיווחים, אלל סיכון, RS10741657, ב- CYP2R1 היה קשור לסבירות גבוהה יותר לאי ספיקת VD.
יתר על כן, CYP27B1 מהווה את ההידרוקסילציה של קלצידיול לקלציטריול. SNPs ב- CYP27B1 נקשרו לרמות VD במחזור. לדוגמה, RS4646536, SNP אינטרוני ב- CYP27B1, נקשר לסיכון של מחסור ב- VD. חוץ מזה, מוטציות אובדן פונקציה ב- CYP27B1 גורמות לריקטטים תלויים VD מסוג 1A (VDDR1A). לחולי VDDR1A עם מוטציות של אובדן פונקציה דו-אלומי ב- CYP27B1 יש קלציטריול בלתי ניתן לגילוי או נמוך, הדורשים תוסף קלציטריול לאורך החיים.
CYP24A1 אחראי על הפעלת קלציטריול. SNPs שונים ב- CYP24A1 נקשרו לריכוזי VD. מחקר על בקרת מקרה דיווח כי גנוטיפים ספציפיים ל- CYP24A1 SNP (Intronic RS2585428 ו- RS4809960) היו קשורים לסיכון למחסור ב- VD. מחקר אחר מצא כי CYP24A1 SNP, RS172167070, היה קשור לרמות קלצידיול ומצב מגיב VD באוכלוסייה לילדים עם סיסטיק פיברוזיס. מוטציות של אובדן פונקציה נדירות של CYP24A1 עשויות לבסס רגישות יתר לתוסף VD, מה שמצביע על תפקיד לבדיקה גנטית בתרחישים קליניים ספציפיים.
בנוסף, הסקירה דנה בשני גנים אחרים שלא טופלו בדרך כלל במחקרים קודמים: CYP11A1, המייצר מטבוליטים ויטמין D ביו -אקטיביים, במיוחד בעור. CYP3A4, אנזים כבד המעורב בהפעלה של קלצידיול וגם של קלציטריול, שם נקשר מוטציה נדירה של תפקוד לתפקוד אצל ילדים.
הערות מסכמות
סטטוס VD הוא תכונה פוליגנית המושפעת מפולימורפיזם בגנים המסדירים את הסינתזה, חילוף החומרים וההובלה שלה, ומוטציות נדירות שיכולות לשנות את חילוף החומרים VD. גרסאות בקולטן ויטמין D (VDR) עשויות גם להשפיע בעקיפין על רמות המסתובבות באמצעות מנגנוני ויסות גנים. גורמים גנטיים אלה, כמו גם וריאציה עונתית, פירושם כי לא תמיד ניתן להשיג רמות VD מספיקות באמצעות המלצות תזונתיות סטנדרטיות. הבנת ההשפעות המצטברות של הסביבה, הגנטיקה והאינטראקציות בין גנים-סביבתיות נחוצה כדי לפתח המלצות מדויקות.
הסקירה מדגישה גם השלכות קליניות. ציוני סיכון גנטי של ויטמין D (GRSS) עשויים בסופו של דבר לסייע בזיהוי אנשים הנמצאים בסיכון למחסור או רעילות, מה שמאפשר אסטרטגיות תוספות מותאמות יותר. עם זאת, כלים אלה דורשים אימות נוסף באוכלוסיות מגוונות. בפרקטיקה הקלינית, גישה מונעת פנוטיפ נותרה הכי אפשרית, אם כי שיטות מתעוררות, כמו אתגרי cholecalciferol במינון גבוה, יכולות להעריך את הזמינות הביולוגית האישית ואת התגובה המטבולית.



