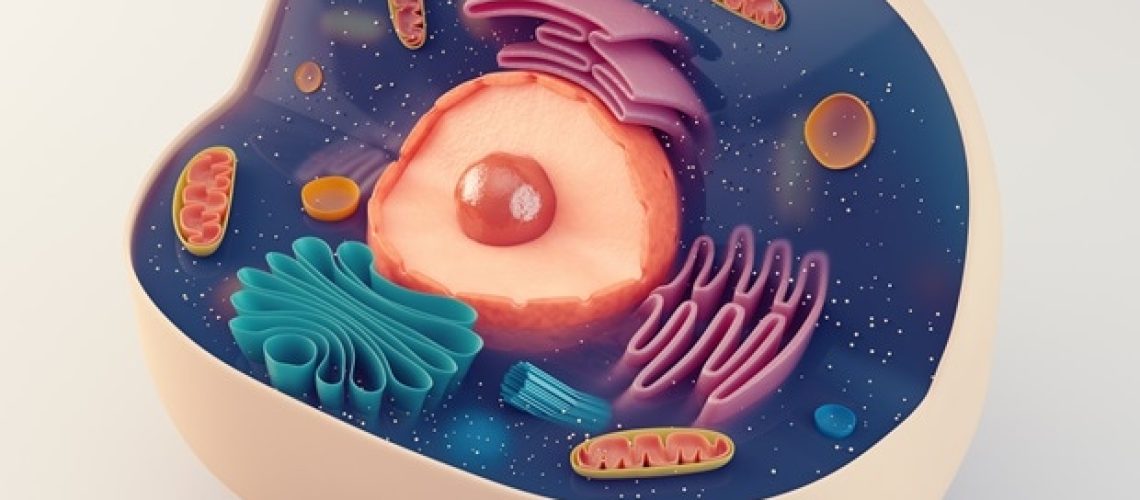
יש שיגידו שזה נראה כמו אצבע. אחרים עשויים לראות תולעת. מדענים בתחום משווים אותה לעתים קרובות לאנטנה. השם הטכני הוא סיליום ראשוני. הנספח הדק והמיקרוסקופי הזה מוציא את פני השטח של מרבית התאים בגוף האדם – ובכל זאת במשך שנים רבות הוא היה חסר לחלוטין באיורים של ספרי לימוד.
מדענים החלו להקדיש תשומת לב רבה יותר לסיליה הראשונית בסביבות שנת 2003. זה כאשר מדען במרכז הסרטן הזיכרון לסלואן קטרינג (MSK), קתרין אנדרסון המנוח, PHD, גילה כי סיליה ראשונית ממלאת תפקיד חשוב מאוד בהתפתחות העובר: הם מעבדים אותות ממשפחה של חלבונים הנקראים קצה רווחים שהציב את הצינור המוקדם, כולל.
מאז, האורגן דמוי האנטנה הזה הפך לנושא חם למחקר, בין היתר משום שפגמים בסיליה ראשונית יכולים להוביל לשלל בעיות רפואיות – כל דבר, החל מאובדן שמיעה וחיך שסוע ועד איברים פנימיים של האדם הממוקמים בצד הלא נכון של הגוף. אך שאלה עיקרית שלא נענתה היא אילו רמזים מולקולריים אומרים לתאים ליצור מלכתחילה ציליום ראשוני.
במאמר חדש שפורסם השבוע ב מַדָעביולוגים התפתחותיים של MSK, Yinwen Liang, PhD, ו- Alexandra Joyner, PhD, מדווחים כי הם פתרו חלק מהתעלומה: שני גורמי שעתוק, SP5 ו- SP8, משמשים כמעין מתג כניסה להתחלת היווצרות CILIUM. בתאים ללא סיליום ראשוני, הפעלת גנים אלה עלולה לגרום להם לבנות אחד כזה.
לתוצאות השלכות מיידיות וארוכות טווח על הבנה וטיפול במחלות הנגרמות כתוצאה מסיליה ראשונית חסרה או לא תקינה – המכונה סילופתיות – המשפיעות על 1 מכל 2,000 אנשים ברחבי העולם.
הצבת כלים חדשים לשימוש בלימוד היווצרות סיליום
כאשר ד"ר ליאנג, מדען בכיר במעבדת ג'וינר ולעבר עמית פוסט -דוק במעבדה של קתרין אנדרסון, התחילה לראשונה לחשוב מדוע לסוגי תאים מסוימים יש ציציות ראשוניות ואחרים, היא חשדה שזה היה מקרה של פירוק מועדף – כלומר, תאים חסרי סיליה ראשונית מקדמים באופן פעיל את הפרק של המבנה. בתאים שעושים סיליום ראשוני, אולי כיבוי תהליך הפירוק, כך שהחלבונים יכולים להצטבר וליצור אחד.
אולם לניסויים שנועדו למקד ולחסום פירוק כזה לא השפיעו מעט על נוכחותם או היעדרו של סיליה ראשונית. זה הוביל את ד"ר ליאנג להצטרף עם ד"ר ג'וינר, שמעבדה במכון סלואן קטרינג יש כלים מצוינים ללימוד האופן בו גנים מסדירים תהליכים התפתחותיים. אם הפירוק אינו המפתח, הם חשבו, אז אולי גורמי התמלול שמפעילים גנים ספציפיים או כבויים הם מה שקובע אם תא בונה סיליום ראשוני.
להגיע לשאלה הזו, ד"ר. ליאנג וג'וינר השתמשו לראשונה בשיטה הנקראת רצף RNA של תאים יחיד (SCRNASEQ) כדי לזהות אילו מהגנים המעורבים בהיווצרות ובתפקוד CILIA מופעלים בסוגי תאים עם ובלי CILIA ראשוני. המדענים ניצלו את העובדה שלרוב התאים בעובר העכבר יש ציציות ראשוניות ואילו תאים משק החלמון העכבר העכבר אינם עושים זאת. בעזרת ScrnaseQ הם זיהו יותר ממאה גנים כאלה המתבטאים יותר בתאים מצולפים.
בשלב הבא הם תהו אם אחד מאותם גנים היו מה שנקרא גורמי שעתוק – חלבונים שתפקידם העיקרי מופעל על גנים אחרים. כדי לענות על שאלה זו, הם פנו לטכניקה שנקראה Assay עבור כרומטין נגיש טרנספוזאז עם רצף (ATAC-SEQ), החושף היכן הגנום "פתוח" וניתן "לקרוא אותו" או לתמלול.
בשיטה זו הצליחו המדענים הביתה בשני גנים שהיו סימנים מספרים של גורמי שעתוק. ניתוח נוסף העלה כי שני הגנים הללו, SP5 וכן SP8היו פעילים מאוד בסוגי תאים עם סיליום ראשוני, אך לא פעילים בתאים חסרי אחד.
מציאת הגורמים ש'דלק את כל העניין '
התוצאות הנעימות ביותר הגיעו כאשר הן הפילו את הגנים הללו בתאים עם CILIA או הכניסו אותם לתאים חסרי CILIA. תוצאות אלה הראו זאת SP5 וכן SP8 נדרשו להיווצרות סיליום ראשונית בעובר העכבר המוקדם. יתר על כן, פשוט ביטוי יתר של גן אחד, SP8הספיק בכדי ליזום היווצרות ציליום ראשונית בתאים בלעדיהם.
אם אתה מוסיף SP8 לתאים חוץ -עקביים, רבים מהתאים מייצרים כעת את Cilia. איש מעולם לא ראה את התוצאה הזו לפני כן. "
ד"ר אלכסנדרה ג'וינר, דוקטורט, ביולוג התפתחותי MSK
ד"ר. ליאנג וג'וינר טענו כי שני החלבונים הללו, SP5 ו- SP8, יושבים בראש עץ ההחלטה של התא לייצור סיליה ראשונית. "אנו רואים בזה פריצת דרך גדולה למצוא את גורמי התמלול במעלה הזרם שמדליקים את כל העניין", מוסיף ד"ר ליאנג.
ד"ר ליאנג יעזוב את MSK בקרוב כדי להתחיל במעבדה משלה בסין, שם היא מקווה להמשיך לעבוד על תרגום תגליות בסיסיות אלה לפריצות דרך קליניות לאנשים עם סילופתיות.
"המטרה שלי לטווח הארוך היא לשפר את ההבנה שלנו כיצד נוצרת CILIA ואז להשתמש במידע זה כדי להועיל למחקר הקליני של סיליופתיות", היא אומרת.
ד"ר ג'וינר פרש מ- MSK בתחילת השנה וכעת הוא חבר אמריטוס בפקולטה ל- MSK. קרא עוד על הקריירה הארוכה והמכובדת שלה.